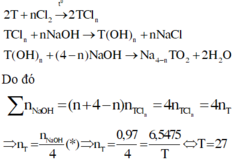Hòa tan hoàn toàn 5,1g oxit kim loại R2O3 vào dung dịch HCl, phản ứng tạo ra 13.35g RCl3 và nước,xác định CTHH của oxit

Những câu hỏi liên quan
Hòa tan hoàn toàn 0,8g một Oxit kim loại (II) vào dung dịch HCl, sau phản ứng thu được 1,9g muối gang. Xác định CTHH của Oxit kim loại trên.
CTHH của oxit : AO
AO + 2HCl -> ACl2 + H2O
A+16.............A + 71
0.8.........................1.9
\(\Rightarrow1.9\cdot\left(A+16\right)=0.8\cdot\left(A+71\right)\)
\(\Rightarrow A=24\)
A là : Mg
CTHH : MgO
Đúng 2
Bình luận (0)
hòa tan hoàn toàn 0,8 gam một oxit kim loại hóa trị II vào dung dịch HCl sau phản ứng thu đc 1,9 gam muối khan xác định CTHH của oxit kim loại gọi tên (cho Al=27,H=1,O=16,S=32,Cl=35,5)
Đặt kim loại hóa trị II là A.
=> Oxit: AO
\(AO+2HCl\rightarrow ACl_2+H_2O\\ n_{AO}=n_A=\dfrac{1,9-0,8}{35,5.2-16}=0,02\left(mol\right)\\ M_{AO}=\dfrac{0,8}{0,02}=40\left(\dfrac{g}{mol}\right)\\ Mà:M_{AO}=M_A+16\left(\dfrac{g}{mol}\right)\\ \Rightarrow M_A+16=40\\ \Leftrightarrow M_A=24\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Magie\left(Mg=24\right)\\ \Rightarrow Oxit:MgO\)
Gọi tên oxit: Magie oxit.
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 10,2g một oxit kim loại cần 331,8g dung dịch H2SO4 vừa đủ. Dung dịch muối sau phản ứng có nồng độ 10%. Xác định CTHH của oxit kim loại.
Gọi oxit kim loại cần tìm là R2On (n là hóa trị của kim loại cần tìm)
R2On +3H2SO4 -----------> R2(SO4)n +3H2O
m dung dịch sau pứ= 10,2 + 331,8 = 342 (g)
C%dd muối = \(\dfrac{m_{R_2\left(SO_{\text{4}}\right)_n}}{342}.100=10\)
=>m R2(SO4)n =34,2 (g)
Ta có : \(n_{R_2O_n}=n_{R_2\left(SO_4\right)_n}\)
=> \(\dfrac{10,2}{2R+16n}=\dfrac{34,2}{2R+96n}\)
Lập bảng :
| n | 1 | 2 | 3 |
| R | 9 | 18 | 27 |
| Kết luận | Loại | Loại | Chọn (Al) |
Vậy CTHH của oxit kim loại là Al2O3
Đúng 3
Bình luận (0)
khử hoàn toàn 8,12g oxit kim loại bằng co ở nhiệt độ cao, sau khi kết thúc phản ứng thu được 3,316 lít khí. Mặt khác nếu lấy lượng kim loại sinh ra hòa tan vào dung dịch HCl dư thì thoát ra 2,352 lít khí H2. Hãy xác định công thức hóa học của oxit kim loại.
Oxit hóa hoàn toàn 6,5475 gam kim loại T bằng Cl2. Sản phẩm sau phản ứng đem hòa tan vào nước thu được dung dịch X. Cho từ từ dung dịch NaOH vào dung dịch X thấy có kết tủa tạo ra, sau đó kết tủa tan vừa hết thì ngừng, thấy đã dùng hết 970 ml dung dịch NaOH 1M. Xác định kim loại T A. Al B. Cr C. Zn D. Be
Đọc tiếp
Oxit hóa hoàn toàn 6,5475 gam kim loại T bằng Cl2. Sản phẩm sau phản ứng đem hòa tan vào nước thu được dung dịch X. Cho từ từ dung dịch NaOH vào dung dịch X thấy có kết tủa tạo ra, sau đó kết tủa tan vừa hết thì ngừng, thấy đã dùng hết 970 ml dung dịch NaOH 1M. Xác định kim loại T
A. Al
B. Cr
C. Zn
D. Be
Hoà tan hoàn toàn 4g oxit ( A là kim loại hoá trị 2) vào 146g dung dịch HCL 10%. Xác định CTHH của kim loại A
Đặt CTTQ oxit AO.
PTHH: AO + 2HCl -> ACl2 + H2O
mHCl=14,6(g) -> nHCl=0,4(mol)
=> nAO=0,4/2=0,2(mol)
=>M(AO)= 4/0,2= 20(g/mol)
=> A là He (mà nó là khí hiếm mà em)
COI LẠI ĐỀ HE
Đúng 2
Bình luận (0)
1/ Hòa tan hoàn toàn 5,1g một oxít kim loại hóa trị III cần dùng 300ml dung dịch HCl 1M, sau phản ứng thu được dung dịch X. a) Xác định tên của kim loại. b) Tính nồng độ mol của dung dịch sau phản ứng
Đọc tiếp
1/ Hòa tan hoàn toàn 5,1g một oxít kim loại hóa trị III cần dùng 300ml dung dịch HCl 1M, sau phản ứng thu được dung dịch X. a) Xác định tên của kim loại. b) Tính nồng độ mol của dung dịch sau phản ứng
a. CT oxit : \(R_2O_3\)
\(R_2O_3+6HCl\rightarrow2RCl_3+3H_2O\\ n_R=\dfrac{1}{6}n_{HCl}=\dfrac{0,3}{6}=0,05\left(mol\right)\\ M_{R_2O_3}=2R+16.3=\dfrac{5,1}{0,05}=102\\ \Rightarrow R=27\left(Al\right)\\ b.n_{AlCl_3}=\dfrac{1}{3}n_{HCl}=0,1\left(mol\right)\\ \Rightarrow CM_{AlCl_3}=\dfrac{0,1}{0,3}=0,33M\)
Đúng 2
Bình luận (0)
nHCl = 0,3.1=0,3(mol)
PTHH: A2O3 + 6HCl --> 2ACl3 + 3H2O
_____0,05<---0,3--------->0,1___________(mol)
=> \(M_{A_2O_3}=\dfrac{5,1}{0,05}=102\left(g/mol\right)\)
=> MA = 27 (g/mol) => A là Al
b) \(C_{M\left(AlCl_3\right)}=\dfrac{0,1}{0,3}=0,33M\)
Đúng 1
Bình luận (0)
Cho 20,16 lít khí CO phản ứng với một lượng oxit MxOy nung nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được 25,2 gam kim loại M và hỗn hợp khí X. Cho toàn bộ lượng hỗn hợp khí X qua bình chứa dung dịch Ca(OH)2 dư tạo ra m gam kết tủa và có 6,72 lít khí thoát ra. Hòa tan hoàn toàn lượng kim loại trên trong dung dịch HCl dư, thấy thoát ra 10,08 lít khí H2. Xác định công thức oxit và tính m. Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Đọc tiếp
Cho 20,16 lít khí CO phản ứng với một lượng oxit MxOy nung nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được 25,2 gam kim loại M và hỗn hợp khí X. Cho toàn bộ lượng hỗn hợp khí X qua bình chứa dung dịch Ca(OH)2 dư tạo ra m gam kết tủa và có 6,72 lít khí thoát ra. Hòa tan hoàn toàn lượng kim loại trên trong dung dịch HCl dư, thấy thoát ra 10,08 lít khí H2. Xác định công thức oxit và tính m. Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.

Đúng 0
Bình luận (0)
Cho 9,4 gam oxit kim loại A có hóa trị I phản ứng hết với dung dịch axit clohidđric HCl, sau phản ứng thu được nước và 14,9 gam muối clorua (tạo bởi kim loại liên kết với clo). Xác định CTHH của oxit kim loại A
\(n_{A_2O}=\dfrac{9,4}{2M_A+16}\left(mol\right)\)
PTHH: A2O + 2HCl --> 2ACl + H2O
\(\dfrac{9,4}{2M_A+16}\)-->\(\dfrac{9,4}{M_A+8}\)
=> \(\dfrac{9,4}{M_A+8}\left(M_A+35,5\right)=14,9\Rightarrow M_A=39\left(g/mol\right)\)
=> A là K
CTHH: K2O
Đúng 2
Bình luận (0)