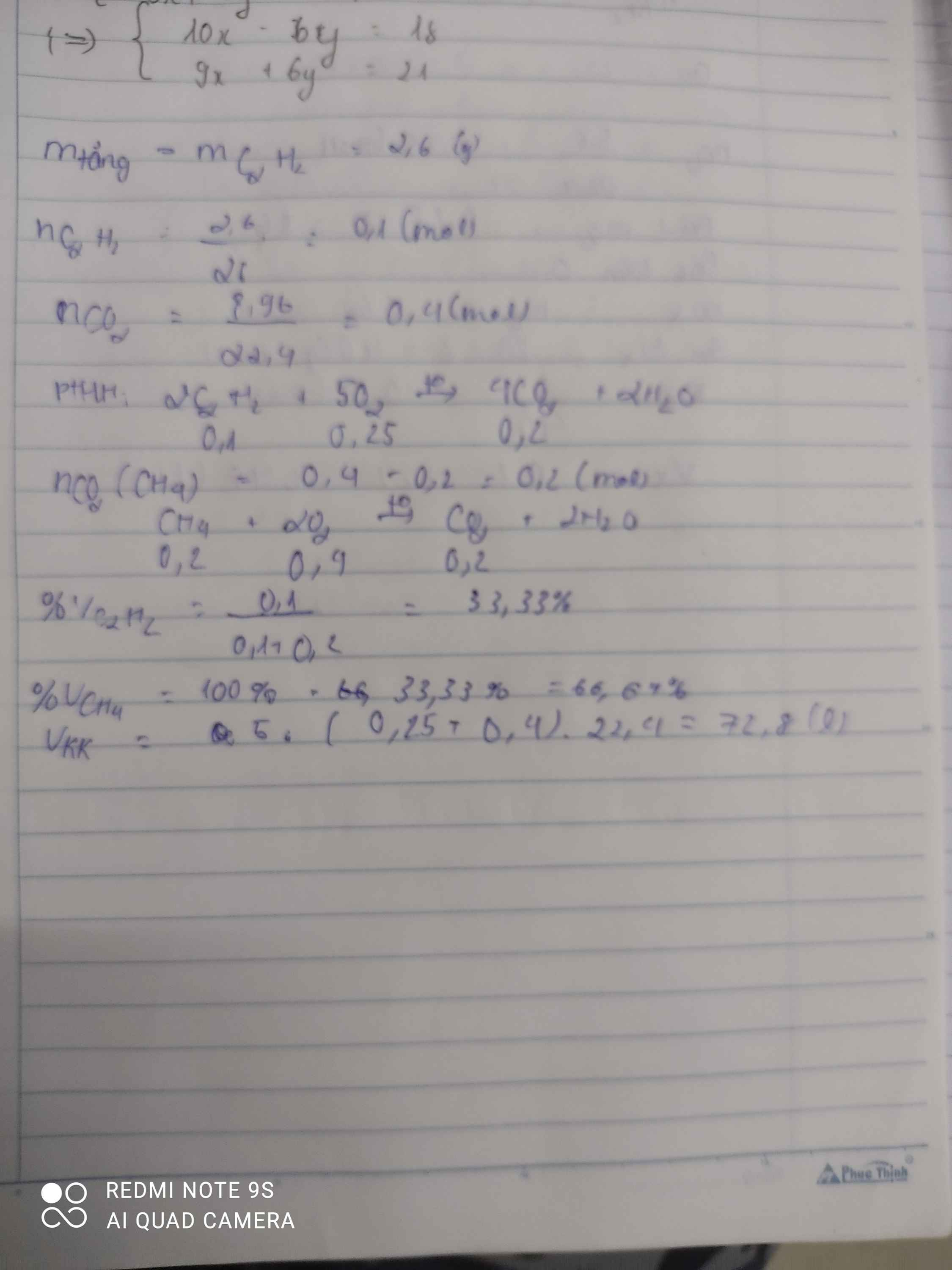Những câu hỏi liên quan
Hidrocacbon (C2H2n+2) có TCHH tương tự axetilen. Cho A vào bình đựng dung dịch brom, sau phản ứng thấy có 0,06 mol brom phản ứng, thu được hai hợp chất hữu cơ và thấy khối lượng bình tăng 1,6 gam. Xác định CTPT của A
Cho 20g hỗn hợp A gồm 3 khí metan, propilen, axetilen lần lượt qua bình 1 đựng dung dịch AgNO3 / NH3 dư, bình 2 đựng dung dịch Br2 dư thấy bình 1 có 48 g kết tủa vàng, bình 2 có 32g brom phản ứng. Viết các phản ứng xảy ra? Tính % thể tích mỗi chất trong hỗn hợp ban đầu?
Cho 20g hỗn hợp A gồm 3 khí metan, propilen, axetilen lần lượt qua bình 1 đựng dung dịch AgNO3/NH3 dư, bình 2 đựng dung dịch Br2 dư thấy bình 1 có 48 g kết g tủa vàng, bình 2 có 32g brom phản ứng. Viết các phản ứng xảy ra? Tính % thể tích mỗi chất trong hỗn hợp ban đầu?
\(C_2H_2+AgNO_3+NH_3->C_2Ag_2+NH_4NO_3\\ CH_2=CH-CH_3+Br_2->CH_2Br-CHBr-CH_3\\ n_{C_2Ag_2}=0,325mol=n_{C_2H_2}\\ m_{C_2H_2}=8,45g\\ n_{Br_2}=n_{C_3H_6}=\dfrac{32}{160}=0,2mol\\ m_{C_3H_6}=8,4g\\ m_{CH_4}=20-8,45-8,4=3,15g\\ n_{CH_4}=0,196875mol\\ n_{hh}=n_{CH_4}+n_{C_2H_2}+n_{C_3H_6}=0,721875mol\\ \%V_{C_3H_6}=\dfrac{0,2}{n_{hh}}.100\%=27,71\%\\ \%V_{C_2H_2}=\dfrac{0,325}{n_{hh}}.100\%=45,02\%\\ \%V_{CH_{_34}}=27,27\%\)
Đúng 1
Bình luận (1)
Dẫn hoàn toàn 6,72 (l) hỗn hợp A gồm C2H6 và C3H6 (đktc) vào 300ml dung dịch Brom vừa đủ phản ứng.Sau khi phản ứng kết thúc thấy khối lượng bình đựng dung dịch Brom tăng 6,3ga)Tính thành phần phần trăm về thể tích mỗi chất trong Ab)Tính nồng độ mol dung dịch Brom cần dùngc)Tính nồng độ mol chất tan có trong dung dịch thu được.(Biết thể tích dung dịch thay đổi không đáng kể).
Đọc tiếp
Dẫn hoàn toàn 6,72 (l) hỗn hợp A gồm C2H6 và C3H6 (đktc) vào 300ml dung dịch Brom vừa đủ phản ứng.Sau khi phản ứng kết thúc thấy khối lượng bình đựng dung dịch Brom tăng 6,3g
a)Tính thành phần phần trăm về thể tích mỗi chất trong A
b)Tính nồng độ mol dung dịch Brom cần dùng
c)Tính nồng độ mol chất tan có trong dung dịch thu được.(Biết thể tích dung dịch thay đổi không đáng kể).
a, PT: \(C_3H_6+Br_2\rightarrow C_3H_6Br_2\)
Ta có: m bình tăng = mC3H6 = 6,3 (g)
\(\Rightarrow n_{C_3H_6}=\dfrac{6,3}{42}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_3H_6}=\dfrac{0,15.22,4}{6,72}.100\%=50\%\\\%V_{C_2H_6}=100-50=50\%\end{matrix}\right.\)
b, Theo PT: \(n_{Br_2}=n_{C_3H_6}=0,15\left(mol\right)\Rightarrow C_{M_{Br_2}}=\dfrac{0,15}{0,3}=0,5\left(M\right)\)
c, Theo PT: \(n_{C_3H_6Br_2}=n_{C_3H_6}=0,15\left(mol\right)\Rightarrow C_{M_{C_3H_6Br_2}}=\dfrac{0,15}{0,3}=0,5\left(M\right)\)
Đúng 1
Bình luận (0)
Cho 3,36 lít hỗn hợp khí gồm metan và axetilen qua bình đựng dung dịch nước brom dư, sau phản ứng thấy thoát ra 2,24 lít khí (đktc) a, Viết phương trình phản ứng xảy ra? b, Tính khối lượng brom tham gia phản ứng? c, Xác định thành phần % thể tích hỗn hợp đầu?
Đọc tiếp
Cho 3,36 lít hỗn hợp khí gồm metan và axetilen qua bình đựng dung dịch nước brom dư, sau phản ứng thấy thoát ra 2,24 lít khí (đktc)
a, Viết phương trình phản ứng xảy ra?
b, Tính khối lượng brom tham gia phản ứng?
c, Xác định thành phần % thể tích hỗn hợp đầu?
\(C_2H_2+2Br_2->C_2H_2Br_4\\ n_{hh}=\dfrac{3,36}{22,4}=0,15mol\\ n_{CH_4}=\dfrac{2,24}{22,4}=0,1mol\\ n_{C_2H_2}=0,05mol\\ n_{Br_2}=2.0,05=0,1mol\\ m_{Br_2}=0,1.160=16g\\ \%V_{CH_4}=\dfrac{0,1}{0,15}.100\%=66,67\%\\ \%V_{C_2H_2}=33,33\%\)
Đúng 1
Bình luận (0)
Cho 5,52 gam hỗn hợp gồm C2H6, C2H4, C3H4 đi qua dung dịch AgNO3/NH3 dư thu được 7,35 gam kết tủa. Khí thoát ra khỏi bình được dẫn vào bình đựng dung dịch Brom dư thấy có 6,4 gam brom phản ứng. % theo khối lượng mỗi chất trong hỗn hợp ban đầu. A. C2H6: 43,48% ; C2H4: 20,29% ; C3H4: 36,23% B. C2H6: 43,23% ; C2H4: 20,29% ; C3H4: 36,48%C. C2H6: 43,48% ; C2H4: 20,23% ; C3H4: 36,29% D. C2H6: 43,29% ; C2H4: 20,48% ; C3H4: 36,23%
Đọc tiếp
Cho 5,52 gam hỗn hợp gồm C2H6, C2H4, C3H4 đi qua dung dịch AgNO3/NH3 dư thu được 7,35 gam kết tủa. Khí thoát ra khỏi bình được dẫn vào bình đựng dung dịch Brom dư thấy có 6,4 gam brom phản ứng. % theo khối lượng mỗi chất trong hỗn hợp ban đầu.
A. C2H6: 43,48% ; C2H4: 20,29% ; C3H4: 36,23% B. C2H6: 43,23% ; C2H4: 20,29% ; C3H4: 36,48%
C. C2H6: 43,48% ; C2H4: 20,23% ; C3H4: 36,29% D. C2H6: 43,29% ; C2H4: 20,48% ; C3H4: 36,23%
\(n_{C_3H_3Ag}=\dfrac{7,35}{147}=0,05\left(mol\right)\)
=> \(n_{C_3H_4}=0,05\left(mol\right)\)
\(n_{Br_2}=\dfrac{6,4}{160}=0,04\left(mol\right)\)
=> \(n_{C_2H_4}=0,04\left(mol\right)\)
=> \(\left\{{}\begin{matrix}\%C_3H_4=\dfrac{0,05.40}{5,52}.100\%=36,23\%\\\%C_2H_4=\dfrac{0,04.28}{5,52}.100\%=20,29\%\\\%C_2H_6=100\%-36,23\%-20,29\%=43,48\%\end{matrix}\right.\)
=> A
Đúng 2
Bình luận (0)
Dẫn 1,68 lít hỗn hợp khí X gồm 2 hidrocacbon mạch hở vào bình đựng dung dịch brom (dư). Sau phản ứng hoàn toàn thấy phản ứng hoàn toàn thấy thoát ra 1,12 lít khí và lượng brom phản ứng là 4 gam. Nếu đốt cháy hoàn toàn 1,68 lít hỗn hợp X thì thu được 2,8 lít CO2. Công thức phân tử của 2 hidrocacbon trong X là: A. CH4 và C2H4. B. CH4 và C3H4. C. CH4 và C3H6. D. C2H6 và C3H6.
Đọc tiếp
Dẫn 1,68 lít hỗn hợp khí X gồm 2 hidrocacbon mạch hở vào bình đựng dung dịch brom (dư). Sau phản ứng hoàn toàn thấy phản ứng hoàn toàn thấy thoát ra 1,12 lít khí và lượng brom phản ứng là 4 gam. Nếu đốt cháy hoàn toàn 1,68 lít hỗn hợp X thì thu được 2,8 lít CO2. Công thức phân tử của 2 hidrocacbon trong X là:
A. CH4 và C2H4.
B. CH4 và C3H4.
C. CH4 và C3H6.
D. C2H6 và C3H6.
Vì sau phản ứng với dung dịch brom dư, có khí thoát ra khỏi bình nên trong hỗn hợp X ban đầu có ankan.

Do đó trong hỗn hợp X có 1 hidrocacbon có số nguyên tử C trong phân tử nhỏ hơn 1,67 và 1 hidrocacbon có số nguyên tử C trong phân tử lớn hơn 1,67.
Mà anken luôn có số nguyên tử C trong phân tử lớn hơn hoặc bằng 2.
Nên ankan trong X có số nguyên tử C nhỏ hơn 1,67.
Suy ra ankan đó là CH4.
Gọi công thức của anken trong X là CnH2n.
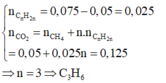
Do đó 2 hidrocacbon trong X là CH4 và C3H6.
Đáp án C.
Đúng 0
Bình luận (0)
Câu 31. Đốt cháy hoàn toàn hỗn hợp X gồm metan và axetilen thu được 8,96 lít khí cacbonđioxit (đktc). Mặt khác khi dẫn hỗn hợp X qua bình đựng dung dịch brom dư, phản ứng xong thấy khối lượng bình đựng dung dịch brom tăng 2,6 gam. a) Tính tỉ lệ phần trăm về thể tích các khí trong hỗn hợp X?b) Tính thể tích không khí cần dùng để đốt cháy hỗn hợp trên?
Đọc tiếp
Câu 31. Đốt cháy hoàn toàn hỗn hợp X gồm metan và axetilen thu được 8,96 lít khí cacbonđioxit (đktc). Mặt khác khi dẫn hỗn hợp X qua bình đựng dung dịch brom dư, phản ứng xong thấy khối lượng bình đựng dung dịch brom tăng 2,6 gam.
a) Tính tỉ lệ phần trăm về thể tích các khí trong hỗn hợp X?
b) Tính thể tích không khí cần dùng để đốt cháy hỗn hợp trên?
\(n_{CO_2}=\dfrac{8,96}{22,4}=0,4mol\)
\(m_{tăng}=m_{Br_2}=m_{C_2H_2}=2,6g\)
\(\Rightarrow n_{C_2H_2}=\dfrac{2,6}{26}=0,1mol\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
0,1 0,1
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_2+\dfrac{5}{2}O_2\underrightarrow{t^o}2CO_2+H_2O\)
0,1 0,25 0,2
\(\Rightarrow n_{CO_2\left(CH_4\right)}=0,4-0,2=0,2mol\)
\(\Rightarrow n_{CH_4}=0,2mol\Rightarrow n_{O_2}=0,4mol\)
a)\(\%V_{CH_4}=\dfrac{0,2}{0,4}\cdot100\%=50\%\)
\(\%V_{C_2H_2}=100\%-50\%=50\%\)
b)\(\Sigma n_{O_2}=0,4+0,25=0,65mol\)
\(\Rightarrow V_{O_2}=0,65\cdot22,4=14,56l\)
\(\Rightarrow V_{kk}=14,56\cdot5=72,8l\)
Đúng 2
Bình luận (4)
cho 6,72 lít khí metan và etilen vào bình đựng dung dịch nước brom thì thấy 32g brom phản ứng a Tính % V mỗi chất ban đầu b đốt cháy toàn bộ hỗn hợp trên rồi dẫn khí thu đc vào bình đựng nước vôi trong. Tính khối lượng kết tủa thu đc
Đọc tiếp
cho 6,72 lít khí metan và etilen vào bình đựng dung dịch nước brom thì thấy 32g brom phản ứng a Tính % V mỗi chất ban đầu b đốt cháy toàn bộ hỗn hợp trên rồi dẫn khí thu đc vào bình đựng nước vôi trong. Tính khối lượng kết tủa thu đc
a)
$C_2H_4 + Br_2 \to C_2H_4Br_2$
$n_{C_2H_4} = n_{Br_2} = \dfrac{32}{160} =0,2(mol)$
$\%V_{C_2H_4} = \dfrac{0,2.22,4}{6,72}.100\% = 66,67\%$
$\%V_{CH_4} = 100\% -66,67\% = 33,33\%$
b)
$n_{CH_4} = 0,1(mol)$
Bảo toàn C :
$n_{CO_2} = n_{CH_4} + 2n_{C_2H_4} = 0,5(mol)$
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
$n_{CaCO_3} = n_{CO_2} = 0,5(mol)$
$m_{CaCO_3} = 0,5.100 = 50(gam)$
Đúng 1
Bình luận (0)