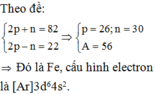Nguyên tử sắt có 82 hạt cơ bản,trong đó số hạt mang điện chiếm 63,4% tổng số hạt. a.Viết kí hiệu nguyên tử b.Viết cấu hình electron nguyên tử sắt

Những câu hỏi liên quan
Nguyên tố X có tổng số hạt cơ bản là 34, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 10
a) Hãy viết kí hiệu nguyên tử của ngtố X
b) Việt cấu hình electron nguyên tử, cấu hình electron theo orbital của X
c) Từ cấu hình electron, dự đoán tính chất hoá học
d) Xác đinh vị trí của X trong bảng tuần hoàn
a, Ta có: P + N + E = 34
Mà: P = E (Do nguyên tử trung hòa về điện.)
⇒ 2P + N = 34 (1)
Theo đề, số hạt mang điện nhiều hơn số hạt không mang điện là 10.
⇒ 2P - N = 10 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}P=E=11=Z\\N=12\end{matrix}\right.\) ⇒ A = 11 + 12 = 23
→ KH: \(^{23}_{11}X\)
b, Cấu hình e: 1s22s22p63s1
Cấu hình e theo orbital:
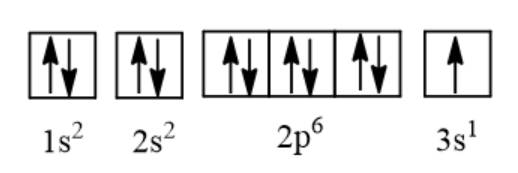
c, X có 1 e hóa trị → tính kim loại
d, - Z = 11 → ô số 11
- Có 3 lớp e → chu kỳ 3
- e cuối cùng phân bố ở phân lớp s, có 1 e hóa trị → nhóm IA
Vậy: X thuộc ô số 11, chu kỳ 3, nhóm IA
Đúng 0
Bình luận (0)
Nguyên tử X có tổng các loại hạt cơ bản là 46, trong đó số hạt mang điện tích nhiều hơn số hạt không mang điện tích là 14 hạt.
a) Tính số p, n, e, A của nguyên tử X. ( Z=15)
b) Viết kí hiệu nguyên tử và cấu hình electron của X.
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Cấu hình electron của X là: A. [Ar]3d44s2 B. [Ar]3d6 C. [Ar]3d54s1 D. [Ar]3d64s2
Đọc tiếp
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Cấu hình electron của X là:
A. [Ar]3d44s2
B. [Ar]3d6
C. [Ar]3d54s1
D. [Ar]3d64s2
Câu 2: Nguyên tử nguyên tố X có tổng số hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Xác định số hiệu nguyên tử, số khối và kí hiệu nguyên tử X.
Tổng số hạt proton, nơtron và electron trong 1 nguyên tử nguyên tố X là 82:
p + e + n = 82 hay 2p + n = 82 (do p = e) (1)
Số hạt mang điện (p và e) nhiều hơn số hạt không mang điện (n) là 22 hạt
(p+e) – n = 22 hay 2p – n = 22 (2)
Giải (1), (2) ta có p = e = 26; n =30
Số khối của X = Z + N = p + n =56
Đúng 1
Bình luận (0)
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Cấu hình electron của ion
X
2
+
là A.
[
Ar
]
3
d
4
4
s
2
B.
[
Ar
]
3
d
6...
Đọc tiếp
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Cấu hình electron của ion X 2 + là
A. [ Ar ] 3 d 4 4 s 2
B. [ Ar ] 3 d 6
C. [ Ar ] 3 d 5 4 s 1
D. [ Ar ] 3 d 6 4 s 1
Tổng số hạt trong nguyên tử của Nguyên tố Y là 34. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 10 a.Tìm các hạt cấu tạo nên nguyên tử của Nguyên tố Y b.Viết kí hiệu nguyên tử Y
a, viết cấu hình electron của các nguyên tử A,B biết rằng:- Tổng số các loại hạt cơ bản trong nguyên tử A là 34. Số hạt mang điện nhiều hơn số hạt không mang điện là 10- số hiệu nguyên tử của B ít hơn số hiệu nguyên tử của A 2 đơn vị. Kí hiệu của nguyên tử B là b, liên kết trong hợp chất tạo thành từ A và B thuộc loại liên kết gì? Vì sao? Viết công thức của hợp chất tạo thành
Đọc tiếp
a, viết cấu hình electron của các nguyên tử A,B biết rằng:
- Tổng số các loại hạt cơ bản trong nguyên tử A là 34. Số hạt mang điện nhiều hơn số hạt không mang điện là 10
- số hiệu nguyên tử của B ít hơn số hiệu nguyên tử của A 2 đơn vị. Kí hiệu của nguyên tử B là b, liên kết trong hợp chất tạo thành từ A và B thuộc loại liên kết gì? Vì sao? Viết công thức của hợp chất tạo thành
\(\begin{cases} 2Z_A+n_A=34\\ 2Z_A-n_A=10 \end{cases} ⇒ \begin{cases} Z_A=11 (Na)\\ n_A=12 \end{cases} \)
\(Z_A-Z_B=2 ⇒ Z_B=9 (F)\)
\(⇒\) Vậy hợp chất AB là NaF, thuộc loại liên kết ion, do Na, F lần lượt là kim loại và phi kim điểm hình.
Đúng 0
Bình luận (0)
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Số hiệu nguyên tử, số khối, tên nguyên tố X và kí hiệu hóa học tương ứng là: A. 27, 60 và tên gọi là coban, kí hiệu hóa học Co. B. 26, 56 và tên gọi là sắt, kí hiệu hóa học Fe. C. 28, 59 và tên gọi là niken, kí hiệu hóa học Ni. D. 29, 63 và tên gọi là đồng, kí hiệu hóa học Cu.
Đọc tiếp
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Số hiệu nguyên tử, số khối, tên nguyên tố X và kí hiệu hóa học tương ứng là:
A. 27, 60 và tên gọi là coban, kí hiệu hóa học Co.
B. 26, 56 và tên gọi là sắt, kí hiệu hóa học Fe.
C. 28, 59 và tên gọi là niken, kí hiệu hóa học Ni.
D. 29, 63 và tên gọi là đồng, kí hiệu hóa học Cu.
Đáp án B
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 82 → 2p + n = 82
Số hạt mang điện nhiều hơn số hạt không mang điện là 22 → 2p - n =22
→ p= 26 và n = 30
→ Số hiệu nguyên tử của X là 26, số khối là 56. Tên nguyên tố sắt( Fe)
Đúng 1
Bình luận (0)
tổng số hạt cơ bản trong nguyên tử X là 40 trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 20 xác định kí hiệu nguyên tử X xác định số lớp electron của nguyên tử X
Z=(S+a)/4=(40+20)/4=15 suy ra photpho. Photpho có 3 lớp e. Lớp thứ nhất có 2 e, lớp thứ 2 có 8 e, lớp thứ 3 có 5 e.
Đúng 0
Bình luận (0)