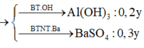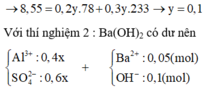Tính số mol các ion có trong : a) 100ml dung dịch HNO3 0.25M b) 200ml dung dịch Ba(OH)2 0,15M c) 200ml dung dịch AL2(SO4)3 0.2M

Những câu hỏi liên quan
Tính số mol, nồng độ mol ion H+ và OH- và pH của dung dịch axit b) HNO3 0,04M c) dung dịch HCl 0.001M d) dung dịch H2SO4 0,003M e) dung dịch HNO3 có pH=2 f) dung dịch H2SO4 có pH=4 g) 200ml dung dịch H2SO4 0,01M + 100ml dung dịch HCl 0,05M Giúp em với ạ
1)Trộn lẫn 100ml dung dịch K2SO4 0,5M và 200ml dung dịch Fe2(SO4)3 0,1M và với 100ml dung dịch MgCl2 0,2M. Tính nồng độ mol/l của các ion trong dung dịch sau cùng.2) Một dung dịch KOH có nồng độ mol/l ion OH- gấp 4 lần trong dung dịch Ba(OH)2 0,1M.a) Tính nồng độ dung dịch KOH.b) Nếu trộn mỗi dung dịch 200ml với nhau thì được dung dịch mơi có nồng độ ion OH- bao nhiêu?
Đọc tiếp
1)Trộn lẫn 100ml dung dịch K2SO4 0,5M và 200ml dung dịch Fe2(SO4)3 0,1M và với 100ml dung dịch MgCl2 0,2M. Tính nồng độ mol/l của các ion trong dung dịch sau cùng.
2) Một dung dịch KOH có nồng độ mol/l ion OH- gấp 4 lần trong dung dịch Ba(OH)2 0,1M.
a) Tính nồng độ dung dịch KOH.
b) Nếu trộn mỗi dung dịch 200ml với nhau thì được dung dịch mơi có nồng độ ion OH- bao nhiêu?
Trộn lẫn 200ml dung dịch NaOH 1M với 100ml dung dịch HNO3 0,5 M thì thu được dung dịch D a) Tính nồng độ mol của các ion có trong dung dịch D b) tính thể tích dung dịch H2SO4 1M để trung hòa hoàn toàn dung dịch D
a) \(n_{NaOH}=0,2.1=0,2\left(mol\right)\); \(n_{HNO_3}=0,2.0,5=0,1\left(mol\right)\)
\(NaOH+HNO_3\rightarrow NaNO_3+H_2O\)
0,2.............0,1
Lập tỉ lệ : \(\dfrac{0,2}{1}>\dfrac{0,1}{1}\) => Sau phản ứng NaOH dư
Dung dịch D gồm NaNO3 và NaOH dư
\(n_{NaNO_3}=n_{HNO_3}=0,1\left(mol\right)\)
\(n_{NaOH\left(pứ\right)}=n_{HNO_3}=0,1\left(mol\right)\)
\(n_{NaOH\left(dư\right)}=0,2-0,1=0,1\left(mol\right)\)
Ion trong dung dịch D : Na+ , NO3-, OH-
\(\left[Na^+\right]=\dfrac{0,1+0,1}{0,2}=1M\)
\(\left[NO_3^-\right]=\dfrac{0,1}{0,2}=0,5M\)
\(\left[OH^-\right]=\dfrac{0,1}{0,2}=0,5M\)
b)Trong dung dịch D chỉ có NaOH dư phản ứng
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+H_2O\)
0,1................0,05
=> \(V_{H_2SO_4}=\dfrac{0,05}{1}=0,05\left(l\right)\)
Đúng 1
Bình luận (0)
X là dung dịch Al2(SO4)3, Y là dung dịch Ba(OH)2. Trộn 200ml dung dịch X với 300ml dung dịch Y thu được 8,55 gam kết tủa. Trộn 200ml dung dịch X với 500ml dung dịch Y thu được 12,045 gam kết tủa. Nồng độ mol/l của dung dịch X là A. 0,075M B. 0,100M C. 0.150M D. 0.050M
Đọc tiếp
X là dung dịch Al2(SO4)3, Y là dung dịch Ba(OH)2. Trộn 200ml dung dịch X với 300ml dung dịch Y thu được 8,55 gam kết tủa. Trộn 200ml dung dịch X với 500ml dung dịch Y thu được 12,045 gam kết tủa. Nồng độ mol/l của dung dịch X là
A. 0,075M
B. 0,100M
C. 0.150M
D. 0.050M
câu 1: cho 100ml dung dịch chứ 5,85g NaCl; 5,6g KOH; 11,1g CaCl. tính nồng đọ mol của các chất trong dung dịch
câu 2:
a) cho 200ml dung dịch Ba(OH)2 1,5M. tính số mol Ba(oh)2
b) cho 200g dung dịch ãit có chứa 0,2 mol HCl và 0,1 mol H2SO4. tính nồng đọ % moiõ ãit trong dung dịch
Câu 1:
\(n_{NaCl}=\dfrac{5,85}{58,5}=0,1\left(mol\right)\Rightarrow C_{M_{ddNaCl}}=\dfrac{0,1}{0,1}=1M\)
\(n_{KOH}=\dfrac{5,6}{56}=0,1\left(mol\right)\Rightarrow C_{M_{ddKOH}}=\dfrac{0,1}{0,1}=1M\)
\(n_{CaCl_2}=\dfrac{11,1}{111}=0,1\left(mol\right)\Rightarrow C_{M_{ddCaCl_2}}=\dfrac{0,1}{0,1}=1M\)
Đúng 1
Bình luận (0)
Câu 2:
a,\(n_{Ba\left(OH\right)_2}=0,2.1,5=0,3\left(mol\right)\)
b,\(C\%_{ddHCl}=\dfrac{0,2.36,5.100\%}{200}=3,65\%\)
\(C\%_{ddH_2SO_4}=\dfrac{0,1.98.100\%}{200}=4,9\%\)
Đúng 1
Bình luận (0)
Tính nồng độ các ion trong a) dung dịch Al2(SO4)3 0,2M b) dung dịch MgCl2 0,15M
a, \(\left[Al^{3+}\right]=0,2.2=0,4\left(M\right)\)
\(\left[SO_4^{2-}\right]=0,2.3=0,6\left(M\right)\)
b, \(\left[Mg^{2+}\right]=0,15.1=0,15\left(M\right)\)
\(\left[Cl^-\right]0,15.2=0,3\left(M\right)\)
Đúng 1
Bình luận (0)
Có 100ml dung dịch S chứa các ion: H+ (x mol), Cl-(0,1 mol), SO42-(0,15 mol) và có 200ml dung dịch B chứa các ion: Na+ (0,2 mol), Ba2+ (0,2 mol), và OH- (y mol).a) Xác định x,y.b) Để trung hòa 100ml dung dịch A trên phải cần bao nhiêu ml dung dịch B?c) Trộn 100ml dung dịch A với 100ml dung dịch B sẽ thu được bao nhiêu gam muối không tan?
Đọc tiếp
Có 100ml dung dịch S chứa các ion: H+ (x mol), Cl-(0,1 mol), SO42-(0,15 mol) và có 200ml dung dịch B chứa các ion: Na+ (0,2 mol), Ba2+ (0,2 mol), và OH- (y mol).
a) Xác định x,y.
b) Để trung hòa 100ml dung dịch A trên phải cần bao nhiêu ml dung dịch B?
c) Trộn 100ml dung dịch A với 100ml dung dịch B sẽ thu được bao nhiêu gam muối không tan?
Bài : Tính số mol của các ion trong các dung dịch sau: A)200 ml dung dịch Al2(SO4)3 28,5% (có d = 1,2 g/ml). B)100 ml dung dịch chứa hỗn hợp HCl 3M và HNO3 1M.
a) \(m_{ddAl_2\left(SO_4\right)_3}=200\cdot1,2=240\left(g\right)\)
\(\Rightarrow m_{Al_2\left(SO_4\right)_3}=\dfrac{240\cdot28,5}{100}=68,4\left(g\right)\)
\(\Rightarrow n_{Al_2\left(SO_4\right)_3}=0,2mol\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Al^{3+}}=2n_{Al_2\left(SO_4\right)_3}=0,4mol\\n_{SO^{2-}_4}=0,6mol\end{matrix}\right.\)
b) \(n_{HCl}=0,1\cdot3=0,3mol\) \(\Rightarrow n_{Cl^-}=0,3mol\)
\(n_{HNO_3}=0,1\cdot1=0,1mol\) \(\Rightarrow n_{NO^-_3}=0,1mol\)
\(\Sigma n_{H^+}=n_{HCl}+n_{HNO_3}=0,3+0,1=0,4mol\)
Đúng 1
Bình luận (0)
Tính nồng độ các ion có trong dung dịch các trường hợp sau
a) 2 lít dung dịch có hòa tan 0,5 mol K2SO4
b) trộn lẫn 200ml dung dịch KOH 1M với 100ml dung dịch HCl 1M được dung dịch X
c) trộn 0,5 ml dung dịch ba(oh)2 0,5 M với 1 lít dung dịch HNO3 0,1 M và HCl 0, 05M thu được dung dịch D
a, \(K_2SO_4\rightarrow2K^++SO_4^{2-}\)
___0,5_______1______0,5_ (mol)
\(\Rightarrow\left\{{}\begin{matrix}\left[K^+\right]=\frac{1}{2}=0,5M\\\left[SO_4^{2-}\right]=\frac{0,5}{2}=0,25M\end{matrix}\right.\)
b, Ta có: \(n_{OH^-}=n_{K^+}=n_{KOH}=0,2.1=0,2\left(mol\right)\)
\(n_{H^+}=n_{Cl^-}=0,1.1=0,1\left(mol\right)\)
PT ion: \(OH^-+H^+\rightarrow H_2O\)
______0,2_____0,1_________ (mol)
⇒ OH- dư. ⇒ nOH- (dư) = 0,1 (mol)
Dd X gồm: K+; Cl- và OH-(dư).
\(\Rightarrow\left\{{}\begin{matrix}\left[K^+\right]=\frac{0,2}{0,3}=\frac{2}{3}M\\\left[Cl^-\right]=\frac{0,1}{0,3}=\frac{1}{3}M\\\left[OH^-\right]_{\left(dư\right)}=\frac{0,1}{0,3}=\frac{1}{3}M\end{matrix}\right.\)
c, Ta có: \(\left\{{}\begin{matrix}n_{Ba^{2+}}=n_{Ba\left(OH\right)_2}=0,0005.0,5=0,00025\left(mol\right)\\n_{OH^-}=2n_{Ba\left(OH\right)_2}=2.0,0005.0,5=0,0005\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\Sigma n_{H^+}=n_{HNO_3}+n_{HCl}=1.0,1+1.0,05=0,15\left(mol\right)\\n_{NO_3^-}=n_{HNO_3}=1.0,1=0,1\left(mol\right)\\n_{Cl^-}=n_{HCl}=1.0,05=0,05\left(mol\right)\end{matrix}\right.\)
PT ion: \(OH^-+H^+\rightarrow H_2O\)
____0,0005____0,15_________ (mol)
⇒ H+ dư. ⇒ nH+ (dư) = 0,1495 (mol)
Dd D gồm: Ba2+; NO3-; Cl- và H+(dư)
\(\Rightarrow\left\{{}\begin{matrix}\left[Ba^{2+}\right]=\frac{0,00025}{1,0005}\approx2,5.10^{-4}M\\\left[NO_3^-\right]=\frac{0,1}{1,0005}\approx0,09M\\\left[Cl^-\right]=\frac{0,05}{1,0005}\approx0,049M\\\left[H^+\right]_{\left(dư\right)}=\frac{0,1495}{1,0005}\approx0,15M\end{matrix}\right.\)
Bạn tham khảo nhé!
Mà phần c số lẻ quá, không biết đề là 0,5 ml hay 0,5 lít bạn nhỉ?