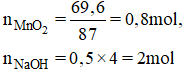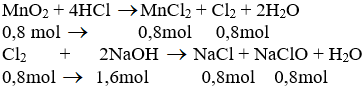9. Cho 40g CaO vào 500ml dung dịch HCl 0.3M . Tính Cm của dung dịch thu được sau phản ứng, biết thể tích CaO không đáng kể

Những câu hỏi liên quan
9. Cho 40g CaO vào 500ml dung dịch HCl 0.3M . Tính Cm của dung dịch thu được sau phản ứng, biết thể tích CaO không đáng kể9. Cho 40g CaO vào 500ml dung dịch HCl 0.3M . Tính Cm của dung dịch thu được sau phản ứng, biết thể tích CaO không đáng kể
Hoà tan 40g MgO vào 500 ml dung dịch HCl 1M Tính nồng độ mol của các chất có trong dung dịch thu được sau phản ứng Giả sử thể tích của dung dịch thay đổi không đáng kể
Xem chi tiết
Ta có: \(n_{MgO}=\dfrac{40}{40}=1\left(mol\right)\)
\(n_{HCl}=0,5.1=0,5\left(mol\right)\)
PT: \(MgO+2HCl\rightarrow MgCl_2+H_2O\)
Xét tỉ lệ: \(\dfrac{1}{1}< \dfrac{0,5}{2}\), ta được MgO dư.
Theo PT: \(n_{MgCl_2}=\dfrac{1}{2}n_{HCl}=0,25\left(mol\right)\)
\(\Rightarrow C_{M_{MgCl_2}}=\dfrac{0,25}{0,5}=0,5\left(M\right)\)
Đúng 4
Bình luận (0)
10. Cho 10g CaCO3 vào 500ml dung dịch HCl 0,5M .Tính Cm của các chất trong dung dịch thu được, biết thể tích CaCO3 không đáng kể
10. Cho 10g CaCO3 vào 500ml dung dịch HCl 0,5M .Tính Cm của các chất trong dung dịch thu được, biết thể tích CaCO3 không đáng kể
PTHH: \(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{CaCO_3}=\dfrac{10}{100}=0,1\left(mol\right)\\n_{HCl}=0,5\cdot0,5=0,25\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,25}{2}\) \(\Rightarrow\) HCl còn dư
\(\Rightarrow\left\{{}\begin{matrix}n_{CaCl_2}=0,1\left(mol\right)\\n_{HCl\left(dư\right)}=0,05\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{CaCl_2}}=\dfrac{0,1}{0,5}=0,2\left(M\right)\\C_{M_{HCl\left(dư\right)}}=\dfrac{0,05}{0,5}=0,1\left(M\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Cho 5,475 g HCl vào 500ml Ca(OH)2 0,2 M Thu được dung dịch A thể tích thay đổi không đáng kể a Viết phương trình phản ứng xảy ra B Tính CM các chất sau phản ứng
2HCl+Ca(OH)2->CaCl2+2H2O
0,15------0,075-----0,075-----0,15
n HCl=\(\dfrac{5,475}{36,5}\)=0,15 mol
n Ca(OH)2=0,2.0,5 =0,1 mol
=>Ca(OH)2 dư
CM Ca(OH)2 dư =\(\dfrac{0,025}{0,5}\)=0,05M
CM CaCl2 = \(\dfrac{0,075}{0,5}\)=0,15 M
Đúng 1
Bình luận (0)
cho 10g cuo vào 500ml dung dịch hcl vừa đủ. a)viết pthh b) tính cu của muối trong dung dịch thu được( giả sử thể tích thay đổi không đáng kể) c) tính cm( hcl) đã dùng
a,\(n_{CuO}=\dfrac{10}{80}=0,125\left(mol\right)\)
PTHH: CuO + 2HCl → CuCl2 + H2
Mol: 0,125 0,25 0,125
b,\(m_{CuCl_2}=0,125.135=16,875\left(g\right)\Rightarrow m_{Cu}=\dfrac{64.16,875}{135}=8\left(g\right)\)
c,\(C_{M_{ddHCl}}=\dfrac{0,25}{0,5}=0,5M\)
Đúng 0
Bình luận (1)
Hoà tan 28g sắt bằng dung dịch HCL 2M vừa đủ a , tính thể tích dung dịch HCL cần dùng b , tính thể tích khí thoát ra ở điều kiện tiêu chuẩn c , tính CM dung dịch thu được sau phản ứng coi thể tích dung dịch sau phản ứng thay đôi không đáng kể so với thể tích HCL đã dùng
a,\(n_{Fe}=\dfrac{28}{56}=0,5\left(mol\right)\)
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,5 1 0,5 0,5
\(V_{ddHCl}=\dfrac{1}{2}=0,5\left(l\right)\)
b,\(V_{H_2}=0,5.22,4=11,2\left(l\right)\)
c,\(C_{M_{ddFeCl_2}}=\dfrac{0,5}{0,5}=1M\)
Đúng 2
Bình luận (0)
Cho 69,6g MnO2 tác dụng với dung dịch HCl đặc dư thu được một lượng khí X. Dẫn khí X vào 500ml dung dịch NaOH 4M thu được dung dịch A. Tính nồng độ mol của các chất trong dung dịch A. Giả thiết rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.
a) Phương trình hóa học của phản ứng:
b) Theo pt (1): nCl2 = nMnCl2 = nMnO2 = 0,8 mol
Theo pt (2): nNaCl = nNaClO = nCl2 = 0,8 mol
nNaOH pư = 2. nCl2 = 2. 0,8 = 1,6 mol
⇒ nNaOH dư = 2 - 1,6 = 0,4 mol
Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM (NaCl) = CM (NaClO) = CM(MnCl2) = 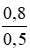
CM (NaOH)dư = 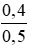
tích cho mình nha![]()
Đúng 2
Bình luận (0)
Cho 250ml dung dịch H2SO4 1,5M phản ứng với 37,8g Na2SO3 thì thu được V( l ) khí SO2 (đktc)
a Viết PTHH
b Tính thể tích SO2 thu được
c Tính CM các chất dung dịch sau phản ứng ( biết thể tích dung dịch sau pư thay đổi không đáng kể )
250ml = 0,25l
\(n_{H2SO4}=1,5.0,25=0,375\left(mol\right)\)
\(n_{Na2SO3}=\dfrac{37,8}{126}=0,3\left(mol\right)\)
a) Pt : \(H_2SO_4+Na_2SO_3\rightarrow Na_2SO_4+SO_2+H_2O|\)
1 1 1 1 1
0,375 0,3 0,3 0,3
b) Lập tỉ số so sánh : \(\dfrac{0,375}{1}>\dfrac{0,3}{1}\)
⇒ H2SO4 dư , Na2SO3 phản ứng hết
⇒ Tính toán dựa vào số mol của Na2SO3
\(n_{SO2}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
\(V_{SO2\left(dktc\right)}=0,3.22,4=6,72\left(l\right)\)
c) \(n_{Na2SO4}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
\(n_{H2SO4\left(dư\right)}=0,375-0,3=0,075\left(mol\right)\)
\(C_{M_{Na2SO4}}=\dfrac{0,3}{0,25}=1,2\left(M\right)\)
\(C_{M_{H2SO4\left(dư\right)}}=\dfrac{0,075}{0,25}=0,3\left(M\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)