Cho 24g hỗn hợp MgO và CaCO3 tác dụng vừa đủ với 500ml dd HCl 1,2M thu được V lit khí ở đktc. V có giá trị bao nhiêu?
2.Cho Mg tác dụng vừa đủ với 250ml dd HCl 1M thu được V(lit) khí H2 (đktc). Vậy V có giá trị là:
nHCl = 0.25*1=0.25 (mol)
Mg + 2HCl => MgCl2 + H2
.........0.25.......................0.125
VH2 = 0.125*22.4=2.8(l)
\(n_{HCl}=0,25.1=0,25\left(mol\right)\)
PTHH: Mg + 2HCl → MgCl2 + H2
Mol: 0,25 0,125
\(\Rightarrow V_{H_2}=0,125.22,4=2,8\left(l\right)\)
Câu 1. Cho 25,2 gam hỗn hợp (Na,CO; CaCO3 MgCO,) tác dụng vừa đủ với 250ml dung dịch H,SO, loãng nồng độ 1M. sau phản ứng thu được m gam muối và V (lit) khí (đktc). Tính m; V?
Câu 2. Hỗn hợp X nặng m gam gồm Al,03; CuO; Fe,O, tác dụng vừa đủ với 500ml dung dịch H,SO, loãng nồng độ 0,75M. sau phản ứng thu được 58,5 gam hỗn hợp muối. Tính giá trị của m?
Câu 1:
Ta có: \(n_{H_2SO_4}=0,25.1=0,25\left(mol\right)\)
PT: \(Na_2CO_3+H_2SO_4\rightarrow Na_2SO_4+H_2O+CO_2\)
\(CaCO_3+H_2SO_4\rightarrow CaSO_4+H_2O+CO_2\)
\(MgCO_3+H_2SO_4\rightarrow MgSO_4+H_2O+CO_2\)
Theo PT, có: \(n_{H_2O}=n_{CO_2}=n_{H_2SO_4}=0,25\left(mol\right)\)
\(\Rightarrow V_{CO_2}=0,25.22,4=5,6\left(l\right)\)
Theo ĐLBT KL, có: mhh + mH2SO4 = m muối + mH2O + mCO2
⇒ m muối = mhh + mH2SO4 - mH2O - mCO2
= 25,2 + 0,25.98 - 0,25.18 - 0,25.44
= 34,2 (g)
Bạn tham khảo nhé!
Câu 2:
Ta có: \(n_{H_2SO_4}=0,5\cdot0,75=0,375\left(mol\right)=n_{H_2O}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{H_2SO_4}=0,375\cdot98=36,75\left(g\right)\\m_{H_2O}=0,375\cdot18=6,75\left(g\right)\end{matrix}\right.\)
Bảo toàn khối lượng: \(m_{oxit}=m_{muối}+m_{H_2O}-m_{H_2SO_4}=28,5\left(g\right)\)
Không biết Fe,O, là chất gì bạn nhỉ?
Cho m gam hỗn hợp A gồm Al , Fe và Zn tác dụng vừa đủ V lit dung dịch HCl 2M . Sau phản ứng người ta thu được 11 , 2 lit khí H2 ( ở đktc ) . Giá trị của V là ?
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
Bảo toàn nguyên tố H : \(n_{HCl}.1=n_{H_2}.2\\ \Rightarrow n_{HCl}=0,5.2=1\left(mol\right)\\ \Rightarrow V_{HCl}=\dfrac{1}{2}=0,5\left(lít\right)\)
nHCl.1=nH2.2⇒nHCl=0,5.2=1(mol)⇒VHCl=12=0,5(lít)
Acid + Muối → Acid (mới) + Muối (mới)
Acid mạnh + Muối tan → Acid mới + Muối (mới)
Điều kiện phản ứng:Các chất tạo thành phải có ít nhất một chất kết tủa hoặc dễ bay hơi hay dễ phân huỷ, hoặc yếu hơn so với chất tham gia (đối với acid).
Acid (mới) có thể mạnh hơn acid cũ nếu muối (mới) là: CuS, HgS, Ag2S, PbS, CdS
Ví dụ:
H2SO4 + BaCl2 → BaSO4 (kết tủa) + 2 HCl
2 HNO3 + K2S → 2 KNO3 + H2S (bay hơi)
6 HCl + Cu3(PO4)2 → 3 CuCl2 + 2 H3PO4 (yếu hơn HCl)
Ba(NO3)2 + H2SO4 → BaSO4↓ + 2 HNO3
Cho 19,02 gam hỗn hợp Mg, Ca, CaO, MgO, MgCO3, CaCO3 tác dụng với dung dịch HCl vừa đủ, thu được 4,704 lít hỗn hợp khí (đktc) có tỉ khối so với H2 là 12,5 và dung dịch chứa 12,825 gam MgCl2 và m gam CaCl2. Giá trị của m là
Gọi \(\left\{{}\begin{matrix}n_{H_2}=a\left(mol\right)\\n_{CO_2}=b\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}a+b=\dfrac{4,704}{22,4}=0,21\\\overline{M}=\dfrac{2a+44b}{a+b}=12,5.2=25\end{matrix}\right.\)
=> a = 0,095 (mol); b = 0,115 (mol)
Đặt nHCl = x (mol)
\(n_{MgCl_2}=\dfrac{12,825}{95}=0,135\left(mol\right)\)
Bảo toàn Cl: \(n_{CaCl_2}=\dfrac{x-0,27}{2}\left(mol\right)\)
Bảo toàn H: \(n_{H_2O}=\dfrac{x-2.0,095}{2}=\dfrac{x-0,19}{2}\left(mol\right)\)
BTKL:
\(m_{hh\left(bđ\right)}+m_{HCl}=m_{MgCl_2}+m_{CaCl_2}+m_{H_2}+m_{CO_2}+m_{H_2O}\)
=> \(19,02+36,5x=12,825+\dfrac{x-0,27}{2}.111+0,095.2+0,115.44+\dfrac{x-0,19}{2}.18\)
=> x = 0,63 (mol)
=> \(n_{CaCl_2}=0,18\left(mol\right)\)
=> mCaCl2 = 0,18.111 = 19,98 (g)
Cho 38,04 gam hỗn hợp Mg, Ca, MgO, CaO, MgCO3, CaCO3 tác dụng với dung dịch HCl vừa đủ thu được 9,408 lít hỗn hợp khí (đktc) có tỉ khối so với H2 là 12,5 và dung dịch chứa 25,65 gam MgCl2 và m gam CaCl2. Giá trị của m là
A. 39,96
B. 38,85
C. 37,74
D. 41,07
Đáp án A
n khí = 0,42 mol
nMgCl2 = 0,27 mol
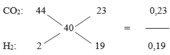
Quy đổi hỗn hợp đầu về: Ca (x mol), Mg (0,27 mol), C (0,23 mol), O (y mol)
m hỗn hợp = 40x+0,27.24+0,23.12+16y = 38,04 (1)
BT e: 2nCa + 2nMg + 4nC = 2nO + 2nH2 => 2x + 0,27.2 + 0,23.4 = 2y + 0,19.2 (2)
Giải (1) và (2) => x = 0,36; y = 0,9
=> mCaCl2 = 0,36.111 = 39,96 gam
Cho 19,02 gam hỗn hợp Mg, Ca, CaO, MgO, MgCO3, CaCO3 tác dụng với dung dịch HCl vừa đủ thu được 4,704 lít hỗn hợp khí (đktc) có tỉ khối so với H2 là 12,5 và dung dịch chứa 12,825 gam MgCl2 và m gam CaCl2. Giá trị của m là
A. 18,78
B. 19,425
C. 20,535
D. 19,98
Cho 38,04 gam hỗn hợp Mg, Ca, MgO, CaO, MgCO3, CaCO3 tác dụng với dung dịch HCl vừa đủ thu được 9,408 lít hỗn hợp khí (đktc) có tỉ khối so với H2 là 12,5 và dung dịch chứa 25,65 gam MgCl2 và m gam CaCl2. Giá trị của m là
A. 39,96.
B. 38,85.
C. 37,74.
D. 41,07.
Giải thích:
n khí = 0,42 mol
nMgCl2 = 0,27 mol
CO2: 44 23 0,23
25 =
H2: 2 19 0,19
Quy đổi hỗn hợp đầu về: Ca (x mol), Mg (0,27 mol), C (0,23 mol), O (y mol)
m hỗn hợp = 40x+0,27.24+0,23.12+16y = 38,04 (1)
BT e: 2nCa + 2nMg + 4nC = 2nO + 2nH2 => 2x + 0,27.2 + 0,23.4 = 2y + 0,19.2 (2)
Giải (1) và (2) => x = 0,36; y = 0,9
=> mCaCl2 = 0,36.111 = 39,96 gam
Đáp án A
Cho 19,02 gam hỗn hợp Mg, Ca, CaO, MgO, MgCO3, CaCO3 tác dụng với dung dịch HCl vừa đủ, thu được 4,704 lít hỗn hợp khí (đktc) có tỉ khối so với H2 là 12,5 và dung dịch chứa 12,825 gam MgCl2 và m gam CaCl2. Giá trị của m là
A. 20,535
B. 18,78
C. 19,425
D. 19,98
Cho 38,04 gam hỗn hợp Mg, Ca, MgO, CaO, MgCO3, CaCO3 tác dụng với dung dịch HCl vừa đủ thu được 9,408 lít hỗn hợp khí (đktc) có tỉ khối so với H2 là 12,5 và dung dịch chứa 25,65 gam MgCl2 và m gam CaCl2. Giá trị của m là
A. 39,96.
B. 38,85.
C. 37,74.
D. 41,07.
Đáp án A
n khí = 0,42 mol
nMgCl2 = 0,27 mol
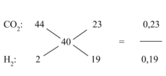
Quy đổi hỗn hợp đầu về: Ca (x mol), Mg (0,27 mol),
C (0,23 mol), O (y mol)
m hỗn hợp = 40x+0,27.24+0,23.12+16y = 38,04 (1)
BT e: 2nCa + 2nMg + 4nC = 2nO + 2nH2
=> 2x + 0,27.2 + 0,23.4 = 2y + 0,19.2 (2)
Giải (1) và (2) => x = 0,36; y = 0,9
=> mCaCl2 = 0,36.111 = 39,96 gam