Câu9: Nguyên tử của nguyên tố R có tổng số hạt p.n,e bằng 18. Số hạt không mang điện bằng trung bình cộng của tổng số hạt mang điện. Tính Số khối của nguyên tử X và viết kí hiệu nguyên tử X.

Những câu hỏi liên quan
Nguyên tử của nguyên tố R có tổng số hạt p, n, e bằng 18 và tổng số hạt không mang điện bằng trung bình cộng của tổng số hạt mang điện. Vậy số electron độc thân của nguyên tử R là
A. 1
B. 2
C. 3
D. 4
Vì trong nguyên tử số hạt electron bằng số hạt proton nên trong R có số hạt proton, notron và electron lần lượt là Z, N và Z.
Theo giả thiết đề bài ta có:
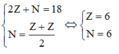
Khi đó cấu hình electron của R là 1s22s22p2.
Do đó số electron độc thân của R là 4.
Đáp án D
Đúng 0
Bình luận (0)
Nguyên tử của nguyên tố R có tổng số hạt p, n, e bằng 18 và tổng số hạt không mang điện bằng trung bình cộng của tổng số hạt mang điện. Vậy số electron độc thân của nguyên tử R là A. 1 B. 2 C. 3 D. 4
Đọc tiếp
Nguyên tử của nguyên tố R có tổng số hạt p, n, e bằng 18 và tổng số hạt không mang điện bằng trung bình cộng của tổng số hạt mang điện. Vậy số electron độc thân của nguyên tử R là
A. 1
B. 2
C. 3
D. 4
Đáp án D
Vì trong nguyên tử số hạt electron bằng số hạt proton nên trong R có số hạt proton, notron và electron lần lượt là Z, N và Z.
Theo giả thiết đề bài ta có: 2 Z + N = 18 N = Z + Z 2 ⇔ Z = 6 N = 6
Khi đó cấu hình electron của R là 1s22s22p2.
Do đó số electron độc thân của R là 4.
Đúng 0
Bình luận (0)
Nguyên tử của nguyên tố R có tổng số hạt p, n, e bằng 18. Số hạt không mang điện bằng trung bình cộng của tổng số hạt mang điện. Vậy số electron độc thân của nguyên tử R là
A. 1
B. 2
C. 3
D. 4
Đáp án B.
Tổng số các loại hạt proton, nơtron và electron của R là 18
p + n + e = 18 => 2p + n = 18 (1)
Số hạt không mang điện bằng trung bình cộng của tổng số hạt mang điện
n = (p+e)/2 hay n = p = e (2)
Từ (1), (2) ta có p = e = n =6
Cấu hình e của R : 1s2 2s2 2p2. Số electron độc thân = 2
Đúng 0
Bình luận (0)
Nguyên tử của nguyên tố X có tổng số hạt p, n và e bằng 82, biết tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 22 hạt. Xác định Z và viết kí hiệu nguyên tử của nguyên tố X. b tính số nguyên tử y trong 4gam y2o3
Theo đề có hệ phương trình:
\(\left\{{}\begin{matrix}2p+n=82\\2p-n=22\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}p=e=26\\n=30\end{matrix}\right.\)
Z: 26
Kí hiệu nguyên tử của nguyên tố X: Fe
b. Đề khác rồi=)
Đúng 1
Bình luận (1)
`a)`
Tổng hạt là `2p+n=82(1)`
Số hạt mang điện hơn không mang điện là `22.`
`->2p-n=22(2)`
`(1)(2)->p=e=26;n=30`
`->Z=p=26;A=26+30=56`
`->X:\ Fe`
KHNT: \(_{26}^{56}Fe\)
` b)`
`n_{Fe_2O_3}=4/{160}=0,025(mol)`
`->n_{Fe}=2n_{Fe_2O_3}=0,05(mol)`
`->` Số nguyên tử `Fe` là `0,05.6,022.10^{23}=3,011.10^{22}`
Đúng 1
Bình luận (0)
Nguyên tử của nguyên tố X có tổng số hạt p, n và e bằng 82, biết tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 22 hạt. Xác định Z và viết kí hiệu nguyên tử của nguyên tố X.
Ta lập HPT: \(\left\{{}\begin{matrix}p+n+e=82\\p+e-n=22\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}2p+n=82\\2p-n=22\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}p=Z=26\\n=30\end{matrix}\right.\)
Kí hiệu nguyên tử: Zn
Đúng 1
Bình luận (0)
Tổng số hạt p,n,e có trong một loại nguyên tử của nguyên tố X là 54 , trong đó tổng số hạt mang điện gấp số hạt không mang điện là 1,7 lần . Hãy xác định số hiệu nguyên tử , số khối và viết kí hiệu nguyên tử X
Nguyên tử Nguyên tố X:
+) 2P + N= 54 (1)
Mặt khác: (2) 2P=1,7N
Từ (1), (2) ta dễ dàng lập hpt :
\(\left\{{}\begin{matrix}2P+N=54\\2P=1,7N\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=E=Z=17\\N=20\end{matrix}\right.\)
=> Số hiệu nguyên tử: Z=17
Số khối: A=N+P=20+17=37
KH nguyên tử X: \(^{37}_{17}Cl\)
Đúng 2
Bình luận (0)
Gọi số hạt p, n, e trong X lần lượt là P, N, E
Có: P + N + E = 54
Mà: P = E (Do nguyên tử trung hòa về điện.)
⇒ 2P + N = 54 (1)
Theo đề bài: Số hạt mang điện gấp số hạt không mang điện là 1,7 lần.
⇒ 2P = 1,7N (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}P=E=17\\N=20\end{matrix}\right.\)
⇒ Nguyên tố X có Z = 17, A = 37
Kí hiệu: \(^{37}_{17}X\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (2)
Tổng số hạt cơ bản trong ngyên tử X bằng 52 . Số hạt mang điện nhiều hơn số hạt không mang điện 16 hạt
a. Viết kí hiệu nguyên tử X
b. Nguyên tố A có 2 đồng vị X và Y . Tổng số hạt trong Y nhiều hơn trong X là 2 hạt . Xác định nguyên tử khối trung bình của A biết X chiếm 75% số nguyên tử
một nguyên tử x có tổng số hạt là 40 hạt mang điện nhỏ hơn hạt không mang điện là 1 tìm e số p số n và viết kí hiệu tính khối lượng bằng gram của một nguyên tử x
có tổng số hạt là 40 hạt
⇒2e + n =40 (1)
số hạt mang điện âm ít hỏn số hạt ko mag điện lá 1
⇒n - e = 1 (2)
từ (1) và (2)⇒\(\left\{{}\begin{matrix}\text{e=13}\\n=14\end{matrix}\right.\)
⇒X là Al
Đúng 0
Bình luận (0)
Nguyên tử của nguyên tố X có tổng số hạt là 49. Số hạt không mang điện bằng 53,125% số hạt mang điện. Kí hiệu nguyên tử của nguyên tố X là
Có p+n+e = 49
=> 2p + e = 49
Có \(\dfrac{n}{2p}.100\%=53,125\%\)
=> p = e = 16; n = 17
=> X là S (lưu huỳnh)
Đúng 1
Bình luận (1)





















