Cần dùng ? lít H2 ( dktc) để phản ứng hết với 1,6 CuO ở nhiệt độ cao
giúp mình với mình cần gấp lắm :<<
người ta dùng CO khử o,3 mol fe3o4 và dùng khí hidro để khử 0,15 mol CuO ở nhiệt độ cao a, tính số lít CO và H2 ở đktc cần dùng cho mỗi phản ứng b, tính số gam sắt và đồng thu được ở mỗi phản ứng
\(Fe_3O_4+4CO\rightarrow\left(t^o\right)3Fe+4CO_2\)
0,3 0,225 ( mol )
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,15 0,15 ( mol )
\(V_{CO}=n.22,4=0,2.22,4=6,72l\)
\(V_{H_2}=n.22,4=0,15.22,4=3,36l\)
\(m_{Fe}=n.M=0,225.56=12,6g\)
\(m_{Cu}=n.M=0,15.64=9,6g\)
Để hòa tan hoàn toàn 28,8 gam hỗn hợp A gồm Fe3O4, Fe2O3, FeO và Fe cần vừa đủ 180 gam dung dịch HCl 18,25%. Sau phản ứng thu được V lít khí H2 và dung dịch B. Cho toàn bộ lượng H2 sinh ra tác dụng hết với CuO dư ở nhiệt độ cao, sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 1,6 gam.
a) Nếu cô cạn dung dịch B thì thu được bao nhiêu gam muối khan.
b) Nếu hỗn hợp A ban đầu tỉ lệ mol Fe2O3 : FeO = 1:1. Tính nồng độ phần trăm của mỗi chất có trong dung dịch B.
dùng 11,2 lít H2(đktc) để khử 48 gam CuO ở nhiệt độ cao. Sau phản ứng được 41,6 gam chất rắn tính hiejeu suất phản ứng tính % thể tích h2 đã phản ứng % khối lượng CuO đã phản ứng
\( CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\\ n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\ n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\\ Vì:\dfrac{0,5}{1}< \dfrac{0,6}{1}\Rightarrow CuO\left(dư\right)\Rightarrow Tính.theo.n_{H_2}\\ Đặt:a=n_{CuO\left(p.ứ\right)}\\ m_{rắn}=41,6\left(g\right)\\ \Leftrightarrow64a+80.\left(0,6-a\right)=41,6\\ \Leftrightarrow a=0,4\left(mol\right)\\ n_{CuO\left(LT\right)}=n_{H_2}=0,5\left(mol\right)\\ \Rightarrow H=\dfrac{n_{CuO\left(TT\right)}}{n_{CuO\left(LT\right)}}.100\%=\dfrac{0,4}{0,5}.100=80\%\)
Thể tích H2 phản ứng: 11,2 (lít) (đề bài)
\( \%m_{CuO\left(p.ứ\right)}=\dfrac{0,4}{0,6}.100\%=66,667\%\) (Do số mol tỉ lệ thuận với khối lượng)
Hoà tan hoàn toàn 57,6 gam hỗn hợp X gồm , Fe 2 O 3 , FeO và Fe trong dung dịch HCl thì cần dùng 360 gam dung dịch HCl 18,25% để tác dụng vừa đủ. Sau phản ứng thu được V lít khí H 2 và dung dịch Y.
Cho toàn bộ H 2 sinh ra tác dụng hết với CuO dư ở nhiệt độ cao, sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 3,2 gam. Nếu cô cạn dung dịch Y thì thu được bao nhiêu gam muối khan ?
n HCl = 360 x 18,25/(100x36,5) = 1,8 mol
H 2 + CuO → t ° Cu + H 2 O
n CuO = x
Theo đề bài
m CuO (dư) + m Cu = m CuO (dư) + m Cu p / u - 3,2
m Cu = m Cu p / u - 3,2 => 64x = 80x - 3,2
=> x= 0,2 mol → m H 2 = 0,4g
Fe + 2HCl → FeCl 2 + H 2
Số mol HCl tác dụng với Fe 3 O 4 , Fe 2 O 3 , FeO là 1,8 - 0,4 = 1,4 mol
Phương trình hóa học của phản ứng:
Fe 3 O 4 + 8HCl → 2 FeCl 3 + FeCl 2 + 4 H 2 O (1)
Fe 2 O 3 + 6HCl → 2 FeCl 3 + 3 H 2 O (2)
FeO + 2HCl → FeCl 2 + H 2 O (3)
Qua các phản ứng (1), (2), (3) ta nhận thấy n H 2 O = 1/2 n HCl = 1,4:2 = 0,7 mol
Áp dụng định luật bảo toàn khối lượng, ta có:
m hỗn hợp + m HCl = m muối + m H 2 O + m H 2
57,6 + 1,8 x 36,5 = m muối + 0,7 x 18 +0,4
m muối = 57,6 + 65,7 - 12,6 - 0,4 = 110,3 (gam)
Khử m gam bột CuO bằng khí H2 ở nhiệt độ cao thu được hỗn hợp chất rắn X. Để hòa tan hết X cần vừa đủ 1 lít dung dịch HNO3 1M, thu được 4,48 lít NO (đktc). Hiệu suất của phản ứng khử CuO bằng bao nhiêu?
A. 70%
B. 75%
C. 80%
D. 85%
CuO + H2 \(-^{t^o}\rightarrow\) Cu + H2O (1)
3Cu + 8HNO3 \(\rightarrow\) 3Cu(NO3)2 + 2NO + 4H2O (2)
CuO + 2HNO3 \(\rightarrow\) Cu(NO3)2 + 2NO + 4H2O (3)
Ta có : nNO = 0,2 mol.
Theo (2) :\( n_{Cu}=\frac{3}{2}n_{NO}=0,3\) mol ; \(n_{HNO_{3}}=\frac{8}{3}n_{NO}=0,8 (mol).\)
Theo (3) : \(n_{CuO}=\frac{1}{2}n_{HNO_{3}}=\frac{1}{2}(1-0,8)=0,1(mol).\)
=> nCuO ban đầu = 0,1 + 0,3 = 0,4 (mol)
Hiệu suất của quá trình khử CuO là :\( H = \frac{0,3}{0,4}.100=75%.\)
=> Chọn B.
Khử m gam bột CuO bằng khí H2 ở nhiệt độ cao thu được hỗn hợp chất rắn X. Để hòa tan hết X cần vừa đủ 1 lít dung dịch HNO3 1M, thu được 4,48 lít NO (đktc). Hiệu suất của phản ứng khử CuO bằng bao nhiêu?
A. 70%
B. 75%
C. 80%
D. 85%
Đáp án B
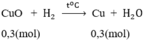
Số mol HNO3: nHNO3 = 1. 1 = 1(mol)
Số mol NO: 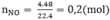
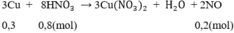
Theo pt: nHNO3 = 4. nNO = 4. 0,2 = 0,8 mol
nHNO3 còn lại = 1 – 0,8 = 0,2 (mol)
⇒ CuO dư phản ứng với HNO3
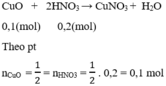
⇒ Tổng nCuO = 0,1 + 0,3 = 0,4 mol
Ban đầu 0,4 mol CuO, phản ứng 0,3 mol CuO
Hiệu suất 
Cho luồng khí H2 dư đi qua ống thủy tinh chứa 20 gam bột CuO ở nhiệt độ cao theo phương trình phản ứng như sau: CuO + H2 Cu + H2O. Sau phản ứng thu được 12 gam chất rắn. Hiệu suất của phản ứng là:
A. 75%.
B. 85%.
C. 90%.
D. 95%.
Mọi người giúp mình với!![]()
Ta có: \(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
Gọi: nCuO (pư) = x (mol) ⇒ nCuO (dư) = 0,25 - x (mol)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Theo PT: \(n_{Cu}=n_{CuO\left(pư\right)}=x\left(mol\right)\)
Chất rắn gồm: Cu và CuO dư.
⇒ 64x + 80.(0,25 - x) = 12 ⇒ x = 0,5 > nCuO ban đầu
→ vô lý
Bạn xem lại đề nhé.
\(n_{CuO}=\dfrac{20}{80}=0,25mol\\ CuO+H_2\xrightarrow[]{t^0}Cu+H_2O\\ n_{Cu\left(LT\right)}=n_{CuO}=0,25mol\\ m_{Cu\left(LT\right)}=0,25.64=16g\\ H=\dfrac{12}{16}\cdot100\%=70\%\\ \Rightarrow A\)
câu 1:cho 5,4 gam Al phản ứng hoàn tòn với dung dịch H2So4 loãng
a) tính VH2(dktc) thu đc sau phản ứng
b) dùng khí h2 thu đc ở trên khử hoàn toàn CuO ở nhiệt độ cao tính khối lượng Cu thu đc sau phản ứng(hiệu suất của p/u đạt 80%)
câu 2:cho các chất có cthh:KOH,CuCl2,Al2O3,ZnSO4,CuO,Zn(OH)2,H3PO4,N2O5,KHSO4,H2CO3.Hãy phân loại và gọi tên các chất
\(C1\\ n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.0,2=0,3\left(mol\right)\\ a,V_{H_2\left(đktc\right)}=0,3.22,4=6,72\left(l\right)\\ b,H_2+CuO\rightarrow\left(t^o\right)Cu+H_2O\\ n_{Cu\left(LT\right)}=n_{H_2}=0,3\left(mol\right)\\ n_{Cu\left(TT\right)}=n_{Cu\left(LT\right)}.H=0,3.80\%=0,24\left(mol\right)\\ m_{Cu\left(TT\right)}=0,24.80=19,2\left(g\right)\)
- Oxit:
+ Oxit bazo: Al2O3 (Nhôm oxit), CuO (Đồng (II) oxit)
+ Oxit axit: N2O5 (dinito pentaoxit)
- Axit:
H2CO3 (Axit cacbonic), H3PO4 (axit photphoric)
- Bazo:
KOH (Kali hidroxit), Zn(OH)2 (Kẽm hidroxit)
- Muối:
KHSO4 (Kali hidrosunfat), CuCl2 (Đồng (II) clorua), ZnSO4 (Kẽm sunfat)
Dùng 1,2 lít (đo ở đktc) khí Hidro khử CuO ở nhiệt độ cao. Sau phản ứng thu được Đồng và hơi nước.
a) Tính khối lượng Cuo bị khử
b) Tính khối lượng Cu được tạo thành
c) Lượng H2 trên có thể bị đốt cháy với bao nhiêu lít O2 (đo ở đktc)
Sửa đề: 1,2 (l) → 1,12 (l)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Ta có: \(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Theo PT: \(n_{Cu}=n_{CuO}=n_{H_2}=0,05\left(mol\right)\)
a, \(m_{CuO}=0,05.80=4\left(g\right)\)
b, \(m_{Cu}=0,05.64=3,2\left(g\right)\)
c, PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{H_2}=0,025\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,025.22,4=0,56\left(l\right)\)