cho 10 gam hỗn hợp gồm một muối clorua của kim loại kiềm và FeCl3 tác dụng với dd AgNO3 dư, thu được 28,7g kết tủa Xác định công thức và tính thành phần % khối lượng muối clorua của kim loại kiềm trong hỗn hợp

Những câu hỏi liên quan
Cho hỗn hợp X gồm NaCl và muối clorua của kim loại kiềm M. Cho 4,73g hỗn hợp X đó tác dụng với lượng dư dung dịch AgNO3 thì thu được 14,35g kết tủa. Hỏi trong hỗn hợp X chứa muối clorua của kim loại kiềm nào cùn với NaCl
Hòa tan hòa toàn 6,645g hỗn hợp muối clorua của hai kim loại kiềm thuộc hai chu kì liên tiếp nhau vào nước được dd X. Cho toàn bộ dd X tác dụng hoàn toàn với dd AgNO3 (dư), thu được 18,655g kết tủa. Hai kim loại kiềm trên là A. Na, K B. Rb, Cs C. Li , Na D. K , Rb
Đọc tiếp
Hòa tan hòa toàn 6,645g hỗn hợp muối clorua của hai kim loại kiềm thuộc hai chu kì liên tiếp nhau vào nước được dd X. Cho toàn bộ dd X tác dụng hoàn toàn với dd AgNO3 (dư), thu được 18,655g kết tủa. Hai kim loại kiềm trên là
A. Na, K
B. Rb, Cs
C. Li , Na
D. K , Rb
Đáp án C
![]()
nAgCl = 18,655/143,5 = 0,13
⇒ M= 6,645/ 0,13 - 35,5 = 15,61
⇒ M1 = 9 (Li) < 15,61 < M2 = 23(Na)
Đúng 0
Bình luận (0)
Cho m gam hỗn hợp muối clorua của một kim loại kiềm và một kim loại kiềm thổ tác dụng vừa đủ với dung dịch AgNO3 thu được 7,175 gam kết tủa đồng thời khối lượng dung dịch giảm 3,83 g
a Tính m (biết hai muối được trộn theo tỉ lệ mol 3:1)
b) khối lượng nguyên tử kim loại kiềm kiếm kim loại kiềm thổ 1u. xác định công thức 2 muối
Bài này khó quá ai giúp với!!!
BTKL:
m dung dịch giảm= m kết tủa - =3,83 \(\rightarrow\) m=7,175 -3,83=3,345 gam
Hỗn hợp muối gồm ACl và BCl2
\(ACl+AgNO_3\rightarrow AgCl+ANO_3\)
\(BCl_2+2AgNO_3\rightarrow2AgCl+B\left(NO_3\right)_2\)
\(n_{AgCl}=\frac{7,175}{143,5}=0,05\left(mol\right)\)
Ta có: nACl=3nBCl2
Mà \(n_{ACl}+2n_{Cl2}=0,05\left(mol\right)\rightarrow n_{ACl}=0,03\left(mol\right),n_{BCl2}=0,01\left(mol\right)\)
\(\rightarrow0,03\left(A+35,5\right)+0,01\left(B+35,5.2\right)=3,345\rightarrow0,03A+0,01B=1,57\)
Nếu A-B=1\(\rightarrow\) A=39,5; B=38,5
Nếu B-A=1 \(\rightarrow\) A=39; B=40
Vậy A là K; B là Ca
\(\rightarrow\) 2 muối là KCl và CaCl2
Hỗn hợp X gồm M2CO3, MHCO3, MCl (M là kim loại kiềm). Hòa tan hoàn toàn 30,15 gam hỗn hợp X trong V ml dung dịch HCl 10,52% (D 1,05g/ml) thu được dung dịch Y và 5,6 lít CO2 (đktc). Chia Y thành 2 phần bằng nhau. – Phần 1: tác dụng vừa đủ với 100 ml dung dịch KOH 1M thu được m gam muối. – Phần 2: tác dụng hoàn toàn với dung dịch AgNO3 dư thu được 50,225 gam kết tủa. a. Xác định tên kim loại M. b. Tính thành phần phần trăm theo khối lượng của từng chất trong hỗn hợp X. c. Tính V và m.
Đọc tiếp
Hỗn hợp X gồm M2CO3, MHCO3, MCl (M là kim loại kiềm). Hòa tan hoàn toàn 30,15 gam hỗn hợp X trong V ml dung dịch HCl 10,52% (D = 1,05g/ml) thu được dung dịch Y và 5,6 lít CO2 (đktc). Chia Y thành 2 phần bằng nhau.
– Phần 1: tác dụng vừa đủ với 100 ml dung dịch KOH 1M thu được m gam muối.
– Phần 2: tác dụng hoàn toàn với dung dịch AgNO3 dư thu được 50,225 gam kết tủa.
a. Xác định tên kim loại M.
b. Tính thành phần phần trăm theo khối lượng của từng chất trong hỗn hợp X.
c. Tính V và m.
Hòa tan hoàn toàn 6,645 gam hỗn hợp muối clorua của hai kim loại kiềm thuộc hai chu kì kế tiếp nhau vào nước được dung dịch X. Cho toàn bộ dung dịch X tác dụng hoàn toàn với dung dịch AgNO3 (dư), thu được 18,655 gam kết tủa. Tìm 2 kim loại kiềm
A. Na, K
B. Li, Be
C. Li, Na
D. K, Rb
Đáp án C
Hướng dẫn Ta có: ![]()
![]() Cl + AgNO3 →
Cl + AgNO3 → ![]() NO3 + AgCl
NO3 + AgCl
0,13 mol 0,13 mol
=> (![]() + 35,5).0,13 = 6,645 →
+ 35,5).0,13 = 6,645 → ![]() = 15,62
= 15,62
Mà 2 kim loại kiềm thuộc hai chu kì kế tiếp nhau → Li (7) và Na(23)
Đúng 0
Bình luận (0)
Hoà tan hoàn toàn 6,645 gam hỗn hợp muối clorua của hai kim loại kiềm thuộc hai chu kì kế tiếp nhau vào nước được dung dịch X. Cho toàn bộ dung dịch X tác dụng hoàn toàn với dung dịch AgNO3 (dư), thu được 18,655 gam kết tủa. Hai kim loại kiềm trên là A. Na và K B. Rb và Cs C. K và Rb D. Li và Na
Đọc tiếp
Hoà tan hoàn toàn 6,645 gam hỗn hợp muối clorua của hai kim loại kiềm thuộc hai chu kì kế tiếp nhau vào nước được dung dịch X. Cho toàn bộ dung dịch X tác dụng hoàn toàn với dung dịch AgNO3 (dư), thu được 18,655 gam kết tủa. Hai kim loại kiềm trên là
A. Na và K
B. Rb và Cs
C. K và Rb
D. Li và Na
MCl + AgNO3 -> AgCl + MNO3 (M là hai kim loại kiềm)
mol: 0,13 0,13
Ta có : (M+35,5).0,13 = 6,645
=> M = 15,62
Hai kim loại kiềm trên là Li và Na.
=> Đáp án D
Đúng 0
Bình luận (0)
Cho dung dịch chứa 6,595 gam muối clorua của kim loại kiềm thuộc hai chu kì liên tiếp và dung dịch AgNO3 (dư), thu được 15,785 gam kết tủa. Phần trăm khối lượng của muối có khối lượng phân tử nhỏ là: A. 92,719% B. 11,296% C. 7,281% D. 88,704%
Đọc tiếp
Cho dung dịch chứa 6,595 gam muối clorua của kim loại kiềm thuộc hai chu kì liên tiếp và dung dịch AgNO3 (dư), thu được 15,785 gam kết tủa. Phần trăm khối lượng của muối có khối lượng phân tử nhỏ là:
A. 92,719%
B. 11,296%
C. 7,281%
D. 88,704%
Đáp án D
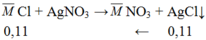
![]()
![]()
![]()
Ta có :
a +b = 0,11 (1)
58,5a + 74,5b = 6,595 (2)
⇒ a = 0,1 , b = 0,01
⇒ % m NaCl = 0,1.58,5.100% / 6,595 = 88,7%
Đúng 0
Bình luận (0)
Hoàn tan 4,25gam một muối clorua của kim loại kiềm M vào nước được 200ml dung dịch X. Lấy 10ml dung dịch X cho phản ứng với một lượng dư dung dịch AgNO3 thu được 0,7175g kết tủa. Xác định công thức muối đã dùng và nồng độ mol/l của dung dịch X?
Xem chi tiết
Cứ 10ml dd X phản ứng với dd AgNO3 dư tạo 0,7175 g kết tủa
\(\Rightarrow\) Với 200ml dd X phản ứng với dd AgNO3 dư tạo \(0,7175\cdot20=14,35\left(g\right)\) kết tủa
PTHH: \(RX+AgNO_3\rightarrow RNO_3+AgX\downarrow\)
Theo phương trình: \(n_{RX}=n_{AgX}\) \(\Rightarrow\dfrac{4,25}{R+X}=\dfrac{14,35}{108+X}\)
Ta thấy với \(\left\{{}\begin{matrix}R=7\\X=35,5\end{matrix}\right.\) thì phương trình trên thỏa mãn
\(\Rightarrow\) Muối cần tìm là LiCl (0,1 mol) \(\Rightarrow C_{M_{LiCl}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
Đúng 1
Bình luận (0)
Có hh Q gồm kim loại M(có hóa trị II trong hợp chất)oxit và muối clorua của M.Cho20,2g hỗn hợp Q vào dd HCL dư thu đc dd Q1 và 5,6 lít khí H2 (đktc).Lấy toàn bộ dd Q1 cho tác dụng với dd NaOH dư thu đc kết tủa O2.Nung kết tủa O2 đến khối lượng ko đổi thu đc 22g chất rắn.Nếu cũng lấy 20,2g hỗn hợp Q cho vào 300ml dd CuCL2 1M,sau khi phản ứng xong,lọc bỏ chất rắn,làm khô dd thu đc 34,3g muối khan.Giả thiết các phản ứng xảy ra hoàn toàn.Biết rằng kim loại M,oxit của nó ko tan và ko tác dụng với nướ...
Đọc tiếp
Có hh Q gồm kim loại M(có hóa trị II trong hợp chất)oxit và muối clorua của M.Cho20,2g hỗn hợp Q vào dd HCL dư thu đc dd Q1 và 5,6 lít khí H2 (đktc).Lấy toàn bộ dd Q1 cho tác dụng với dd NaOH dư thu đc kết tủa O2.Nung kết tủa O2 đến khối lượng ko đổi thu đc 22g chất rắn.Nếu cũng lấy 20,2g hỗn hợp Q cho vào 300ml dd CuCL2 1M,sau khi phản ứng xong,lọc bỏ chất rắn,làm khô dd thu đc 34,3g muối khan.Giả thiết các phản ứng xảy ra hoàn toàn.Biết rằng kim loại M,oxit của nó ko tan và ko tác dụng với nước ở điều kiện thường ,muối clorua của M tan hoàn toàn trong nước,kim loại M hoạt động hóa học hơn Cu.
a)Viết các pthh và xác định kim loại M
b)Tính thành phần phần trăm về khối lượng các chất trong hỗn hợp Q















