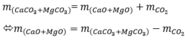Nung 26g hỗn hợp gồm MgCO3 và MgO thu được 15g MgO. Tính thành phần % theo khối lượng của mỗi chất trong hỗn hợp ban đầu.

Những câu hỏi liên quan
Bài 5 : Cho 10,4g hỗn hợp gồm : MgO, MgCO3 tác dụng vừa đủ với 200ml dd acid CH3COOH thì thu đc 2,479 lít khí CO2 (đkc)
a) Tính thành phần % về khối lượng mỗi chất trong hỗn hợp ban đầu
b) Tính nồng độ mol dd CH3COOH cần dùng
a, \(n_{CO_2}=\dfrac{2,479}{24,79}=0,1\left(mol\right)\)
PT: \(MgO+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+H_2O\)
\(MgCO_3+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+CO_2+H_2O\)
Theo PT: \(n_{MgCO_3}=n_{CO_2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{MgCO_3}=\dfrac{0,1.84}{10,4}.100\%\approx80,77\%\\\%m_{MgO}\approx19,23\%\end{matrix}\right.\)
b, \(n_{MgO}=\dfrac{10,4-0,1.84}{40}=0,05\left(mol\right)\)
Theo PT: \(n_{CH_3COOH}=2n_{MgO}+2n_{MgCO_3}=0,3\left(mol\right)\)
\(\Rightarrow C_{M_{CH_3COOH}}=\dfrac{0,3}{0,2}=1,5\left(M\right)\)
Đúng 2
Bình luận (0)
Nung nóng hỗn hợp CaCO3 và MgCO3 đến khối lượng không đổi thu được khối lượng chất rắn bằng 1/2 khối lượng hỗn hợp ban đầu xác định thành phần phần trăm theo khối lượng các chất trong hỗn hợp ban đầu
CaCO3=>CaO+CO2
..x.................x
MgCO3=>MgO+CO2
y..................y
100x+84y=m
56x+40y=m/2
=> 100x+84y=112x+80y ,<=>12x=4y =>x:y=1:3
%CaCO3=100/(100+3.84).100=28,409%=>MgC...
Đúng 1
Bình luận (0)
Nung hỗn hợp X gồm
C
a
C
O
3
và
M
g
C
O
3
theo phản ứng :
C
a
C
O
3
→
t
°
C
a
O
+
C
O
2
M
g
C
O
3
→
t
°
M
g...
Đọc tiếp
Nung hỗn hợp X gồm C a C O 3 và M g C O 3 theo phản ứng :
C a C O 3 → t ° C a O + C O 2
M g C O 3 → t ° M g O + C O 2
Nếu đem nung 31,8 gam hỗn hợp X thì thu được 7,84 lít C O 2 (đktc). Tính khối lượng của hỗn hợp của oxit thu được.
khi phân hủy bằng nhiệt 14,2 gam hỗn hợp X gồm CaCO3 và MgCO3 ta thu được chất rắn Y gồm CaO và MgO và 6,6 gam CO2. Tính thành phần % khối lượng các chất trong hỗn hợp X.
Gọi số mol CaCO3, MgCO3 là a, b (mol)
=> 100a + 84b = 14,2 (1)
\(n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)\)
PTHH: CaCO3 --to--> CaO + CO2
a-------------------->a
MgCO3 --to--> MgO + CO2
b---------------------->b
=> a + b = 0,15
=> a = 0,1; b = 0,05
=> \(\left\{{}\begin{matrix}\%m_{CaCO_3}=\dfrac{100.0,1}{14,2}.100\%=70,42\%\\\%m_{MgCO_3}=\dfrac{0,05.84}{14,2}.100\%=29,58\%\end{matrix}\right.\)
Đúng 4
Bình luận (0)
\(n_{CO_2}=\dfrac{6,6}{44}=0,15mol\)
\(CaCO_3\underrightarrow{t^o}CO_2+CaO\)
\(x\) \(\rightarrow\) \(x\)
\(MgCO_3\underrightarrow{t^o}MgO+CO_2\)
\(y\) \(\rightarrow\) \(y\)
\(\Rightarrow\left\{{}\begin{matrix}100x+84y=14,2\\x+y=0,15\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
\(\%m_{CaCO_3}=\dfrac{0,1\cdot100}{14,2}\cdot100\%=70,42\%\)
\(\%m_{MgCO_3}=100\%-70,42\%=29,57\%\)
Đúng 4
Bình luận (0)
Cho hỗn hợp A gồm Mgo và MgoCo3 tác dụng hết với dd H2So4 5 phần trăm sau pứ thu được 11,2 lít hỗn hợp khí (đktc).a)viết pthh xảy ra.b)tính khối lượng dd H2so4 5phan tram đã dùng.c)tính kl mỗi chất trong hỗn hợp A.Biết mgco3 tác và mgo trong A được trộn theo tỉ lệ kl là : 7:3
Xem chi tiết
a/ \(n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(MgCO_3+H_2SO_4\rightarrow MgSO_4+H_2O+CO_2\)
\(0,5---0,5----0,5---0,5-0,5\)
\(MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
\(b---b----b-----b\)
\(\Rightarrow m_{MgCO_3}=0,5.\left(24+12+16.3\right)=42\left(g\right)\)
\(\dfrac{m_{MgCO_3}}{m_{MgO}}=\dfrac{7}{3}\Rightarrow m_{MgO}=42.\dfrac{3}{7}=18\left(g\right)\Rightarrow n_{MgO}=b=0,45\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4}=0,45+0,5=0,95\left(mol\right)\) \(\Rightarrow m_{dd}=\dfrac{0,95.98}{0,05}=1862\left(g\right)\)
Đúng 1
Bình luận (0)
Bài 3: Nung hỗn hợp 2 muối CaCO3 và MgCO3 thu được 76 gam hỗn hợp 2 oxit (CaO và MgO) và 3,36 lít khí CO2 ( ở đktc). Tính khối lượng hỗn hợp muối ban đầu?
\(m_{CO_2}=\dfrac{3,36}{22,4}.44=6,6(g)\)
Áp dụng định luật BTKL: \(m_{\text{hh muối}}=m_{\text{hh oxit}}+m_{CO_2}=76+6,6=82,6(g)\)
Đúng 3
Bình luận (0)
Bài 2: Hòa tan 16 g hỗn hợp CuO và MgO vào dung dịch HCl dư. Sau phản ứng thu được 32,5 g muối.
a. Tính thành phần % theo khối lượng mỗi chất trong hỗn hợp ban đầu.
b. Tính khối lượng mỗi muối thu được sau phản ứng.
Gọi \(\left\{{}\begin{matrix}n_{CuO}=x\\n_{MgO}=y\end{matrix}\right.\)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
x x ( mol )
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
y y ( mol )
Ta có:
\(\left\{{}\begin{matrix}80x+40y=16\\135x+95y=32,5\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow m_{CuO}=0,1.80=8g\)
\(\Rightarrow m_{MgO}=0,2.40=8g\)
\(\%m_{CuO}=\dfrac{8}{16}.100=50\%\)
\(\%m_{MgO}=\dfrac{8}{16}.100=50\%\)
\(m_{CuCl_2}=0,1.135=13,5g\)
\(m_{MgCl_2}=0,2.95=19g\)
Đúng 3
Bình luận (0)
Cho 4gam hỗn hợp Mg và MgO tác dụng hoàn toàn với lượng dư dung dịch axit sunfuric loãng. Thể tích khí thu được là 2,24l khí (đtkc). Tính thành phần % theo khối lượng của Mg và MgO trong hỗn hợp ban đầu.
Số mol của khí hidro
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Pt : Mg + 2HCl → MgCl2 + H2\(|\)
1 2 1 1
0,1 0,1
MgO + 2HCl → MgCl2 + H2O\(|\)
1 2 1 1
Số mol của magie
nMg= \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
Khối lượng của magie
mMg= nMg . MMg
= 0,1 . 24
= 2,4 (g)
Khối lượng của magie oxit
mMgO = 4 - 2,4
= 1,6 (g)
0/0Mg = \(\dfrac{m_{Mg}.100}{m_{hh}}=\dfrac{2,4.100}{4}=60\)0/0
0/0MgO = \(\dfrac{m_{MgO}.100}{m_{hh}}=\dfrac{1,6.100}{4}=40\)0/0
Chúc bạn học tốt
Đúng 2
Bình luận (0)
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(PTHH:MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
\(PTHH:Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
Mol: 0,1 0,1
mMg=0,1.24=2,4
=> mMgO=4-2,4=1,6
\(\%m_{Mg}=\dfrac{2,4.100}{4}=60\%;\%m_{MgO}=100-60=40\%\)
Đúng 0
Bình luận (2)
Nung nóng một hỗn hợp gồm CaCO3 và MgO tới khối lượng không đổi, thì số gam chất rắn còn lại chỉ bằng 2/3 số gam hỗn hợp trước khi nung. Vậy trong hỗn hợp ban đầu thì CaCO3 chiếm phần trăm theo khối lượng là A. 75,76%. B. 66,67%. C. 33,33%. D. 24,24%.
Đọc tiếp
Nung nóng một hỗn hợp gồm CaCO3 và MgO tới khối lượng không đổi, thì số gam chất rắn còn lại chỉ bằng 2/3 số gam hỗn hợp trước khi nung. Vậy trong hỗn hợp ban đầu thì CaCO3 chiếm phần trăm theo khối lượng là
A. 75,76%.
B. 66,67%.
C. 33,33%.
D. 24,24%.
Đáp án A
+ S ơ đ ồ p h ả n ứ n g : C a C O 3 M g O → t 0 ⏟ 30 g a m C a O M g O ⏟ 20 g a m + C O 2 ↑ ⇒ n C a C O 3 = n C O 2 = 30 - 20 44 ⇒ % m C a C O 3 = 10 . 100 44 . 30 = 75 , 76 %
Đúng 0
Bình luận (0)