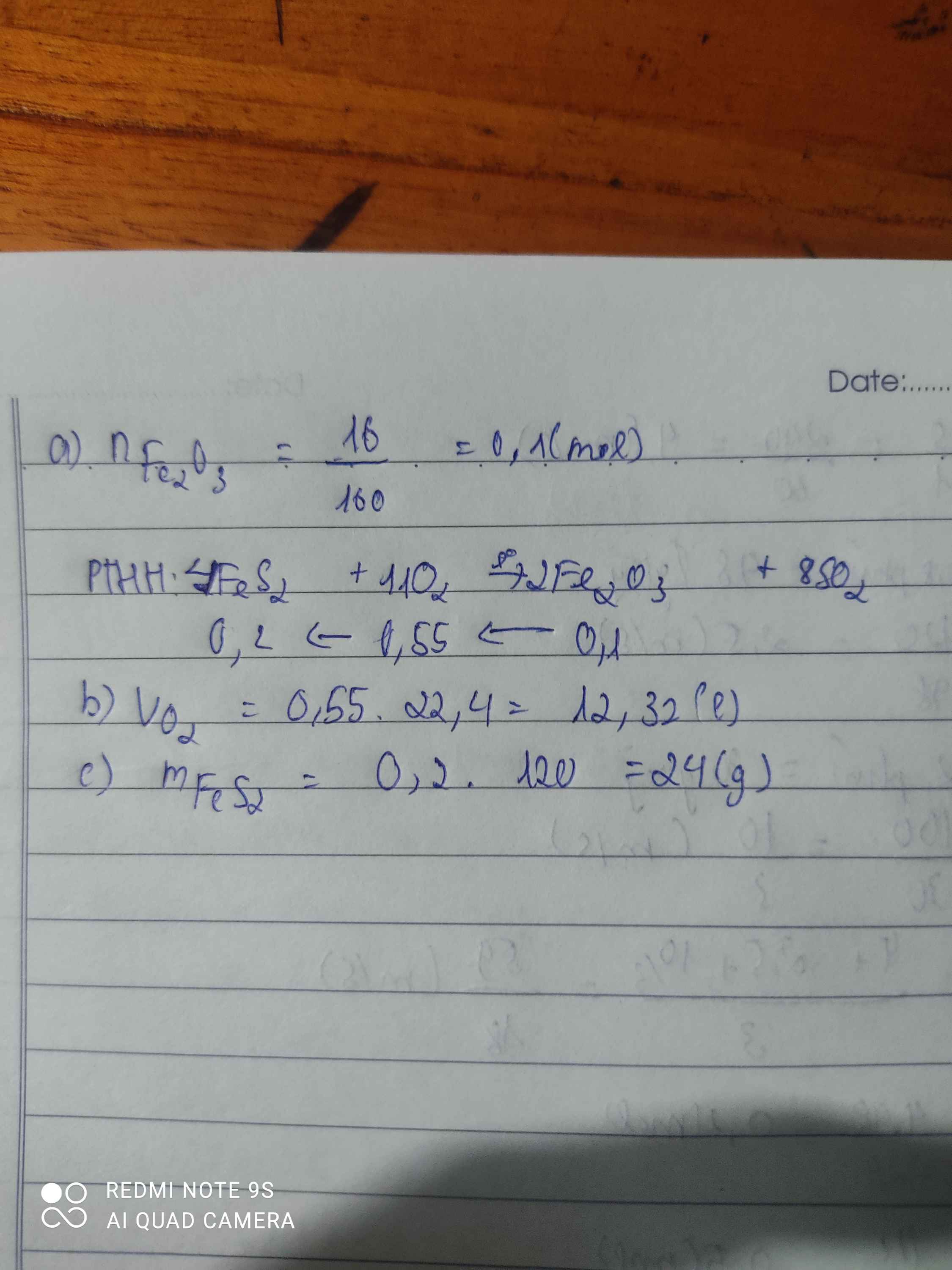Al\(_2\)O\(_3\) tác dụng với quỳ tím thành màu gì?

Những câu hỏi liên quan
Câu 33: Khi cho quỳ tím vào dung dịch axit, quỳ tím chuyển màu gì:A. Đỏ B. XanhC. Tím D. Không màuCâu 34: Kim loai tác dụng với nước ở nhiệt độ thường là:A. Fe, Mg, Al B. Fe, Cu, AgC. Zn, Al, Ag D. Li, Na, KCâu 35: Điện phân hoàn toàn 2 lít nước ở trạng thái lỏng (biết khối lượng riêng của nước là 1kg/l). Thể tích khí hidro và thể tích khí oxi thu được ở đktc là:A. 1244,4 lít và 622,2 lít B. 3733,2 lít và 1866,6 lítC. 4977,6 lít và...
Đọc tiếp
Câu 33: Khi cho quỳ tím vào dung dịch axit, quỳ tím chuyển màu gì:
A. Đỏ B. Xanh
C. Tím D. Không màu
Câu 34: Kim loai tác dụng với nước ở nhiệt độ thường là:
A. Fe, Mg, Al B. Fe, Cu, Ag
C. Zn, Al, Ag D. Li, Na, K
Câu 35: Điện phân hoàn toàn 2 lít nước ở trạng thái lỏng (biết khối lượng riêng của nước là 1kg/l). Thể tích khí hidro và thể tích khí oxi thu được ở đktc là:
A. 1244,4 lít và 622,2 lít B. 3733,2 lít và 1866,6 lít
C. 4977,6 lít và 2488,8 lít D. 2488,8 lít và 1244,4 lít
Câu 36: Cho mẩu Na vào nước thấy có 4,48 lít khí bay lên. Tính khối lượng Na
A.9,2 g B. 4,6g C. 2g D. 9,6g
Câu 37: Đốt hoàn toàn 2 mol khí H2 thì thể tích O2 cần dùng ở đktc là bao nhiêu lít?
A. 22,4 lít B. 11,2 lít C. 44,8 lít D. 8,96 lít
Câu 33: Khi cho quỳ tím vào dung dịch axit, quỳ tím chuyển màu gì:
A. Đỏ B. Xanh
C. Tím D. Không màu
Câu 34: Kim loai tác dụng với nước ở nhiệt độ thường là:
A. Fe, Mg, Al B. Fe, Cu, Ag
C. Zn, Al, Ag D. Li, Na, K
Câu 35: Điện phân hoàn toàn 2 lít nước ở trạng thái lỏng (biết khối lượng riêng của nước là 1kg/l). Thể tích khí hidro và thể tích khí oxi thu được ở đktc là:
A. 1244,4 lít và 622,2 lít B. 3733,2 lít và 1866,6 lít
C. 4977,6 lít và 2488,8 lít D. 2488,8 lít và 1244,4 lít
Giải thích:
\(2H_2O\underrightarrow{đp}2H_2+O_2\)
\(\dfrac{1}{9}\) --->\(\dfrac{1}{9}\)------>\(\dfrac{1}{18}\)
\(n_{H_2O}=\dfrac{2000}{18}=\dfrac{1000}{9}\left(mol\right)\)
\(V_{H_2}=\dfrac{1000}{9}.22,4=2488,89\left(l\right)\\ V_{O_2}=\dfrac{1000}{18}.22,4=1244,44\left(l\right)\)
Câu 36: Cho mẩu Na vào nước thấy có 4,48 lít khí bay lên. Tính khối lượng Na
A.9,2 g B. 4,6g C. 2g D. 9,6g
Giải thích:
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
0,4<---------------------------0,2
\(n_{Na}=0,4.23=9,2\left(g\right)\)
Câu 37: Đốt hoàn toàn 2 mol khí H2 thì thể tích O2 cần dùng ở đktc là bao nhiêu lít?
A. 22,4 lít B. 11,2 lít C. 44,8 lít D. 8,96 lít
Giải thích:
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
2----->1
\(V_{O_2}=1.22,4=22,4\left(l\right)\)
Đúng 3
Bình luận (0)
Câu 33: A
Câu 34: D
Câu 35:
\(m_{H_2O}=2\left(kg\right)=2000\left(g\right)\Rightarrow n_{H_2O}=\dfrac{2000}{18}=\dfrac{1000}{9}\left(mol\right)\)
PT: \(2H_2O\underrightarrow{đp}2H_2+O_2\)
Theo PT: \(\left\{{}\begin{matrix}n_{H_2}=n_{H_2O}=\dfrac{1000}{9}\left(mol\right)\\n_{O_2}=\dfrac{1}{2}n_{H_2O}=\dfrac{500}{9}\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=\dfrac{1000}{9}.22,4\approx2488,8\left(l\right)\\V_{O_2}=\dfrac{500}{9}.22,4\approx1244,4\left(l\right)\end{matrix}\right.\)
→ Đáp án: D
Câu 36: A (giống câu 30)
Câu 37:
PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{H_2}=1\left(mol\right)\Rightarrow V_{O_2}=1.22,4=22,4\left(l\right)\)
→ Đáp án: A
Đúng 2
Bình luận (0)
Cho 100ml dd HCl 1M tác dụng với 200ml dd nạo 1,5M thu được dd X. Dd X làm giấy quỳ tím đổi thành màu gì? Giải thích? Viết phương trình hóa học
\(n_{HCl}=1.0,1=0,1(mol);n_{NaOH}=1,5.0,2=0,3(mol)\\ PTHH:NaOH+HCl\to NaCl+H_2O\)
Vì \(\dfrac{n_{HCl}}{1}<\dfrac{n_{NaOH}}{1}\) nên \(NaOH\) dư
Vậy dd X gồm \(NaOH\) và \(NaCl\) sẽ làm quỳ tím hóa xanh
Đúng 1
Bình luận (0)
Cho FeS_2 tác dụng với O_2 thì thu được Fe_2O_3 và SO_2 sau p.ưa, Viết PTHH của p.ư trên?b, Tìm thể tích oxi ở (đktc) cần sử dụng biết sau p.ư thu được 16g Fe_2O_3?c, Xác định khối lượng FeS_2 đã sử dụng
Đọc tiếp
Cho FeS\(_2\) tác dụng với O\(_2\) thì thu được Fe\(_2\)O\(_3\) và SO\(_2\) sau p.ư
a, Viết PTHH của p.ư trên?
b, Tìm thể tích oxi ở (đktc) cần sử dụng biết sau p.ư thu được 16g Fe\(_2\)O\(_3\)?
c, Xác định khối lượng FeS\(_2\) đã sử dụng
4FeS+7O2-to>2Fe2O3+4SO2
0,2----0,35------0,1 mol
n Fe2O3=\(\dfrac{16}{160}\)=0,1 mol
=>VO2=0,35.22,4=7,84l
=>m FeS2=0,2.120=24g
Đúng 1
Bình luận (1)
Tiến hành thí nghiệm với các chất X, Y, Z, T. Kết quả được ghi ở bảng sau:
Mẫu thử
Thí nghiệm
Hiện tượng
X
Tác dụng với
Hợp chất màu tím
Y
Quỳ tím ẩm
Quỳ chuyển thành màu xanh
Z
Tác dụng với dung dịch nước brom
Dung dịch mất màu và có kết tủa trắng
T
Tác dụng với dung dịch brom
Dung dịch mất màu
Các chất X, Y, Z, T lần lượt là: A. Acrilonitrin, anilin, Gly...
Đọc tiếp
Tiến hành thí nghiệm với các chất X, Y, Z, T. Kết quả được ghi ở bảng sau:
| Mẫu thử |
Thí nghiệm |
Hiện tượng |
| X |
Tác dụng với |
Hợp chất màu tím |
| Y |
Quỳ tím ẩm |
Quỳ chuyển thành màu xanh |
| Z |
Tác dụng với dung dịch nước brom |
Dung dịch mất màu và có kết tủa trắng |
| T |
Tác dụng với dung dịch brom |
Dung dịch mất màu |
Các chất X, Y, Z, T lần lượt là:
A. Acrilonitrin, anilin, Gly-Ala-Ala, metylamin.
B. Gly-Ala-Ala, metylamin, anilin, acrilonitrin
C. Gly-Ala-Ala, metylamin, acrilonitrin, anilin.
D. Metylamin, anilin, Gly-Ala-Ala, acrilonitrin.
Tiến hành thí nghiệm với các chất X, Y, Z, T. Kết quả được ghi ở bảng sau:
Mẫu thử
Thí nghiệm
Hiện tượng
X
Tác dụng với
Hợp chất màu tím
Y
Quỳ tím ẩm
Quỳ chuyển thành màu xanh
Z
Tác dụng với dung dịch nước brom
Dung dịch mất màu và có kết tủa trắng
T
Tác dụng với dung dịch brom
Dung dịch mất màu
Các chất X...
Đọc tiếp
Tiến hành thí nghiệm với các chất X, Y, Z, T. Kết quả được ghi ở bảng sau:
| Mẫu thử |
Thí nghiệm |
Hiện tượng |
| X |
Tác dụng với |
Hợp chất màu tím |
| Y |
Quỳ tím ẩm |
Quỳ chuyển thành màu xanh |
| Z |
Tác dụng với dung dịch nước brom |
Dung dịch mất màu và có kết tủa trắng |
| T |
Tác dụng với dung dịch brom |
Dung dịch mất màu |
Các chất X, Y, Z, T lần lượt là
A. Acrilonitrin, anilin, Gly-Ala-Ala, metylamin.
B. Gly-Ala-Ala, metylamin, anilin, acrilonitrin
C. Gly-Ala-Ala, metylamin, acrilonitrin, anilin.
D. Metylamin, anilin, Gly-Ala-Ala, acrilonitrin
Đáp án B
![]() hợp chất màu tím => loại A và D.
hợp chất màu tím => loại A và D.
![]() trắng.
trắng.
Đúng 0
Bình luận (0)
Tiến hành thí nghiệm với các chất X, Y, Z, T. Kết quả được ghi ở bảng sau:
Mẫu thử
Thí nghiệm
Hiện tượng
X
Tác dụng với
C
u
O
H
2
Hợp chất màu tím
Y
Quỳ tím ẩm
Quỳ chuyển thành màu xanh
Z
Tác dụng với dung d...
Đọc tiếp
Tiến hành thí nghiệm với các chất X, Y, Z, T. Kết quả được ghi ở bảng sau:
| Mẫu thử |
Thí nghiệm |
Hiện tượng |
| X |
Tác dụng với C u O H 2 |
Hợp chất màu tím |
| Y |
Quỳ tím ẩm |
Quỳ chuyển thành màu xanh |
| Z |
Tác dụng với dung dịch nước brom |
Dung dịch mất màu và có kết tủa trắng |
| T |
Tác dụng với dung dịch brom |
Dung dịch mất màu |
Các chất X, Y, Z, T lần lượt là:
A. Acrilonitrin, anilin, Gly-Ala-Ala, metylamin
B. Gly-Ala-Ala, metylamin, anilin, acrilonitrin
C. Gly-Ala-Ala, metylamin, acrilonitrin, anilin
D. Metylamin, anilin, Gly-Ala-Ala, acrilonitrin
Viết PTHH hoàn thành sơ đò chuỗi phản ứng sauAl(OH)_{ }_3 underrightarrow{left(1right)} Al_2O_3underrightarrow{left(2right)} Al_2(SO_4)_3underrightarrow{left(3right)} BaSO_4
Đọc tiếp
Viết PTHH hoàn thành sơ đò chuỗi phản ứng sau
Al(OH)\(_{ }\)\(_3\) \(\underrightarrow{\left(1\right)}\) Al\(_2\)O\(_3\)\(\underrightarrow{\left(2\right)}\) Al\(_2\)(SO\(_4\))\(_3\)\(\underrightarrow{\left(3\right)}\) BaSO\(_4\)
\(1\\ 2Al\left(OH\right)_3\rightarrow\left(t^o\right)Al_2O_3+3H_2O\\ 2\\ Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\\ Al_2\left(SO_4\right)_3+3BaCl_2\rightarrow3BaSO_4+2AlCl_3\)
Đúng 1
Bình luận (1)
cho 200(g) BaCl2 10,4(%) tác dụng vừa đủ với dung dịch H2SO4 (41,9%). a) viết phương trình phản ứng xảy ra. b) nếu cho quỳ tím cho vào dung dịch sau phản ứng quỳ tím có màu gì? c) tính khối lượng chất kết tủa tạo thành. d) tính khối lượng dung dịch H2SO4 4,9(%) đã dùng. e) tính nồng độ phần trăm dung dịch sau phản ứng
\(n_{BaCl_2}=\dfrac{200.10,4\%}{208}=0,1\left(mol\right)\\ a,BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\\ b,Qu\text{ỳ}-t\text{í}m-ho\text{á}-\text{đ}\text{ỏ}-do-c\text{ó}-\text{ax}it-HCl\\ c,n_{BaSO_4}=n_{H_2SO_4}=n_{BaCl_2}=0,1\left(mol\right)\\ m_{k\text{ết}-t\text{ủa}}=m_{BaSO_4}=233.0,1=23,3\left(g\right)\\ d,m_{\text{dd}H_2SO_4}=\dfrac{0,1.98}{4,9\%}=200\left(g\right)\\ e,m_{\text{dd}HCl}=200+200-23,3=376,7\left(g\right)\\ n_{HCl}=0,1.2=0,2\left(mol\right)\\ C\%_{\text{dd}HCl}=\dfrac{0,2.36,5}{376,7}.100\approx1,938\%\)
Đúng 1
Bình luận (0)
Bài 7. Cho 300 ml dung dịch NaOH 1M tác dụng với 100 ml dung dịch H2SO4 1M thu được dung dịch X. Cho quỳ tím vào dung dịch X, quỳ tím sẽ đổi màu gì?
\(n_{NaOH}=0,3\cdot1=0,3mol\)
\(n_{H_2SO_4}=0,1\cdot1=0,1mol\)
Ta nhận thấy \(n_{NaOH}>n_{H_2SO_4}\left(0,3>0,1\right)\)
Khi nhúng quỳ tím thì chắc chắn quỳ hóa xanh do tính bazo thể hiện nhiều hơn tính axit (vì số mol bazo nhiều hơn).
Đúng 2
Bình luận (0)