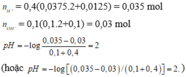cho 100ml dd h2so4 aM tác dụng voi 150ml dd chứa naoh 0,1M và ba(oh) 0 025M thu được pg kết tủa dd X( pH = 2). giá trị a và p theo thứ tự lần lượt là?

Những câu hỏi liên quan
cho 100ml dd h2so4 aM tác dụng voi 150ml dd chứa naoh 0,1M và ba(oh) 0 025M thu được pg kết tủa và 250ml dd X( pH = 2). giá trị a và p theo thứ tự lần lượt là?
Ta có sơ đồ đường chéo:
\(\left\{{}\begin{matrix}\left[H^+\right]=2aM\\\left[OH^-\right]=0,15M\end{matrix}\right.\)\(\left[H^+\right]=0,01M\)\(\dfrac{0,15+0,01}{2a-0,01}\)=\(\dfrac{V_1}{V_2}\)=\(\dfrac{0,1}{0,15}\)
=> a = 0,125
=> p=nBaSO4= 0,00375.233=0,87375
Đúng 0
Bình luận (0)
Cho 100ml dd A gồm NaOH xM & Ba(OH)2 1,5M vào 100ml dd B gồm H2SO4 1M & AlCl; y M thu được 31,1 gam kết tủa. Cho 150 ml dd A tác dụng với 200 ml dd B thu được 63,5 gam kết tủa . Tính x, y ?
Xem chi tiết
Trộn 100 ml dd (gồm Ba(OH)2 0,1M và NaOH 0,1M) với 400 ml dd (gồm H2SO4 0,0375M và HCl 0,0125M), thu được dd X. Giá trị pH của dd X là
A.7.
B. 2.
C. 1.
D. 6.
Trộn 300 ml dd hh gồm H2SO4 0,1M và HCl 0, 15M với V ml dd hh gồm NaOH 0,3M và Ba(OH)2 0,1M, thu được dd X có pH = 12. Giá trị của V là:
\(n_{H^+}=0.3\cdot0.1\cdot2+0.3\cdot0.15=0.105\left(mol\right)\)
\(n_{OH^-}=0.001V\cdot0.3+0.001V\cdot2\cdot0.1=0.0032V\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(0.105.......0.105\)
\(n_{OH^-\left(dư\right)}=0.0032V-0.105\left(mol\right)\)
\(\left[OH^-\right]=\dfrac{0.0032V-0.105}{0.3+0.001V}\left(M\right)\)
\(pH=14+log\left[OH^-\right]=12\)
\(\Leftrightarrow log\left[OH^-\right]=-2\)
\(\Leftrightarrow log\left[\dfrac{0.0032V-0.105}{0.3+0.001V}\right]=-2\)
\(\Leftrightarrow V=33.85\left(ml\right)\)
Đúng 0
Bình luận (0)
nH+=0,3.0,1.2+0,3.0,15=0,105 mol
nOH- ban đầu =0,3V + 0,1.2V=0,5V mol
Sau phản ứng thu được dung dịch có pH=12
⇒OH- dư ⇒ pOH=2
⇒ [OH- ] dư = 0,01 M
nOH- dư = 0,01(0,3+V)=0,003+0,01V (mol)
nOH- phản ứng=nOH- ban đầu - nOH- dư
= 0,5V - 0,003 - 0,01V
= 0,49V - 0,003 (mol )
H+ + OH- → H2O
0,105 → 0,105
nOH- phản ứng = nH+
⇒0,49V - 0,003 =0,105
⇒ V≃0,22 lít=200ml
Đúng 0
Bình luận (0)
Giúp mình với ạ :<
Cho 200 ml dd A gồm HCl 0.3M và H2SO4 xM vào 100ml dd B gồm NaOh 0.2M và Ba(OH)2 yM, phản ứng hoàn toàn, thu được 34,95g kết tủa và dd C. Nếu cho thêm dd Na2SO4 dư vào dd C, thu được thêm 27,96g kết tủa. pH của dd C là?
Trộn 100ml dd X chứa Cuso4 0,1M và Mgcl2 0,3M tác dụng với 400 dd Y gồm Ba(oh)2 0,05M và Koh 0,2M .Tính kết tủa thu được sau phản ứng?
Cho 2.7 gam al phản ứng với 450ml dd HCl 1M tạo dd A . Cho A tác dụng vs 500 ml dd NaOH 1M thu được kết tủa . khối lượng kết tủa là?
đang cần gấp ai lm đc gúp em trong chiều nay đc ko ạ cảm ơn nhìu nhìu
Đúng 0
Bình luận (0)
Giải giúp mk theo phương pháp điện li nha.
Đề bài: Cho 2 dd H2SO4 aM và NaOH bM. Tính a, b biết :
- Trung hoà 180ml dd NaOH bM cần dùng 75ml dd H2SO4 aM.
- Cho 400ml dd H2SO4 aM tác dụng với Ba(OH)2 tạo 3, 94g kết tủa. Trung hoà dd thu đc cần dùng 50ml dd NaOH bM.
tính pH và giá trị a: trộn 100ml dd Ba(OH)2 0,01M với 100ml dd H2SO2 0,05M. Sau phản ứng thu được dd A và a gam kết tủa
Sửa đề H2SO2 thành H2SO4
\(n_{Ba^{2+}}=n_{Ba\left(OH\right)2}=0,01.0,1=0,001\left(mol\right)\)
\(\Rightarrow n_{OH^-}=2n_{Ba\left(OH\right)2}=2.0,001=0,002\left(mol\right)\)
\(n_{SO_4^{2-}}=n_{H2SO4}=0,1.0,05=0,005\left(mol\right)\)
\(\Rightarrow n_{H^+}=2n_{H2SO4}=2.0,005=0,01\left(mol\right)\)
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\)
0,001 0,01 0,01
Xét tỉ lệ : \(0,001< 0,01\Rightarrow SO_4^{2-}dư\)
\(n_{Ba^{2+}\left(pư\right)}=n_{BaSO4}=0,001\left(mol\right)\Rightarrow m_{BaSO4}=0,001.233=0,233\left(g\right)\)
\(H^++OH^-\rightarrow H_2O\)
0,01 0,002
Xét tỉ lệ : \(0,01>0,002\Rightarrow H^+dư\)
\(n_{H^+dư}=0,01-0,002=0,008\left(mol\right)\Rightarrow\left[H^+\right]=\dfrac{0,008}{0,1+0,1}=0,04M\)
\(\Rightarrow pH=-log\left(0,04\right)\approx1,4\)
Đúng 2
Bình luận (0)
Trộn 100ml dd ba(oh)2 0.3M với 100ml dd h2so4 0.05M thu được dd X và kết tủa Y a/ tính ph của dd Y b/ tính kl kết tủa Y c/ tính nồng độ các ion còn lại trong dd X