7. Cho 18,4 g rượu etylic tác dụng với Na
a) viết pt
b) tính Vrượu đã dùng biết D=0,8 g/ml
c) tính Vh2 ( đkc)
Cần gấp
Cho 2,9g rượu etylic tác dụng hết với Na a. Tính thể tích khí H2 thu được ở đktc ? b. Tính thể tích rượu etylic đã dùng? Biết Dr= 0,8 g/ml
\(nC_2H_5OH=\dfrac{2,9}{46}=0,06\left(mol\right)\)
\(C_2H_5OH+Na\rightarrow C_2H_5ONa+\dfrac{1}{2}H_2\)
0,06 0,06 0,06 0,03 (mol)
VH2 = 0,03.22,4= 0,672 (l)
V = m /D
=> V rượu etylic = 2,9 / 0,8 = 3,625 (ml)
Đốt cháy 37,75 ml rượu etylic cho sản phẩm qua nước vôi trong dư được 100g kết tủa
a) Xác định độ rượu trên biết Drượu, D H2O
b) Cho dung dịch trên tác dụng với Na lấy dư thì thu được bao nhiêu lít H2 ở đkc
c) Nếu dùng m g rượu 45° tác dụng với Na thì cần bao nhiêu g rượu để thu được thể tích h2 ở trên
Hòa tan m gam rượu etylic ( D = 0,8 g/ml) vào 108 ml nước ( D= 1 g/ml) tạo thành dung dịch A. Cho dung dịch A tác dụng với kim loại Na dư, thu được 85,12 lít khí H2 (đktc). Tính giá trị m và nồng độ mol của rượu etylic
nH2 = 85,12 : 22,4 = 3,8 (mol) ; nH2O = VH2O.D = 108 (g) => nH2O = 108/18 = 6 (mol)
PTHH:
2Na + 2C2H5OH → 2C2H5ONa + H2↑
x → 0,5x (mol)
2Na + 2H2O → 2NaOH + H2↑
6 → 3 (mol)
Ta có: nH2 = 0,5x + 3 = 3,8
=> x = 1,6 (mol) = nC2H5OH
mC2H5OH = 1,6.46 = 73,6 (g)
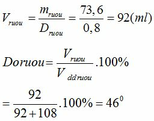
Cho 20 ml rượu etylic 96o tác dụng với Na dư.
a) Tìm thể tích và khối lượng rượu nguyên chất, biết Dr = 0,8 g/ml
b) Tính thể tích H2 thu được ở đktc biết DH2O = 1 g/ml
a)
\(V_{C_2H_5OH}=\dfrac{96.20}{100}=19,2\left(ml\right)\)
=> \(m_{C_2H_5OH}=19,2.0,8=15,36\left(g\right)\)
b) \(n_{C_2H_5OH}=\dfrac{15,36}{46}=\dfrac{192}{575}\left(mol\right)\)
\(V_{H_2O}=20-19,2=0,8\left(ml\right)\)
=> \(m_{H_2O}=0,8.1=0,8\left(g\right)\)
=> \(n_{H_2O}=\dfrac{0,8}{18}=\dfrac{2}{45}\left(mol\right)\)
PTHH: 2C2H5OH + 2Na --> 2C2H5ONa + H2
\(\dfrac{192}{575}\)------------------------->\(\dfrac{96}{575}\)
2H2O + 2Na --> 2NaOH + H2
\(\dfrac{2}{45}\)----------------------->\(\dfrac{1}{45}\)
=> \(V_{H_2}=22,4.\left(\dfrac{96}{575}+\dfrac{1}{45}\right)=4,238\left(l\right)\)
C2H5OH + Na -- > C2H5OHNa + 1/2 H2
Na+H2O --- > NaOH + 1/2H2
Vr = 20x96/100 = 19,2ml = 0.0192 (l)
mC2H5OH = D.V = 19,2 x 0.8 = 15.36 (g)
nC2H5OH = m/M = 15.36 / 46 = 0.43 (mol)
=> nH2 = 0.215 (mol)
VH2O = 1 ml => mH2O = 1 (g)
=> nH2O = m/M = 1/18 = 0.056 (mol)
=> nH2 = 0.028 (mol)
nH2 = 0.215 + 0.028 = 0.243 (mol)
=> VH2 = 22.4 x 0,243 = 5,4432 (l)
Bài 10: Cho 200ml rượu etylic X tác dụng hết với Na thấy bay ra 51,28 l H22 ĐKTC.
a, Tính độ rượu của rượu X.
b, Tính mNa. { coi Vdd= Vrượu + Vnc}. Biết d rượu = 0,8g/ml.
Bài 11: DD A là hh rượu etylic và nc. Cho 20,2g A tác dụng vs Na dư thu đc 5,6 l H2 đktc.
a, Tính độ rượu của rượu A
b, Nếu dung rượu 40ocho td với Na thì cần bao nhiêu g rượu để thu đc lượng H2 trên. { coi Vdd= Vrượu + Vnc}. Biết d rượu = 0,8g/ml.
Mong các bạn giúp mik sớm một chút... Thanks~~~
Cho 16ml rượu etylic 71,875° phản ứng với Kali. Tính VH2 (đkc). Biết D rượu=0,8g/ml, DH2O=1g/ml.
\(V_{C_2H_5OH\left(\text{nguyên chất}\right)}=16.71,875\%=11,5\left(ml\right)\\ \rightarrow m_{C_2H_5OH\left(\text{nguyên chất}\right)}=11,5.0,8=9,2\left(g\right)\\ \rightarrow n_{C_2H_5OH\left(\text{nguyên chất}\right)}=\dfrac{9,2}{46}=0,2\left(mol\right)\)
PTHH: 2C2H5OH + 2K ---> 2C2H5OK + H2
0,2 0,1
=> VH2 = 0,1.22,4 = 2,24 (l)
Để xác định độ rượu của một loại ancol etylic (kí hiệu là X) người ta lấy 10 ml X cho tác dụng hết với Na dư thu được 2,564 lít H2 (đktc). Tính độ rượu của X biết khối lượng riêng của ancol etylic nguyên chất là 0,8 g/ml. 92,50
A. 87,5o.
B. 85,7o.
C. 91,0o.
D. 92,5o.
Cho 10,1 gam dung dịch rượu etylic tác dụng với kim loại Na dư thu được 2,8 lít H 2 (đktc). Biết khối lượng riêng của rượu etylic là 0,8 g/ml và của nước là 1 g/ml. Xác định độ rượu đem tham gia phản ứng?
A. 92 , 74 o
B. 96 o
C. 73 , 92 0
D. 97 , 24 o
Đáp án: A
Vì dung dịch rượu gồm rượu etylic và nước nên ta gọi:
n H 2 O = x m o l và n C 2 H 5 O H = y m o l
PTHH:
2 N a + 2 H 2 O → 2 N a O H + H 2 ↑ ( 1 )
x mol → 0,5.x mol
2 N a + 2 C 2 H 5 O H → 2 C 2 H 5 O N a + H 2 ↑
y mol → 0,5.y mol
Ta có hệ phương trình:
18 x + 46 y = 10 , 1 0 , 5 x + 0 , 5 y = 0 , 125 ⇒ x = 0 , 05 y = 0 , 2
V C 2 H 5 O H nguyên chất = m D = 0 , 2 . 46 0 , 8 = 11 , 5 m l
V H 2 O = m D = 10 , 1 - 9 , 2 1 = 0 , 9 m l
=> V d d r ư ợ u = V H 2 O + V C 2 H 5 O H = 0,9 + 11,5 = 12,4 ml
=> Độ rượu D 0 = V C 2 H 5 O H V d d r u o u . 100 = 11 , 5 12 , 4 . 100 = 92 , 74 0
Dung dịch A là hỗn hợp rượu etylic và nước. Cho 20,2 g A tác dụng với Na (dư) thấy thoát ra 5,6 lít khí H2 ( đktc). Xác định độ rượu, biết khối lượng riêng của rượu etylic là 0,8 gam/ml, của nước là 1g/ml.
Gọi \(\left\{{}\begin{matrix}n_{C_2H_5OH}=a\left(mol\right)\\n_{H_2O}=b\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH:
2C2H5OH + 2Na ---> 2C2H5ONa + H2
a --------------------------------------------> 0,5a
2H2O + 2Na ---> 2NaOH + H2
b --------------------------------> 0,5b
Hệ pt \(\left\{{}\begin{matrix}46a+18b=20,2\\0,5a+0,5b=0,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,4\left(mol\right)\\b=0,1\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{C_2H_5OH}=0,4.46=18,4\left(g\right)\\m_{H_2O}=0,1.18=1,8\left(g\right)\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}V_{C_2H_5OH}=\dfrac{18,4}{0,8}=23\left(ml\right)\\V_{H_2O}=\dfrac{1,8}{1}=1,8\left(ml\right)\end{matrix}\right.\)
=> Độ rượu là: \(\dfrac{23}{23+1,8}=92,74^o\)