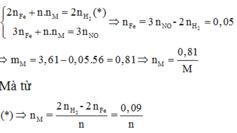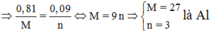Cho m g hh gồm 2 kim loại A và B có hóa trị khong đổi thành 2 phần bằng nhau:
P1: Hòa tan hết trong dd HCl tạo ra 1,792 lít H2 (đktc)
P2: Nung trong oxi dư thu được 2,84g hh 2 oxit
Xác định giá trị của m
Chia hh X gồm Al và kim loại M (hóa trị không đổi) thành 3 phần bằng nhau:
P1: cho vào dd NaOH dư sau khi pứ xảy ra hoàn toàn thấy thoát ra 1,4874 lít khí H2(đktc) và còn lại một phần chất rắn không tan.
P2: đốt cháy trong V1 lít khí Oxi(đktc), thu được dd rắn Y gồm 4 chất. Để hòa tan hoàn toàn Y cần dùng vừa đủ 200ml dd gồm H2SO4 0,3M và HCl 0,4M thu được 0,9916 lít khí H2 (đktc) và dd chỉ chứa 10,64g hh các muối trung hòa.
1) Xác định kim loại M và tính giá trị V1
P3: Cho vào V2 lít dd CuSO4 0,5M khuấy đều sau khi pứ xảy ra hoàn toàn thu được 5,71g chất rắn. Tính giá trị V2
Câu 2: Chia hỗn hợp 2 kim loại A,B có hóa trị không đổi thành 2 phần bằng nhau. Phần 1 tan hết trong dung dịch HCl, tạo ra 1,792 lít H2 (đktc), phần 2 nung trong oxy thu được 2,84 gam hỗn hợp oxit. Khối lượng hỗn hợp hai kim loại trong hỗn hợp đầu là?
Theo gt ta có: $n_{H_2}=0,08(mol)$
Bảo toàn e ta có: $n_{e}=0,16(mol)\Rightarrow n_{O_2}=\frac{n_e}{4}=0,04(mol)$
Do đó $m_{kl}=2,84-0,04.32=1,56(g)$
Suy ra $m_{klbđ}=2.1,56=3,12(g)$
Đặt M là KL chung có hóa trị là n
nH2=0,08
2M + 2nHCl --> 2MCln + nH2
0,16/n <-- 0,16 <-- 0,16/n <--0,08
4M + nO2 --> 2M2On
0,16/n --> 0,08/n
Bảo toàn nguyên tố Oxi: nO trong M2On = (0,08/n).n= 0,08 mol
-> nO2=0,08/2=0,04 mol --> mO2= 0,04.32=1,28g
Bảo toàn khối lượng: mM = mM2On - mO2= 2,84-1,28= 1,56g
hòa tan m (g) hh gồn Fe và kim loại M có hóa trị ko đổi trong dd HCl dư thì thu đc 1,008 lít khí (đktc) và dd chứa 4,575 g muối khan.
a) Tính m
b) hòa tan m g hh ở trên trong dd chứa hh HNO3 đặc và H2SO4 ở nhiệt độ thích hợp thì thu đc 1,8816 lít hh gồm 2 khí(đktc) có tỉ khối hơi so với H2 là 25,25. Xác định M
hòa tan hoàn toàn khối lượng Fe và Cu(tỉ lệ 1:1) bằng axit HNO3 thu được V lít hỗn hợp khí X gồm NO và NO2 và dung dịch Y (chỉ chứa 2 muốivà axit ) tỉ khối của X đối với H2 bằng 19. tính V
các bạn giải theo cách bảo toàn electron nha
a) Ta có: nH2 = 1,008/22.4 = 0,045 \(\rightarrow\) nHCl = 0,045 x 2= 0,09mol
mA = mmuối - mCl = 4,575 - 0,09 x 35,5 = 1,38g
Đặt x, y lần lượt là số mol của Fe, M và n là hóa trị của M trong hợp chất. Từ 2 phương trình ta có:
56x + My = 1,38 (1)
2x + ny = 0,09 (2)
b) Ở câu b này mình cho rằng đó là H2SO4 đặc chứ ko phải loãng vì nếu loãng thì ta ko thu được hh khí có tỉ khối hơi như vậy.
Các phương trình phản ứng:
Fe + 6HNO3 \(\rightarrow\) Fe(NO3)3 +3NO2 + 3H2O
M + 2nHNO3\(\rightarrow\) M(NO3)n + nNO2 + nH20
2Fe + 6H2SO4 \(\rightarrow\) Fe2(SO4)3 + 3SO2 + 6H2O
2M + 2nH2SO4 \(\rightarrow\) M2(SO4)n + nSO2 + 2nH2O
Ta có: dkhí/ H2 =25,25 \(\rightarrow\) Mkhí = 50,5
Số mol 2 khí=1,8816:22,4=0,084mol
lập hệ giải ra: nNO2 = 0,063, nSO2 = 0,021
Ta có các phương trình e như sau:
Fe \(\rightarrow\) Fe3+ + 3e
x---------------3x
M \(\rightarrow\) Mn+ + ne
y--------------ny
N5+ + 1e \(\rightarrow\) N4+
0,063 \(\leftarrow\) 0,063
S6+ + 2e\(\rightarrow\) S4+
0,042 \(\leftarrow\) 0,021
Tổng e nhận = tổng e nhường nên :
3x + ny = 0,063 + 0,042 = 0,105
kết hợp với (2) suy ra được x = 0,015
ny = 0,06 \(\rightarrow\) y = 0,06/n
Thay vào (1) \(\rightarrow\) M = 9n
Biện luận thì tìm được M là Al.
1 .Cho 7,22g hh gồm Fe và kim loại M co shoas trị không đổi .chia hh thành hai phần bằng nhau .
P1 hòa tan hết trg đ HCL thi đc 2,128 l khí H2 ở đktc
P2 hòa tan hết trong đ H2SO4 đặc,nóng thu đc 2,688 lít SO2 ở đktc.
a) xác định kim loại M
b) tính % khối lượng mỗi kim loại
2.cho Br2 dư qua 41,45 gam hh A gồm Nacl ,NaI,NaBr thu đc dd B chứa 36,75 muối ,tiếp tục cho Cl2 dư qua B thu đc 23,4g hh muối C .tính % khới lg muối NaBr trg A .
Chia m gam hỗn hợp 2 kim loại X và Y có hoá trị không đổi thành 2 phần bằng nhau. Phần 1 hoà tan hết trong dung dịch H2SO4 loãng thu được 1,792 lít khí H2 (đktc). Phần 2 nung trong oxi đến khối lượng không đổi thu được 2,84 gam hỗn hợp oxit. Giá trị của m là:
A. 1,56 gam.
B. 2,20 gam.
C. 3,12 gam.
D. 4,40gam.
Chia m gam hỗn hợp 2 kim loại X và Y có hoá trị không đổi thành 2 phần bằng nhau. Phần 1 hoà tan hết trong dung dịch H2SO4 loãng thu được 1,792 lít khí H2 (đktc). Phần 2 nung trong oxi đến khối lượng không đổi thu được 2,84 gam hỗn hợp oxit. Giá trị của m là:
A. 1,56 gam
B. 2,20 gam
C. 3,12 gam
D. 4,40gam
Chia 2m gam hỗn hợp X gồm hai kim loại có hoá trị không đổi thành 2 phần bằng nhau. Cho phần 1 tan hết trong dung dịch HCl (dư) thu được 2,688 lít H2. Nung nóng phần 2 trong oxi (dư) thu được 4,26 gam hỗn hợp oxit. Giá trị của m là
A. 4,68
B. 1,17
C. 3,51
D. 2,34.
Chọn đáp án D
BTE Þ nO = nH2 Þ m = mOxit - mO = 4,26 - 0,12x16 = 2,34
Cho 5,56g hỗn hợp A gồm Fe và kim loại M ( hóa trị không đổi) . Chia A thành 2 phần bằng nhau
Phần 1 : Hòa tan hết trong dd HCl được 1,568 lít khí H2(đktc)
Phần 2 : Tác dụng vừa đủ với 2,016 lít khí Cl2 ( đktc) . Xác định kim loại M? Giúp mình vớii
Gọi: \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_M=y\left(mol\right)\end{matrix}\right.\) (trong 1 phần) ⇒ 56x + MM.y = 5,56:2 (1)
Giả sử M có hóa trị n không đổi.
- Phần 2: \(n_{Cl_2}=\dfrac{2,016}{22,4}=0,09\left(mol\right)\)
PT: \(2Fe+3Cl_2\underrightarrow{t^o}2FeCl_3\)
\(2M+nCl_2\underrightarrow{t^o}2MCl_n\)
Theo PT: \(n_{Cl_2}=\dfrac{3}{2}n_{Fe}+\dfrac{n}{2}n_M=\dfrac{3}{2}x+\dfrac{n}{2}y=0,09\left(2\right)\)
- Phần 1: \(n_{H_2}=\dfrac{1,568}{22,4}=0,07\left(mol\right)\)
+ TH1: M có pư với HCl.
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2M+2nHCl\rightarrow2MCl_n+nH_2\)
Theo PT: \(n_{H_2}=n_{Fe}+\dfrac{n}{2}n_M=x+\dfrac{n}{2}y=0,07\left(3\right)\)
Từ (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}x=0,04\left(mol\right)\\ny=0,06\end{matrix}\right.\)
Thay vào (1), ta được: \(M_M.y=0,54\) \(\Rightarrow\dfrac{M_M.y}{n.y}=\dfrac{0,54}{0,06}\Rightarrow M_M=9n\)
Với n = 3 thì MM = 27 (g/mol) là thỏa mãn.
→ M là Al.
+ TH2: M không pư với HCl.
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(x=n_{Fe}=n_{H_2}=0,07\left(mol\right)\)
Thay vào (1) ta được \(M_M.y=-1,14\) (vô lý vì MM và y đều là số dương)
Vậy: M là Al.
Cho 7,22 gam hỗn hợp X gồm Fe và kim loại M hóa trị không đổi. Chia hỗn hợp thành 2 phần bằng nhau, hòa tan hết phần 1 trong dung dịch HCI dư thu được 2,128 lít H2. Hòa tan hết phần 2 trong HNO3 thu được 1,792 lít NO. Tìm M?
A. Cu
B. Mg
C.Zn
D. Al
Đáp án D
Gọi n là hóa trị của M. Khối lượng hỗn hợp ở mỗi phần là 3,61 gam, và nNO=0,08.
* Quá hình nhường và nhận electron khi hòa tan phần 1 vào dung dịch HCl dư:
Qúa trình nhường electron:
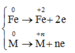
Quá trình nhận electron:
![]()
* Quá trình nhường và nhận electron khi hòa tan phần 2 vào dung dịch HNO3:
Quá trình nhường electron
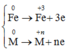
Quá trình nhận electron:
![]()
Áp dụng định luật bảo toàn mol electron, ta có: