Đốt cháy 5,6 g Fe trong không khí thu được ôxít sắt từ.
a) tính khí ôxít và thể tích không khí cần dùng (đktc).
b)tính khối lượng Kali clorat cần thiết để điều chế ra lượng.
4. Khi đốt cháy sắt trong oxi ở nhiệt độ cao thu được oxit sắt từ Fe3O4. a) Tính khối lượng sắt và thể tích khí oxi (đktc) cần dùng để điều chế được 6,96 gam Fe3O4 . b) Tính khối lượng kali clorat KClO3 cần dùng để điều chế được lượng oxi dùng cho phản ứng trên.
a. \(n_{Fe_3O_4}=\dfrac{6,96}{232}=0,03\left(mol\right)\)
PTHH : 3Fe + 2O2 -to-> Fe3O4
0,09 0,06 0,03
\(m_{Fe}=0,09.56=5,04\left(g\right)\)
\(V_{O_2}=0,06.22,4=1,344\left(l\right)\)
b. PTHH : 2KCl + 3O2 -> 2KClO3
0,06 0,04
\(m_{KClO_3}=0,04.122,5=4,9\left(g\right)\)
4
n Fe3O4=\(\dfrac{6,96}{232}=0,03mol\)
3Fe+2O2-to>Fe3O4
0,09---0,06-----0,03 mol
=>m Fe=0,09.56=5,04g
=>VO2=0,06.22,4=1,344l
b)
2KClO3-to>2KCl+3O2
0,04----------------------0,06 mol
=>m KClO3=0,04.122,5=4,9g
\(n_{Fe_3O_4}=\dfrac{6,96}{232}=0,03\left(mol\right)\\ 3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\\ n_{Fe}=3.0,03=0,09\left(mol\right);n_{O_2}=0,03.2=0,06\left(mol\right)\\ a,\Rightarrow m_{Fe}=0,09.56=5,04\left(g\right);V_{O_2\left(đktc\right)}=0,06.22,4=1,344\left(l\right)\\ 2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\uparrow\\ n_{KClO_3}=\dfrac{2}{3}.n_{O_2}=\dfrac{2.0,06}{3}=0,04\left(mol\right)\\ \Rightarrow b,m_{KClO_3}=122,5.0,04=4,9\left(g\right)\)
Câu 3: Đốt cháy hoàn toàn 16,8 gam Sắt (Fe) trong không khí
a) Tính khối lượng sản phẩm thu được?
b) Tính thể tích khí oxi, và thể tích không.khí cần dùng ở đktc? (biết rằng oxi chiếm 20% thể tích không khí)
c) Tính khối lượng KMnO4 cần dùng để điều chế đủ oxi cho phản ứng trên? Biết rằng lượng oxi thu được hao hụt 20%
Cho biết: Fe = 56, O = 16, K = 39, Mn = 55
a.b.
\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,3 0,2 0,1 ( mol )
\(m_{Fe_3O_4}=0,1.232=23,2g\)
\(V_{O_2}=0,2.22,4=4,48l\)
\(V_{kk}=4,48.5=22,4l\)
c.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,4 0,2 ( mol )
\(m_{KMnO_4}=\dfrac{0,4.158}{\left(100-20\right)\%}=79g\)
a/ Số mol Fe là : nFe = 16,8: 56 = 0,3 mol
PTPƯ:
3Fe + 2O2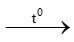 Fe3O4 (1)
Fe3O4 (1)
0,3 mol → 0,2mol → 0,1 mol
Từ (1) ta có số mol Fe3O4 = 0,1mol
→ m Fe3O4 = n.M = 0,1.232 = 23,2gam
b/ Từ (1) ta có số mol O2 đã dùng nO2 = 0,2 mol
Thể tích khí oxi đã dùng ở đktc: VO2 = n.22,4 = 0,2.22,4 = 4,48 lít
Thể tích không khí đã dùng: Vkk = 5. VO2= 5.4,48 = 22,4 lít.
c/ PTPƯ
2 KMnO4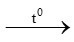 K2MnO4 + MnO2 + O2 (2)
K2MnO4 + MnO2 + O2 (2)
0,4444mol ← 0,222mol
Vì lượng Oxi thu được hao hụt 10% nên số mol O2 cần có là:
nO2 = 0,2mol.100/90 = 0.222 mol
Từ (2) ta có số mol KMnO4 = 0,444mol
Khối lượng KMnO4 bị nhiệt phân
mKMnO4 = n.M = 0,444.158 = 70.152 gam
Đốt cháy hoàn toàn 3,6 g mg trong khí oxi.
a/ Tính thể tích khí oxi ở đktc .
b/ Nếu dùng kali clorat ( chất xúc tác MnO2 ) để điều chế lượng khí oxi thì lượng kali clorat cần dùng là bao nhiêu ?
a)
\(n_{Mg} = \dfrac{3,6}{24} = 0,15(mol)\\ 2Mg + O_2 \xrightarrow{t^o} 2MgO\\ n_{O_2} = \dfrac{1}{2}n_{Mg} = 0,075(mol)\\ \Rightarrow V_{O_2} = 0,075.22,4 = 1,68(lít)\)
b)
\(2KClO_3 \xrightarrow{t^o,MnO_2} 2KCl + 3O_2\\ n_{KClO_3} = \dfrac{2}{3}n_{O_2} = \dfrac{2}{3}.0,075 = 0,05(mol)\\ \Rightarrow m_{KClO_3} = 0,05.122,5 = 6,125(gam)\)
Đốt cháy hoàn toàn 3,6 gam magie trong khí oxi trên thì khối lượng kali clorat cần dùng.
A. Tính thể tích khí oxi (đktc) cần dùng?
B. Nếu dùng dịch KCLO3(có xúc tác MnO2) để điều chế lượng khí oxi trên thì khối lượng kali clorat cần dùng là bao nhiêu?
(O=16,CL=35,5,K=39,Mn=55)
2Mg+O2-to>2MgO
0,15---0,075 mol
2KClO3-to->2KCl+3O2
0,05-----------------------0,075
n Mg=\(\dfrac{3,6}{24}\)=0,15 mol
=>VO2=0,075.22,4=1,68l
=>m KClO3=0,05.122,5=6,125g
a. \(n_{Mg}=\dfrac{3.6}{24}=0,15\left(mol\right)\)
PTHH : 2Mg + O2 ----to----> 2MgO
0,15 0,075
\(V_{O_2}=0,075.22,4=1,68\left(l\right)\)
b. PTHH : 2KClO3 \(\xrightarrow[MnO_2]{t^o}\) 2KCl + 3O2
0,05 0,075
\(m_{KClO_3}=0,05.122,5=6,125\left(g\right)\)
oxy hóa hoàn toàn 8,4g sắt thu được sản phẩm là sắt từ oxit Fe3O4
a) viết PTHH xảy ra ?
b tính thể tích khí oxy cần dùng? (Đktc)
c) tính khối lượng kali clorat KClO3 cần dùng để điều chế ra lượng oxy dùng trong phản ứng trên?
a) PTHH: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
b) Ta có: \(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
\(\Rightarrow n_{O_2}=0,1\left(mol\right)\) \(\Rightarrow V_{O_2}=0,1\cdot22,4=2,24\left(l\right)\)
c) PTHH: \(2KClO_3\xrightarrow[t^o]{MnO_2}2KCl+3O_2\uparrow\)
Theo PTHH: \(n_{KClO_3}=\dfrac{2}{3}n_{O_2}=\dfrac{1}{15}\left(mol\right)\)
\(\Rightarrow m_{KClO_3}=\dfrac{1}{15}\cdot122,5\approx8,17\left(g\right)\)
Đốt cháy hoàn toàn bột sắt (Fe) trong khí oxy (O2) thu được 46,4 gam ôxít sắt từ( Fe3O4) tính khối lượng sắt và oxy cần dùng biết khối lượng sắt gấp 2,625 lần khối lượng oxy đã phản ứng
PTHH:3Fe+2O2----->Fe3O4
a.nAl=43nO2=43.0,4=815(mol)nAl=43nO2=43.0,4=815(mol)
Đốt cháy hoàn toàn 16,8 gam sắt trong không khí
a) Tính khối lượng sản phẩm thu được
b) Tính thể tích khí oxi, và thể tích không khí cần dùng ở điều kiện tiêu chuẩn ( biết oxi chiếm 20% thể tích không khí)
c) Tính khối lượng KMnO4 cần dùng để điều chế đủ oxi cho phản ứng trên? Biết rằng lượng oxi thu được hao hụt 20%
a) nFe = 16,8/56 = 0,3 (mol)
PTHH: 3Fe + 2O2 -> (t°) Fe3O4
Mol: 0,3 ---> 0,2 ---> 0,1
mFe3O4 = 0,1 . 232 = 23,2 (g)
b) VO2 = 0,2 . 22,4 = 4,48 (l)
Vkk = 4,48 . 5 = 22,4 (l)
c) H = 100% - 20% = 80%
nO2 (LT) = 0,2 : 80% = 0,25 (mol)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,25 . 2 = 0,5 (mol)
mKMnO4 = 0,5 . 158 = 79 (g)
đốt cháy hoàn toàn 3,6g magie trong khí oxi
a)tính thể tích khí oxi cần dùng
b)nếu dùng kali clorat (có xúc tác Mno2)để điều chế được khí oxi trên thì khối lượng kali clorat cần dùng là bao nhiêu
Theo gt ta có: $n_{Mg}=0,15(mol)$
a, $2Mg+O_2\rightarrow 2MgO$
Ta có: $n_{O_2}=0,5.n_{Mg}=0,075(mol)\Rightarrow V_{O_2}=1,68(l)$
b, $2KClO_3\rightarrow 2KCl+3O_2$ (đk: nhiệt độ, MnO2)
Ta có: $n_{KClO_3}=\frac{2}{3}.n_{O_2}=0,05(mol)\Rightarrow m_{KClO_3}=6,125(g)$
\(n_{Mg}=\dfrac{3.6}{24}=0.15\left(mol\right)\)
\(2Mg+O_2\underrightarrow{t^0}2MgO\)
\(0.15......0.075......0.15\)
\(V_{O_2}=0.075\cdot22.4=1.68\left(l\right)\)
\(2KClO_3\underrightarrow{t^0}2KCl+3O_2\)
\(0.05.......................0.075\)
\(m_{KClO_3}=0.05\cdot122.5=6.125\left(g\right)\)
Theo gt ta có: nMg=0,15(mol)nMg=0,15(mol)
a, 2Mg+O2→2MgO2Mg+O2→2MgO
Ta có: nO2=0,5.nMg=0,075(mol)⇒VO2=1,68(l)nO2=0,5.nMg=0,075(mol)⇒VO2=1,68(l)
b, 2KClO3→2KCl+3O22KClO3→2KCl+3O2 (đk: nhiệt độ, MnO2)
Ta có: nKClO3=2/3.nO2=0,05(mol)⇒mKClO3=6,125(g)
Đốt cháy hoàn toàn 2,7 g nhôm trong không khí thu được nhôm ôxít ( Al2O3):
a) Viết phương trình phản ứng
b) tính khối lượng nhôm ôxít tạo thành
c) tính thể tích ôxi tham gia phản ứng ở đktc

\(a.4Al+3O_2\rightarrow2Al_2O_3\\ b.n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\\ n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=0,05\left(mol\right)\\ \Rightarrow m_{Al_2O_3}=0,05.102=5,1\left(g\right)\\ c.n_{O_2}=\dfrac{3}{4}n_{Al}=0,075\left(mol\right)\\ \Rightarrow V_{O_2}=0,075.22,4=1,68\left(l\right)\)
\(n_{Al}=\dfrac{2,7}{27}=0,1(mol)\\ a,PTHH:4Al+3O_2\xrightarrow{t^o}2Al_2O_3\\ b,n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=0,05(mol)\\ \Rightarrow m_{Al_2O_3}=0,05.102=5,1(g)\\ c,n_{O_2}=\dfrac{3}{4}n_{Al}=0,075(mol)\\ \Rightarrow V_{O_2}=0,075.22,4=1,68(l)\)
đốt cháy kali trong không khí thu được 28,2 g kali oxit
a) viết phương trình phản ứng
b) tính khối lượng kali tham gia phản ứng
c) tính thể tích khí oxi cần dùng ( đktc)
d) tính thể tích không khí cần dùng
PTHH : 4K + O2 ----> 2K2O (1)
Từ gt => nK2O = 28,9 : 94 = 0,3 (mol)
Từ (1) và gt => nK2O = 0,5 nK = 2 nO2
=> nK = 0,6 mol
nO2 = 0,15
=> mK = 0,6 x 39 = 23,4 (g)
VO2 = 0,15 x 22,4 = 3,36 (l)
Vì O2 chỉ chiếm khoảng 20% thể tích không khí
=> Vkk = VO2 x 5 = 3,36 x 5 = 16,8 (l)