cho 11,8 gam hỗn hợp bột chứa nhôm và dồng vào dd axit clohiđric dư phản ứng hoàn toàn với 6.72 lít h2 (đktc)
thành phần phần trăm cua đồng trong hỗn hợp ban đầu là
A.45.76% B.33,33% C.54,24% D.66,675
Hỗn hợp X gồm Al và Cu. Cho 11,8 gam hỗn hợp X vào dung dịch axit clohidric dư thấy thoát ra 6,72 lít khí ở đktc.
a) Viết PTHH
b) Tính thành phần trăm về khối lượng mỗi kim loại trong hỗn hợp X
c) Nếu cho 11,8 gam hỗn hợp X phản ứng hoàn toàn với dung dịch NaOH dư, tính thể tích khí thoát ra ở đktc
a) \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Cu+HCl\rightarrow\)(không phản ứng)
2Al + 6HCl => 2AlCl3 + 3H2
0,3/3*2 (6,72/22,4)
=> mAl = 0,2 *27 =5,4g; mCu = 11,8 - 5,4 = 6,4g
Cho 1.2 gam hỗn hợp gồm sắt và đồng tác dụng với dung dịch axit Clohiđric dư. Sau phản ứng thu được 1,12 lít khí ( ở đktc ). a. Viết các phương trình hoá học. b. Tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu.
Tiến hành phản ứng nhiệt nhôm hỗn hợp gồm Al và FexOy trong khí trơ đến khi phản ứng xảy ra hoàn toàn thu được hỗn hợp rắn X. Chia hỗn hợp X thành hai phần bằng nhau. Phần 1 cho vào dung dịch NaOH loãng dư, thấy lượng NaOH phản ứng là 8,0 gam, đồng thời thoát ra 1,344 lít khí H2 (đktc). Phần 2 tác dụng hết với dung dịch HCl loãng dư, thu được 5,376 lít khí H2 (đktc). Công thức FexOy là:
A. FeO.
B. Fe3O4.
C. Fe2O3.
D. Fe2O3 hoặc Fe3O4.
Hoà tan hoàn toàn 3 gam hỗn hợp gồm cu và Fe.trong axit clohiđric dư. Người ta thu được 0.56 lít khí H2 (ở đktc) a viết các PTPƯ xảy ra b xác định thành phần các kim loại trong hỗn hợp ban đầu
\(n_{H_2}=0,025\)
a) \(Fe+HCl\rightarrow FeCl_2+H_2\uparrow\)
0,025 ← 0,025
b) \(m_{Fe}=0,025\cdot56=1,4\left(g\right)\)
\(\%m_{Fe}=\dfrac{1,4}{3}\cdot100\%=46,67\%\)
\(\%m_{Cu}=100\%-46,67\%=53,33\%\)
4. Cho dd axit clohiđric HCl phản ứng vừa đủ với 15,6 g hỗn hợp A gồm Mg và MgO. Sau phản ứng thu được 6,72 lít khí H2 (đktc).
a. Viết PTHH.
b. Tính thành phần phần trăm khối lượng các chất có trong hỗn hợp.
\(a.Mg+2HCl\rightarrow MgCl_2+H_2\\ MgO+2HCl\rightarrow MgCl_2+H_2O\\ b.n_{H_2}=n_{Mg}=0,3\left(mol\right)\\ \Rightarrow\%m_{Mg}=\dfrac{0,3.24}{15,6}.100=48,15\%;\%m_{MgO}=53,85\%\)
Hoà tan hoàn toàn 12,9g hỗn hợp gồm Mg và ZnO vào 120g dd H2SO4.Sau phản ứng thu được 4,48 lít khí hiđro (đktc) a. Tính phần trăm khối lượng mỗi chất trong hỗn hợp ban đầu b. Tính nồng độ % dd axit H2SO4 phản ứng
a) Đặt: nMg=x(mol); nZnO=y(mol)
nH2SO4= 0,2(mol)
PTHH: Mg + H2SO4 -> MgSO4 + H2
x___________x____x_______x(mol)
ZnO + H2SO4 -> ZnSO4 + H2O
y____y______y(mol)
Ta có:
\(\left\{{}\begin{matrix}24x+81y=12,9\\22,4x=4,48\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
mMg=0,2.24=4,8(g)
%mMg=(4,8/12,9).100=37,209%
=>%mZnO=62,791%
b) nH2SO4=x+y=0,3(mol)
=> \(C\%ddH2SO4=\dfrac{0,3.98}{120}.100=24,5\%\)
Hòa tan hết 31,12 gam hỗn hợp X gồm Mg, Fe, Fe3O4, FeCO3 vào dd hỗn hợp chứa H2SO4 và KNO3. Sau phản ứng thu được 4,48 lít hỗn hợp khí Y (đktc) gồm (CO2, NO, NO2, H2) có tỉ khối so với H2 là 14,6 và dd Z chỉ chứa các muối trung hòa ( Z không chứa Fe3+ ) với tổng khối lượng là m gam. Cho BaCl2 dư vào Z thấy xuất hiện 140,965 gam kết tủa trắng. Mặt khác cho NaOH dư vào Z thì thấy có 1,085 mol NaOH phản ứng đồng thời xuất hiện 42,9 gam kết tủa và 0,56 lít khí (đktc) thoát ra. Biết các phản ứng xảy ra hoàn toàn. Cho các nhận định sau:
a) Giá trị của m là 82,285 gam.
b) Số mol của KNO3 trong dung dịch ban đầu là 0,225 mol
c) Phần trăm khối lượng FeCO3 trong X là 18,638%.
d) Số mol của Fe3O4 trong X là 0,05 mol.
e) Số mol của Mg trong X là 0,15 mol.
Tổng số nhận định đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Hòa tan hết 31,12 gam hỗn hợp X gồm Mg, Fe, Fe3O4, FeCO3 vào dd hỗn hợp chứa H2SO4 và KNO3. Sau phản ứng thu được 4,48 lít hỗn hợp khí Y (đktc) gồm (CO2, NO, NO2, H2) có tỉ khối so với H2 là 14,6 và dd Z chỉ chứa các muối trung hòa ( Z không chứa Fe3+ ) với tổng khối lượng là m gam. Cho BaCl2 dư vào Z thấy xuất hiện 140,965 gam kết tủa trắng. Mặt khác cho NaOH dư vào Z thì thấy có 1,085 mol NaOH phản ứng đồng thời xuất hiện 42,9 gam kết tủa và 0,56 lít khí (đktc) thoát ra. Biết các phản ứng xảy ra hoàn toàn. Cho các nhận định sau:
a) Giá trị của m là 82,285 gam.
b) Số mol của KNO3 trong dung dịch ban đầu là 0,225 mol
c) Phần trăm khối lượng FeCO3 trong X là 18,638%.
d) Số mol của Fe3O4 trong X là 0,05 mol.
e) Số mol của Mg trong X là 0,15 mol.
Tổng số nhận định đúng là
A. 1
B. 2
C. 3
D. 4
Đáp án A
nH2SO4 = nSO42– = nBaSO4 = 140,965 ÷ 233 = 0,605 mol; nNH4+ = nkhí = 0,56 ÷ 22,4 = 0,025 mol.
Bảo toàn điện tích: nNa+ + nK+/Z = 2nSO42– ⇒ nKNO3 = nK+ = 0,605 × 2 - 1,085 = 0,125 mol ⇒ (b) sai
Đặt nMg2+ = x; nFe2+ = y ⇒ nNaOH = 2x + 2y + 0,025 = 1,085 mol; mkết tủa = 58x + 90y = 42,9g.
||⇒ Giải hệ có: x = 0,15 mol; y = 0,38 mol ⇒ (e) đúng.
m = 0,15 × 24 + 0,38 × 56 + 0,125 × 39 + 0,025 × 18 + 0,605 × 96 = 88,285(g) ⇒ (a) sai.
Bảo toàn khối lượng: mH2O = 31,12 + 0,605 × 98 + 0,125 × 101 - 88,285 - 0,2 × 29,2 = 8,91(g) ⇒ nH2O = 0,495 mol.
Bảo toàn nguyên tố Hidro: nH2 = 0,605 × 2 - 0,025 × 4 - 0,495 × 2)/2 = 0,06 mol.
Bảo toàn nguyên tố Nitơ: ∑n(NO,NO2) = ∑nN/Y = 0,125 - 0,025 = 0,1 mol.
⇒ nFeCO3 = nCO2 = 0,2 - 0,1 - 0,06 = 0,04 mol ⇒ %mFeCO3 = 0,04 × 116 ÷ 31,12 × 100% = 14,91% ⇒ (c) sai.
mX = mMg + mFe + mO + mCO3 ⇒ mO = 31,12 - 0,15 × 24 - 0,38 × 56 - 0,04 × 60 = 3,84(g).
⇒ nO = 0,24 mol ⇒ nFe3O4 = 0,06 mol ⇒ (d) sai ⇒ chỉ có (e) đúng
Cho hỗn hợp gồm bột nhôm và oxit sắt. Thực hiện hoàn toàn phản ứng nhiệt nhôm (giả sử chỉ có phản ứng oxit sắt thành Fe) thu được hỗn hợp chất rắn B có khối lượng 19,82 g. Chia hỗn hợp thành 2 phần bằng nhau:
- Phần 1: cho tác dụng với một lượng dư dung dịch NaOH thu được 1,68 lít khí H2 (đktc).
- Phần 2: cho tác dụng với một lượng dư dung dịch HCl thì có 3,472 lít khí H2 (đktc) thoát ra.
Công thức của oxit sắt là
A. Fe2O3.
B. Fe3O4.
C. FeO.
D. Không xác định được.
Đáp án A
Ta có sơ đồ phản ứng:
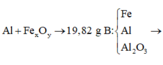
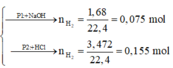
Phần 1:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
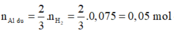
![]()
Phần 2:
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
0,05 → 0,075
Fe + 2HCl → FeCl2 + H2↑ (2)
![]()
![]()
![]()
![]()
Ta có phương trình phản ứng:
![]()
Khối lượng các chất trong 1 phần hỗn hợp B là 19,82/2 = 9,91 g
![]()
![]()
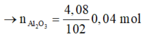
Ta có:
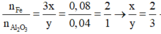
=> Oxit sắt cần tìm là Fe2O3