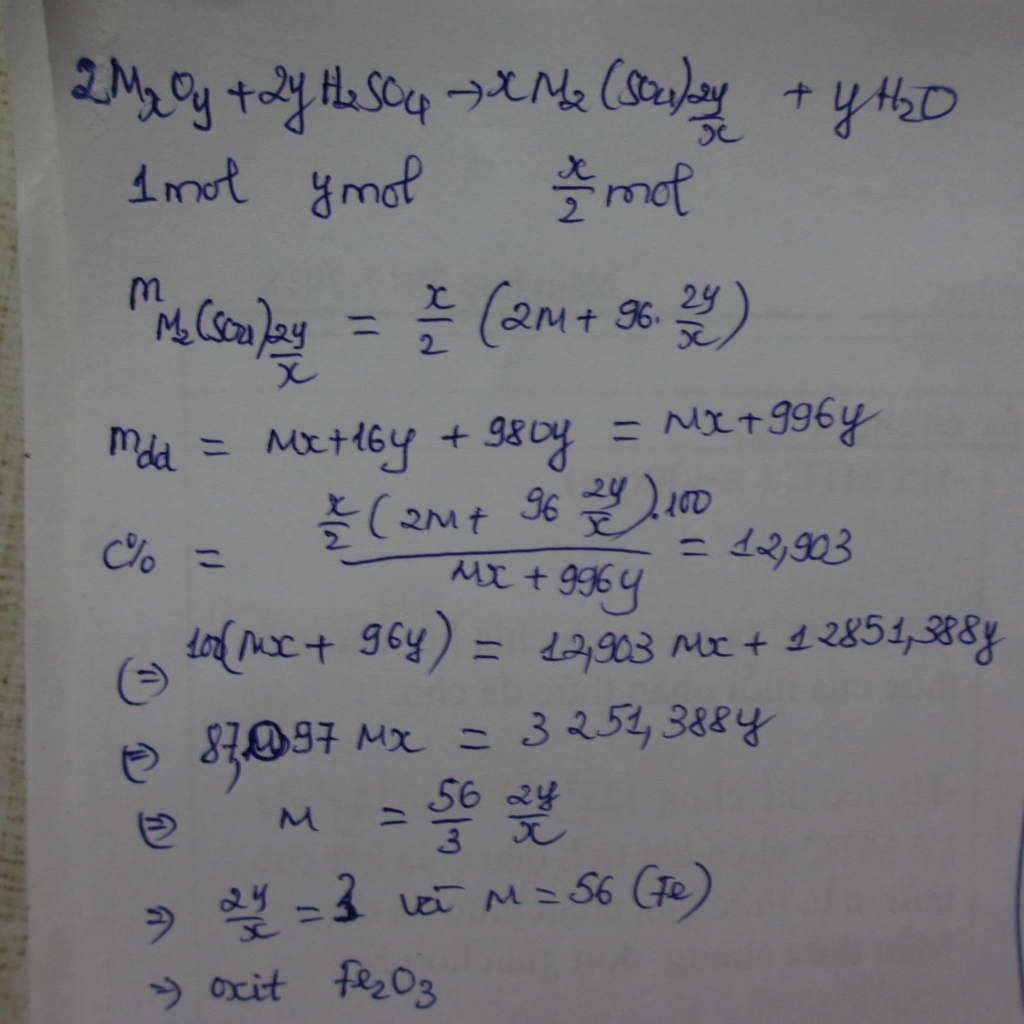Hòa tan hết 3,2 g oxit M2On trong lượng vừa đủ dd H2SO4 10% thu đc dd muối có nồng độ 12,903%.Spu đem cô cạn bớt dd và làm lạnh thu đc 7,868 g tinh thể muối và hiệu suất 70%.Xác định công thức của tinh thể muối

Những câu hỏi liên quan
Bài 1 Hòa tan 3,2 gam oxit M2Om trong một lượng vừa đủ dd H2SO4 10% thu được dd muối Sunfat 12,9%. Cô cạn dd muối rồi l làm lạnh dd thấy thoát ra 7,868 gam tinh muối sunfat với hiệu suất muối kết tinh là 70%. Hãy xác định công thức của tinh thể ngậm nước
Hòa tan 3,2 g oxit M2On trong một lương vừa đủ dd H2SO4 10 % thu được dd muối sunfat 12,9 % . Cô cạn dd muối rồi làm lạnh thấy tách ra 7,868 g tinh thể muối sunfat với hiệu suất muối kết tinh bằng 70 % . Xác định công thức tinh thể .
Hòa tan 4,8 g 1 oxit kim loại bằng dd H2SO4 10% vừa đủ, thu đc dd Muối có nồng độ 12,9%. Sau phản ứng, hạ nhiệt độ dd ấy có 13,488g muối P kết tinh với hiệu suất 80%. Xác định CT muối P
Gọi CTHH của oxit KL là A2On.
PT: \(A_2O_n+nH_2SO_4\rightarrow A_2\left(SO_4\right)_n+nH_2O\)
Ta có: \(n_{A_2O_n}=\dfrac{4,8}{2M_A+16n}\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n.n_{A_2O_n}=\dfrac{4,8n}{2M_A+16n}\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=\dfrac{4,8n}{2M_A+16n}.98=\dfrac{470,4n}{2M_A+16n}\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{\dfrac{470,4n}{2M_A+16n}}{10\%}=\dfrac{4704n}{2M_A+16}\left(g\right)\)
⇒ m dd sau pư = \(4,8+\dfrac{4704n}{2M_A+16}\left(g\right)\)
Theo PT: \(n_{A_2\left(SO_4\right)_n}=n_{A_2O_n}=\dfrac{4,8}{2M_A+16n}\left(mol\right)\)
\(\Rightarrow C\%_{A_2\left(SO_4\right)_n}=\dfrac{\dfrac{4,8.\left(2M_A+96n\right)}{2M_A+16}}{4,8+\dfrac{4704n}{2M_A+16n}}.100\%=12,9\%\)
\(\Rightarrow M_A\approx18,65m\)
Với m = 3, MA = 56 (g/mol) là thỏa mãn.
→ A là Fe.
Ta có: \(n_{Fe_2O_3}=\dfrac{4,8}{160}=0,03\left(mol\right)\)
Theo PT: \(n_{Fe_2\left(SO_4\right)_3}=n_{Fe_2O_3}=0,03\left(mol\right)\)
Gọi CTHH của muối P là Fe2(SO4)3.nH2O.
Có: H = 80% ⇒ nP = 0,03.80% = 0,024 (mol)
\(\Rightarrow M_P=\dfrac{13,488}{0,024}=562\left(g/mol\right)\)
\(\Rightarrow400+18n=562\Rightarrow n=9\)
Vậy: CTHH của P là Fe2(SO4)3.9H2O
Đúng 2
Bình luận (0)
Hòa tan hết 12,8gam oxit MxOy trong vừa đủ dd H2SO4 10%, thu được dd muối có nồng độ 12,903%. Sau phản ứng đem cô bớt dd và làm lạnh nó, thu được 35,968 gam tinh thể muối với hiệu suất 80%. Xác định công thức của tinh thể muối đó
đốt cháy hoàn toàn 12g muối sunfua kim loại R(R có hóa trị II không đổi ) thu được chất rắn A và khí B. hòa tan A bằng 1 lượng vừa đủ dd h2so4 14,5% thu được dd muối có nồng độ 33.33% . khi làm lạnh dd muối xuống nhiệt độ thấp hơn thì có 1 lượng tinh thể muối ngậm nước tách ra có khối lượng là 15,625 g. phần dd bảo hòa có nồng độ là 22,54% . xác định R và công thức của muối ngậm nước nói trên
Đọc tiếp
đốt cháy hoàn toàn 12g muối sunfua kim loại R(R có hóa trị II không đổi ) thu được chất rắn A và khí B. hòa tan A bằng 1 lượng vừa đủ dd h2so4 14,5% thu được dd muối có nồng độ 33.33% . khi làm lạnh dd muối xuống nhiệt độ thấp hơn thì có 1 lượng tinh thể muối ngậm nước tách ra có khối lượng là 15,625 g. phần dd bảo hòa có nồng độ là 22,54% . xác định R và công thức của muối ngậm nước nói trên
Cho 10 gam oxit kim loại MO tác dụng vừa đủ với dd H2SO4 24,5% thu đc dd A chứa muối trung hòa có nồng độ 33,33%. Làm lạnh dd A, thu đc dd bão hòa B có nồng độ 1600/71% và 15,625gam chất rắn C tách ra. Xác định C
PT: \(MO+H_2SO_4\rightarrow MSO_4+H_2O\)
Ta có: \(n_{MO}=\dfrac{10}{M_M+16}\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{MSO_4}=n_{MO}=\dfrac{10}{M_M+16}\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=\dfrac{10}{M_M+16}.98=\dfrac{980}{M_M+16}\left(mol\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{\dfrac{980}{M_M+16}}{24,5\%}=\dfrac{4000}{M_M+16}\left(g\right)\)
⇒ m dd A = \(10+\dfrac{4000}{M_M+16}\left(g\right)\)
\(\Rightarrow C\%_{MSO_4}=\dfrac{\left(M_M+96\right).\dfrac{10}{M_M+16}}{10+\dfrac{4000}{M_M+16}}.100\%=33,33\%\)
\(\Rightarrow M_M=64\left(g/mol\right)\)
Vậy: M là Cu.
Ta có: \(n_{CuO}=\dfrac{10}{80}=0,125\left(mol\right)=n_{CuSO_4\left(A\right)}\)
m dd A = 60 (g) ⇒ m dd B = 60 - 15,625 = 44,375 (g)
\(\Rightarrow n_{CuSO_4\left(B\right)}=\dfrac{44,375.\dfrac{1600}{71}\%}{160}=0,0625\left(mol\right)\)
BTNT Cu, có: \(n_{CuSO_4.nH_2O\left(C\right)}=0,125-0,0625=0,0625\left(mol\right)\)
\(\Rightarrow M_C=\dfrac{15,625}{0,0625}=250\left(g/mol\right)\Rightarrow n=\dfrac{250-160}{18}=5\)
Vậy: C là CuSO4.5H2O
Đúng 1
Bình luận (0)
Hòa tan 10,8 g Mg vào dd H2SO4 20 % vừa đủ , sau khi phản ứng kết thúc thu được dd X . Làm lạnh dd X xuống 20 độ C thu được 14,76 g muối sunfat kết tinh ngậm nước tách ra và còn lại dd muối bão hòa có nồng độ 21,703 % . Xác định CT muối sunfat ngậm nước .
\(n_{Mg}=\dfrac{10,8}{24}=0,45\left(mol\right)\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
0,45-->0,45------>0,45--->0,45
=> \(m_{H_2SO_4}=0,45.98=44,1\left(g\right)\)
=> \(m_{ddH_2SO_4}=\dfrac{44,1.100}{20}=220,5\left(g\right)\)
mdd (20oC) = 10,8 + 220,5 - 0,45.2 - 14,76 = 215,64 (g)
\(m_{MgSO_4\left(dd.ở.20^oC\right)}=\dfrac{215,64.21,703}{100}=46,8\left(g\right)\)
=> nMgSO4 (tách ra) = \(0,45-\dfrac{46,8}{120}=0,06\left(mol\right)\)
=> nH2O (tách ra) = \(\dfrac{14,76-0,06.120}{18}=0,42\left(mol\right)\)
Xét nMgSO4 (tách ra) : nH2O (tách ra) = 0,06 : 0,42 = 1 : 7
=> CTHH: MgSO4.7H2O
Đúng 5
Bình luận (0)
đốt cháy hoàn toàn 4,4 gam muối sunfat của một kim loại M có công thức MS trong õi dư. Chất cháy sau phản ứng đem hòa tan trong 1 lượng dd vừa đủ HNO3 37,8% thấy nồng độ phần trăm trong dd thu đc là 41,72%. Khi làm lạnh dd này thì thoát ra 8,08 gam muối rắn. Lọc tách muối rắn thấy nồng độ phần trăm của muối trong dd náy là 34,7%. Xác định công thức của muối rắn
Cho 8g một oxit kim loại hóa trị 2 tan hết trong 200g dd HCl ( vừa đủ và chưa rõ nồng độ). Cô cạn dd sau phản ứng thu được 19g muối a) xác định công thức oxit b) tính nồng độ % của dd HCl cần dùng