mmmột hỗn hợp rắn A gồm 0,2 mol Na2CO3; 0,1 mol BaCl2 và 0,1 mol MgCl2. Chỉ được dùng thêm nước hãy trình bày cách tách mỗi chất trên ra khỏi hỗn hợp.

Những câu hỏi liên quan
Cho hỗn hợp rắn gồm x mol Na2CO3, 0,2 mol NaHCO3 và 0,08 mol NaOH vào nước dư được dung dịch X, sau đó nhỏ từ từ từng giọt dung dịch HCl vào X. Tiến trình phản ứng được biểu diễn bằng đồ thị sau: Sau khi các phản ứng kết thúc thu được dung dịch E. Cô cạn dung dịch E được hỗn hợp rắn khan R. Nung R đến khối lượng không đổi được m gam rắn khan mới. Giá trị của m là
Đọc tiếp
Cho hỗn hợp rắn gồm x mol Na2CO3, 0,2 mol NaHCO3 và 0,08 mol NaOH vào nước dư được dung dịch X, sau đó nhỏ từ từ từng giọt dung dịch HCl vào X. Tiến trình phản ứng được biểu diễn bằng đồ thị sau:
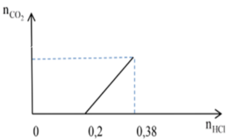
Sau khi các phản ứng kết thúc thu được dung dịch E. Cô cạn dung dịch E được hỗn hợp rắn khan R. Nung R đến khối lượng không đổi được m gam rắn khan mới. Giá trị của m là
![]()
![]()
![]()
![]()
Cho hỗn hợp rắn gồm x mol Na2CO3, 0,2 mol NaHCO3 và 0,08 mol NaOH vào nước dư được dung dịch X, sau đó nhỏ từ từ từng giọt dung dịch HCl vào X. Tiến trình phản ứng được biểu diễn bằng đồ thị sau: Sau khi các phản ứng kết thúc thu được dung dịch E. Cô cạn dung dịch E được hỗn hợp rắn khan R. Nung R đến khối lượng không đổi được m gam rắn khan mới. Giá trị của m là A. 30,85 B. 29,65 C. 33,99 D. 26,57
Đọc tiếp
Cho hỗn hợp rắn gồm x mol Na2CO3, 0,2 mol NaHCO3 và 0,08 mol NaOH vào nước dư được dung dịch X, sau đó nhỏ từ từ từng giọt dung dịch HCl vào X. Tiến trình phản ứng được biểu diễn bằng đồ thị sau:
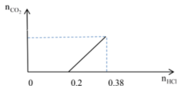
Sau khi các phản ứng kết thúc thu được dung dịch E. Cô cạn dung dịch E được hỗn hợp rắn khan R. Nung R đến khối lượng không đổi được m gam rắn khan mới. Giá trị của m là
A. 30,85
B. 29,65
C. 33,99
D. 26,57
Đáp án B
X gồm: Na2CO3 (x + 0,08) mol; NaHCO3 (0,12 mol)
Nhỏ từ từ HCl vào dung dịch, tại thời điểm 0,2 mol HCl khí mới bắt đầu thoát ra:
CO32- + H+ → HCO3-.
x + 0,08 → x + 0,08
→ x + 0,08 = 0,2 → x = 0,12 mol
Tại thời điểm 0,38 mol HCl:
CO32- + H+ → HCO3-.
0,2 → 0,2 → 0,2
HCO3- + H+ → CO2 + H2O
0,18← 0,18 → 0,18
Dung dịch thu được có: Na+ (0,12. 2 + 0,2 + 0,08 = 0,52 mol); Cl- (bằng mol H+ = 0,38 mol); HCO3- (0,2 + 0,12 – 0,18 = 0,14 mol)
Khi nung nóng: 2HCO3- → CO32- + CO2 + H2O.
Vậy chất rắn thu được: m = 0,52. 23 + (0,14 : 2). 60 + 0,38. 35,5 = 29,65 (gam)
Đúng 0
Bình luận (0)
Tính khối lượng mol trung bình của các hỗn hợp sau: a. Hỗn hợp gồm 0,1 mol CO2 và 0,2 mol CO b. Hỗn hợp gồm 0,2 mol N2 và 0,3 mol H2 c. Hỗn hợp gồm 0,1 mol N2; 0,2 mol NO và 0,2 mol N2O d. Hỗn hợp gồm 0,2 mol Fe; 0,1 mol Mg và 0,1 mol Al
Đọc tiếp
Tính khối lượng mol trung bình của các hỗn hợp sau:
a. Hỗn hợp gồm 0,1 mol CO2 và 0,2 mol CO
b. Hỗn hợp gồm 0,2 mol N2 và 0,3 mol H2
c. Hỗn hợp gồm 0,1 mol N2; 0,2 mol NO và 0,2 mol N2O
d. Hỗn hợp gồm 0,2 mol Fe; 0,1 mol Mg và 0,1 mol Al
a, \(\overline{M}=\dfrac{0,1.44+0,2.28}{0,1+0,2}\approx33,33\left(g/mol\right)\)
b, \(\overline{M}=\dfrac{0,2.28+0,3.2}{0,2+0,3}=12,4\left(g/mol\right)\)
c, \(\overline{M}=\dfrac{0,1.28+0,2.30+0,2.44}{0,1+0,2+0,2}=35,2\left(g/mol\right)\)
d, \(\overline{M}=\dfrac{0,2.56+0,1.24+0,1.27}{0,2+0,1+0,1}=40,75\left(g/mol\right)\)
Đúng 1
Bình luận (0)
Một dung dịch X gồm 0,1 mol Ca2+; 0,2 mol Na+, x mol và 0,2 mol . Cô cạn dung dịch rồi nung hỗn hợp rắn tới khối lượng không đổi ta thu được m gam chất rắn. Giá trị của m là A.3,92 B. 11,22 C. Đ/a khác D. 17,3
Đọc tiếp
Một dung dịch X gồm 0,1 mol Ca2+; 0,2 mol Na+, x mol và 0,2 mol . Cô cạn dung dịch rồi nung hỗn hợp rắn tới khối lượng không đổi ta thu được m gam chất rắn. Giá trị của m là
A.3,92
B. 11,22
C. Đ/a khác
D. 17,3
Đáp án D
Áp dụng định luật bào toàn điện tích cho dung dịch ban đầu ta có
![]()
Khi cô cạn dung dịch thì có phản ứng sau xảy ra
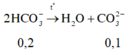
Sau khi dung dịch đã bay hơi hết nước và cô cạn chất rắn tới khối lượng lượng không đổi, nên có phản ứng sau:
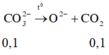
Chú ý: Cách viết phương trình trên không đúng với bản chất hóa học do chất rắn không thể viết được dưới dạng ion nhưng ta có thể viết để có thể đơn giản cách giải trở nên nhanh chóng trong các bài tập trắc nghiệm.
Tuy nhiên các bạn cũng cần lưu ý rằng muối cacbonat của kim loại kiềm không bị nhiệt phân nên lượng muối cacbonat bị nhiệt phần chỉ tương ứng với ion Ca2+ (muối CaCO3) nên nếu thì ![]()
còn lại vẫn tồn tại dưới dạng muối cacbonat của kim loại kiềm. Do vậy nếu không nắm chắc bản chất phản ứng, các bạn vẫn nên viết phản ứng nhiệt phân muối cacbonat dạng phân tử:
![]()
Do đó khối lượng chất rắn thu được cuối cùng là tổng khối lượng của 0,1 mol CaO và 0,2 mol NaCl.
Vậy khối lượng của chất rắn là
m = 0,1.56+0,2.58,5 = 17,3 (gam)
Đúng 0
Bình luận (0)
Hỗn hợp X gồm (0,3 mol Zn và 0,2 mol Al) phản ứng vừa đủ với 0,45 mol hỗn hợp Y gồm (Cl2, O2) thu được x gam chất rắn. phần trăm khối lượng của oxi trong Y và giá trị của x tương ứng là A. 24,32% và 64 B. 18,39% và 51 C. 13,26% và 46 D. 21,11% và 56
Đọc tiếp
Hỗn hợp X gồm (0,3 mol Zn và 0,2 mol Al) phản ứng vừa đủ với 0,45 mol hỗn hợp Y gồm (Cl2, O2) thu được x gam chất rắn. phần trăm khối lượng của oxi trong Y và giá trị của x tương ứng là
A. 24,32% và 64
B. 18,39% và 51
C. 13,26% và 46
D. 21,11% và 56
Giải thích: Đáp án B
Gọi số mol Cl2 và O2 lần lượt là x và y mol
=> ∑ nhh = x + y = 0,45 (mol)
∑ n e (KL nhường) = ∑ n e ( Cl2, O2 nhận) <=> 2.0,3 + 3.0,2 = 2x + 4y (2)
Từ (1) và ( 2) => x = 0,3 và y = 0,15 mol
% mO2 = [ ( 0,15.32): ( 0,15.32 + 0,3.71)]. 100% = 18,39%
BTKL: x = mKL + mhh khí = 0,3.65 + 0,2.27 + 0,3.71 + 0,15. 32 = 51 (g)
Đúng 0
Bình luận (0)
Đốt hoàn toàn 0,2 mol hỗn hợp X gồm etyl axetat và metyl acrylat thu được số mol CO2 nhiều hơn số mol H2O là 0,08 mol. Nếu đun 0,2 mol hỗn hợp X trên với 400 ml dd KOH 0,75M rồi cô cạn dung dịch sau phản ứng thì số gam chất rắn khan thu được là A. 20,56 B. 26,64 C. 26,16 D. 26,40
Đọc tiếp
Đốt hoàn toàn 0,2 mol hỗn hợp X gồm etyl axetat và metyl acrylat thu được số mol CO2 nhiều hơn số mol H2O là 0,08 mol. Nếu đun 0,2 mol hỗn hợp X trên với 400 ml dd KOH 0,75M rồi cô cạn dung dịch sau phản ứng thì số gam chất rắn khan thu được là
A. 20,56
B. 26,64
C. 26,16
D. 26,40
Đáp án : C
X gồm x mol CH3COOC2H5 và y mol CH2=CHCOOCH3
=> x + y = 0,2 mol
Khi đốt cháy X : nCO2 – nH2O = y = 0,08 mol
=> x = 0,12 mol
X + 0,3 mol KOH
=> sản phẩm gồm : 0,08 mol CH2=CHCOOK ; 0,12 mol CH3COOK ; 0,1 mol KOH
=> m = 26,16g
Đúng 0
Bình luận (0)
Hỗn hợp X gồm 0,3 mol Zn và 0,2 mol Al phản ứng vừa đủ với 0,45 mol hỗn hợp Y gồm khí Cl2 và O2, thu được x gam chất rắn. Phần trăm khối lượng của O2 trong Y và giá trị của x tương ứng là A. 18,39% và 51 B. 21,11% và 56 C. 13,26% và 46. D. 24,32% và 64
Đọc tiếp
Hỗn hợp X gồm 0,3 mol Zn và 0,2 mol Al phản ứng vừa đủ với 0,45 mol hỗn hợp Y gồm khí Cl2 và O2, thu được x gam chất rắn. Phần trăm khối lượng của O2 trong Y và giá trị của x tương ứng là
A. 18,39% và 51
B. 21,11% và 56
C. 13,26% và 46.
D. 24,32% và 64
Đáp án A
► Đặt nCl2 = a; nO2 = b ⇒ nY = a + b = 0,45 mol.
Bảo toàn electron: 2a + 4b = 0,3 × 2 + 0,2 × 3 ||⇒ giải hệ cho:
a = 0,3 mol; b = 0,15 mol ⇒ %mO2 = 18,39%.
● Bảo toàn khối lượng: x = 51(g)
Đúng 0
Bình luận (0)
Hỗn hợp X gồm 0,3 mol Zn và 0,2 mol Al phản ứng vừa đủ với 0,45 mol hỗn hợp Y gồm khí Cl2 và O2, thu được x gam chất rắn. Phần trăm khối lượng của O2 trong Y và giá trị của x tương ứng là
A. 18,39% và 51.
B. 21,11% và 56.
C. 13,26% và 46.
D. 24,32% và 64.
Đáp án A
► Đặt nCl2 = a; nO2 = b ⇒ nY = a + b = 0,45 mol.
Bảo toàn electron: 2a + 4b = 0,3 × 2 + 0,2 × 3 ||⇒ giải hệ cho:
a = 0,3 mol; b = 0,15 mol ⇒ %mO2 = 18,39%.
● Bảo toàn khối lượng: x = 51(g)
Đúng 0
Bình luận (0)
Hỗn hợp X gồm 0,3 mol Zn và 0,2 mol Al phản ứng vừa đủ với 0,45 mol hỗn hợp Y gồm khí Cl2 và O2, thu được x gam chất rắn. Phần trăm khối lượng của O2 trong Y và giá trị của x tương ứng là A. 18,39% và 51 B. 21,11% và 56 C. 13,26% và 46 D. 24,32% và 64
Đọc tiếp
Hỗn hợp X gồm 0,3 mol Zn và 0,2 mol Al phản ứng vừa đủ với 0,45 mol hỗn hợp Y gồm khí Cl2 và O2, thu được x gam chất rắn. Phần trăm khối lượng của O2 trong Y và giá trị của x tương ứng là
A. 18,39% và 51
B. 21,11% và 56
C. 13,26% và 46
D. 24,32% và 64
Đáp án A
► Đặt nCl2 = a; nO2 = b
⇒ nY = a + b = 0,45 mol.
Bảo toàn electron: 2a + 4b = 0,3 × 2 + 0,2 × 3
⇒ giải hệ cho:
a = 0,3 mol; b = 0,15 mol
⇒ %mO2 = 18,39%.
● Bảo toàn khối lượng: x = 51(g)
Đúng 0
Bình luận (0)








