Cho 2,7 gam kim loại R tan hết trong 100ml dung dịch H2SO4 dư thu được 12,7 gam muối. Xác định tên kim loại.
Cho 16,8 gam một kim loại R hóa trị 2 tan hoàn toàn trong dung dịch H2SO4 loãng thu được 6,72 lít khí (điều kiện tiêu chuẩn).Xác định tên kim loại ( R) và khối lượng muối thu được.
$R + H_2SO_4 \to RSO_4 + H_2$
$n_R = n_{H_2} = \dfrac{6,72}{22,4} = 0,3(mol)$
$M_R = \dfrac{16,8}{0,3} =56(Fe)$
Vậy R là Sắt
$n_{FeSO_4} = n_{H_2} = 0,3(mol)$
$m_{FeSO_4} = 0,3.152 =45,6(gam)$
1) Xác định tên kim loại A và M khi:
a) Hòa tan hoàn toàn 2,7 gam kim loại A (hóa trị III) trong dung dịch HCl dư sau phản ứng thu được 13,35 gam muối.
b) Hòa tan hoàn toàn 4,8 gam kim loại M trong dung dịch HCl dư sau phản ứng thu được 4,48 lit khí (đktc).
\(a,n_A=\dfrac{2,7}{M_A}\left(mol\right)\\ n_{ACl_3}=\dfrac{13,35}{M_A+106,5}\)
PTHH: \(2A+6HCl\rightarrow2ACl_3+3H_2\)
\(\dfrac{2,7}{M_A}\)-------------->\(\dfrac{2,7}{M_A}\)
\(\rightarrow\dfrac{2,7}{M_A}=\dfrac{13,35}{M_A+106,5}\\ \Leftrightarrow M_A=27\left(g\text{/}mol\right)\)
=> A là Al
\(b,n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: \(2M+2nHCl\rightarrow2MCl_n+nH_2\) (n là hoá trị của M, n ∈ N*)
\(\dfrac{0,4}{n}\)<---------------------------0,2
\(\rightarrow M_M=\dfrac{4,8}{\dfrac{0,2}{n}}=12n\left(g\text{/}mol\right)\)
Vì n là hoá trị của M nên ta có bảng
| n | 1 | 2 | 3 |
| MM | 12 | 24 | 36 |
| Loại | Mg | Loại |
Vậy M là Mg
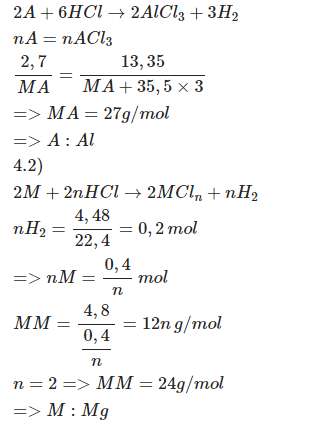
\(\Rightarrow\) \(M:mg\)
Câu4:Cho 2,7 gam kim loại A(hoá trịIll)Tan hoàn toàn trong dung dịch axit sunfuric Loãng dư thu được muối và 3,36lít khí hiđrô(đktc) a)Xác định kim loại A b)Tính khối lượng muối tạo thành
\(n_{H_2\left(dktc\right)}=\dfrac{V}{22,4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ PTHH:2A+3H_2SO_4->A_2\left(SO_4\right)_3+3H_2\)
tỉ lệ 2 : 3 : 1 : 3
n(mol) 0,1<------0,15<------------0,05<-------0,15
\(=>M_A=\dfrac{m}{n}=\dfrac{2,7}{0,1}=27\left(g/mol\right)\)
`=>A` là nhôm
`=>` muối là `Al_2 (SO_4)_3`
\(m_{Al_2\left(SO_4\right)_3}=n\cdot M=0,05\cdot342=17,1\left(g\right)\)
a, \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PT: \(2A+3H_2SO_4\rightarrow A_2\left(SO_4\right)_3+3H_2\)
Theo PT: \(n_A=\dfrac{2}{3}n_{H_2}=0,1\left(mol\right)\Rightarrow M_A=\dfrac{2,7}{0,1}=27\left(g/mol\right)\)
→ A là nhôm.
b, Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}n_{H_2}=0,05\left(mol\right)\Rightarrow m_{Al_2\left(SO_4\right)_3}=0,05.342=17,1\left(g\right)\)
Hòa tan hết 5,4 gam kim loại R (hóa trị III) vào dung dịch H2SO4 loãng thu được 6,72 lít H2 (ở đktc) a/ Xác định tên kim loại b/ Nếu dùng 5,4 gam kim loại trên cho tác dụng hết với H2SO4 đặc nóng thì thể tích khí đo được ở đktc là bao nhiêu
Hòa tan hết 5,4 gam kim loại R (hóa trị III) vào dung dịch H2SO4 loãng thu được 6,72 lít H2 (ở đktc) a/ Xác định tên kim loại b/ Nếu dùng 5,4 gam kim loại trên cho tác dụng hết với H2SO4 đặc nóng thì thể tích khí đo được ở đktc là bao nhiêu
\(n_{H2\left(dktc\right)}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a) Pt : \(2R+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2|\)
2 3 1 3
0,2 0,3
\(n_R=\dfrac{0,3.2}{3}=0,2\left(mol\right)\)
⇒ \(M_R=\dfrac{5,4}{0,2}=27\left(dvc\right)\)
Vậy kim loại R là nhôm
b) \(2Al+6H_2SO_{4\left(đặc,nóng\right)}\rightarrow Al_2\left(SO_4\right)_3+3SO_2+6H_2O|\)
2 6 1 3 6
0,2 0,3
\(n_{SO2}=\dfrac{0,3.3}{2}=0,3\left(mol\right)\)
\(V_{SO2\left(dktc\right)}=0,3.22,4=6,72\left(l\right)\)
Chúc bạn học tốt
a) PTHH: \(2R+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\) \(\Rightarrow n_R=0,2\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{5,4}{0,2}=27\) \(\Rightarrow\) R là Nhôm (Al)
b) PTHH: \(2Al+6H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}Al_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
Theo PTHH: \(n_{SO_2}=0,3\left(mol\right)\) \(\Rightarrow V_{SO_2}=0,3\cdot22,4=6,72\left(l\right)\)
Hòa tan 19,2 gam một kim loại R vào dung dịch HCl dư thu được 17,92 lít khí (đktc). Xác định tên kim loại R.
Gọi \(n\) là hóa trj của kim loại R.
\(n_{H_2}=\dfrac{17,92}{22,4}=0,8mol\)
\(2R+2nHCl\rightarrow2RCl_n+nH_2\)
\(\dfrac{19,2}{M_R}\) 0,8
\(\Rightarrow\dfrac{19,2}{M_R}\cdot n=0,8\cdot2\Rightarrow19,2n=1,6M_R\Rightarrow M_R=12n\)
Nhận thấy \(n=2\left(tm\right)\)\(\Rightarrow M_R=24đvC\)
Vậy R là kim loại Mg.
Cho 2,7 gam một kim loại R hóa trị 3 tan hoàn toàn trong dung dịch HNO3
loãng thu được 2,24 lít khí NO duy nhất (điều kiện tiêu chuẩn).
a. Xác định tên của R?
b. Xác định khối lượng muối thu được?
(Cho khối lượng nguyên tử: K = 39; Ag = 108; Fe = 56; Cu = 64; Al = 27;
Pb = 207; H = 1; N = 14; O = 16)
giúp e với ạ
nNO = 2,25/22,4 = 0,1 (mol)
PTHH: R + 4HNO3 -> R(NO3)3 + NO + 2H2O
nR = nR(NO3)3 = nNO = 0,1 (mol)
MR = 2,7/0,1 = 27 (g/mol)
<=> R là nhôm (Al)
Muối thu được: Al(NO3)3
mAl(NO3)3 = 0,1 . 213 = 21,3 (g)
R+4HNO3->R(NO3)3+NO+2H2O
n NO=\(\dfrac{2,24}{22,4}\)=0,1 mol
=>\(\dfrac{2,7}{M_R}\)=0,1 mol
=>MR=27 g\mol
=>R là Al (nhôm )
->m Al(NO3)3=0,1.213=21,3g
Cách 1:
PT: \(2A+2H_2O\rightarrow2AOH+H_2\)
Ta có: \(n_A=\dfrac{6,9}{M_A}\left(mol\right)\)
\(n_{AOH}=\dfrac{12}{M_A+17}\left(mol\right)\)
Theo PT: \(\dfrac{6,9}{M_A}=\dfrac{12}{M_A+17}\)
\(\Rightarrow M_A=23\left(g/mol\right)\)
Vậy: A là Na.
Cách 2:
Bazơ thu được là AOH.
Ta có: mAOH = mA + mOH
⇒ mOH = 12 - 6,9 = 5,1 (g)
\(\Rightarrow n_{OH}=\dfrac{5,1}{17}=0,03\left(mol\right)\)
⇒ nA = nOH = 0,03 (mol)
\(\Rightarrow M_A=\dfrac{6,9}{0,03}=23\left(g/mol\right)\)
Vậy: A là Na.
Bạn tham khảo nhé!
Cho 0,72 gam kim loại R tác dụng với 120 gam dung dịch HCL a% thu được 120,66 gam dung dịch A a) Xác định tên kim loại R b) Tính a c) Tính C% của chất tan trong dung dịch A
\(PTHH:2R+2nHCl\rightarrow2RCl_n+nH_2\)
\(\left(mol\right)\) \(\dfrac{0,72}{R}\) \(\dfrac{0,72n}{R}\) \(\dfrac{0,72}{R}\) \(\dfrac{0,36n}{R}\)
\(a.\)Theo đề bài ta có:
\(0,72+120-\dfrac{0,36n}{R}.2=120,66\Leftrightarrow R=12n\)
Biện luận: \(\Rightarrow\left\{{}\begin{matrix}n=2\\R=24\left(Mg:Magie\right)\end{matrix}\right.\)
\(b.\) Khi đó: \(n_{HCl}=0,06\left(mol\right)\rightarrow a=\dfrac{0,06.36,5}{120}.100\%=1.825\left(\%\right)\)
\(c.C\%_{ddMgCl_2}=\dfrac{0,03.95}{120,66}.100\%=2,362\left(\%\right)\)
$m_{H_2} = 0,72 + 120 -120,66 = 0,06(gam)$
$n_{H_2} = 0,03(mol)$
Gọi n là hóa trị của R
$2R + 2nHCl \to 2RCl_n + nH_2$
Theo PTHH :
$n_R = \dfrac{2}{n}n_{H_2} = \dfrac{0,06}{n}(mol)$
Suy ra: $\dfrac{0,06}{n}.R = 0,72 \Rightarrow R = 12n$
Với n = 2 thì R = 24(Magie)
b)
$n_{HCl} = 2n_{H_2} = 0,06(mol)$
$C\%_{HCl} = \dfrac{0,06.36,5}{120}.100\% = 1,825\%$
(a = 1,825)
c)
$C\%_{MgCl_2} = \dfrac{0,03.95}{120,66}.100\% = 2,36\%$