Cho 33,8g H2so4.3SO3 hòa tan hoàn toàn vào 800ml dung dịch H2SO4 19%, D=1.25g/ml tạo ra dung dịch A. Tính C% của dung dịch A

Những câu hỏi liên quan
Hòa tan hoàn toàn 19,6 gam Fe vào 200 ml dung dịch H2SO4 loãng
a, viết PTHH
b, Tính thể tích khí H2 thoát ra ở đktc
c, Tính nồng độ mol của dung dịch axit đã dùng
d, Tính khối lượng muối tạo thành
e, Tính nồng độ mol của dung dịch muối tạo thành. Biết thể tích dung dịch không đổi.
f, Nếu hòa tan 19,6 gam Fe ở trên vào 250 ml dung dịch H2SO4 1,6M thì sau phản ứng, chất nào dư và dư bao nhiêu gam.
Đọc tiếp
Hòa tan hoàn toàn 19,6 gam Fe vào 200 ml dung dịch H2SO4 loãng
a, viết PTHH
b, Tính thể tích khí H2 thoát ra ở đktc
c, Tính nồng độ mol của dung dịch axit đã dùng
d, Tính khối lượng muối tạo thành
e, Tính nồng độ mol của dung dịch muối tạo thành. Biết thể tích dung dịch không đổi.
f, Nếu hòa tan 19,6 gam Fe ở trên vào 250 ml dung dịch H2SO4 1,6M thì sau phản ứng, chất nào dư và dư bao nhiêu gam.
a, PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b, Ta có: \(n_{Fe}=\dfrac{19,6}{56}=0,35\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Fe}=0,35\left(mol\right)\Rightarrow V_{H_2}=0,35.22,4=7,84\left(l\right)\)
c, \(n_{H_2SO_4}=n_{Fe}=0,35\left(mol\right)\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,35}{0,2}=1,75\left(M\right)\)
d, \(n_{FeSO_4}=n_{Fe}=0,35\left(mol\right)\Rightarrow m_{FeSO_4}=0,35.152=53,2\left(g\right)\)
e, \(C_{M_{FeSO_4}}=\dfrac{0,35}{0,2}=1,75\left(M\right)\)
d, \(n_{H_2SO_4}=0,25.1,6=0,4\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{n_{Fe}}{1}< \dfrac{n_{H_2SO_4}}{1}\), ta được H2SO4 dư.
Theo PT: \(n_{H_2SO_4\left(pư\right)}=n_{Fe}=0,35\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=0,4-0,35=0,05\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4\left(dư\right)}=0,05.98=4,9\left(g\right)\)
Đúng 2
Bình luận (0)
Cho 3,9g Kali vào 52,2g nước. Phản ứng xảy ra hoàn toàn. a) Tính thể tích chất khí sinh ra (đkc). Tính C% dung dịch tạo thành. b) Cần bao nhiêu ml dung dịch H2SO4 0,8M để trung hòa dung dịch ở trên? giúp em với ạaaa gấpp lắmmm
a) \(n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\)
PTHH: 2K + 2H2O → 2KOH + H2
Mol: 0,1 0,1 0,05
\(V_{H_2}=0,05.22,4=1,12\left(l\right)\)
\(C\%_{ddKOH}=\dfrac{0,1.56.100\%}{3,9+52,2-0,05.2}=10\%\)
b,
PTHH: 2KOH + H2SO4 → K2SO4 + H2O
Mol: 0,1 0,05
\(V_{ddH_2SO_4}=\dfrac{0,05}{0,8}=0,0625\left(l\right)=62,5\left(ml\right)\)
Đúng 1
Bình luận (0)
\(n_K=\dfrac{3,9}{39}=0,1\left(mol\right)\\ 2K+2H_2O\rightarrow2KOH+H_2\\ 0,1.......0,1........0,1..........0,05\left(mol\right)\\ a.V_{H_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\\ m_{ddKOH}=3,9+52,2-0,05.2=56\left(g\right)\\ C\%_{ddKOH}=\dfrac{0,1.56}{56}.100=10\%\\ b.H_2SO_4+2KOH\rightarrow K_2SO_4+2H_2O\\ 0,05.........0,1..........0,05...........0,1\left(mol\right)\\ V_{ddH_2SO_4}=\dfrac{0,05}{0,8}=0,0625\left(l\right)=62,5\left(ml\right)\)
Đúng 0
Bình luận (0)
axit H2SO4 100% hấp thụ SO3 tạo ra oleum theo phương trình H2SO4 + SO3 -> H2SO4.nSO3 . Hòa tan 6,76 gam gam oleum vào nước thành 200 ml dung dịch H2SO4 . 10 ml dung dịch trung hòa vừa hết 16 ml dung dịch NaOH 0,5 M a- tính n b- tính hàm lượng % SO3 trong oleum c- cần có bao nhiêu gam oleum có hàm lượng SO3 như trên để pha vào 100 ml dung dịch H2SO4 40% , d= 1,31 g/ml để tạo ra oleum có hàm lượng SO3 là 10%.
H2SO4 + nSO3 => H2SO4.nSO3
H2SO4.nSO3 + nH2O >> n+1H2SO4
H2SO4 + 2NaOH >> Na2SO4 + 2H2O
Số mol NaOH = 0,008 , số mol H2SO4 200ml = 0,008/2 . 200/10 =0,08
Theo (2) nH2SO4.nSO3 =0,08/n+1
MH2SO4.nSO3 =98 +80n = 6,76/0,08/n+1 =84,5n+ 84,5
13,5 =4,5n
=>n=3
%SO3=3.80/2.80+98 =71%
c,Theo câu b , hàm lượng % của SO3 có trong oleum trên là 71
Cứ 100g oleum có 71g SO3 và 29g H2SO4 Khi đó mdd = 1,31.100 = 131g
a g có 71a/100 ...............29a/100
Vì dd H2SO4 có C=40%
Cứ 100g dd có 40g H2SO4 và 60g H2O
=>131g >> 131.40/100 = 52,4g H2SO4 và 131.60/100 = 78,6 g H2O
Khi cho oleum vào dd H2SO4 thì SO3+H2O
SO3 + H2O >> H2SO4
Cứ 80g cần 18g >> 98g
Vậy ..x..g cần 78,6g >>..y..g
x= 78,6.80/18 = 349,3g
y= 78,6.98/18 = 427,9g
Trong loại oleum mới 10% thì mSO3 = 71a/100 -349,3g
và mH2SO4 = 29a/100 +52,4+ 427,9
=> 71a/100 -349,4 / 29a/100 +480,3 = 10/90
=> Bạn ấn máy tìm a nhé
Đúng 1
Bình luận (0)
1/. Hòa tan hoàn toàn 2,22 gam hỗn hợp A gồm ( Al ; Fe ) bằng dung dịch Axit H2SO4 dư . Sau pư thu được dung dịch B và có 1344 ml khí H2 ở ĐKTC bay ra .a. Tính phần trăm khối lượng mỗi chất có trong hỗn hợp X .b. Nếu cho dung dịch NaOH dư vào dung dịch B ở trên thì thu được kết tủa D . Nung D trong không khí đến khối lượng không đổi thì thu được m gam chất rắn E . Tính giá trị của m .
Đọc tiếp
1/. Hòa tan hoàn toàn 2,22 gam hỗn hợp A gồm ( Al ; Fe ) bằng dung dịch Axit H2SO4 dư . Sau pư thu được dung dịch B và có 1344 ml khí H2 ở ĐKTC bay ra .
a. Tính phần trăm khối lượng mỗi chất có trong hỗn hợp X .
b. Nếu cho dung dịch NaOH dư vào dung dịch B ở trên thì thu được kết tủa D . Nung D trong không khí đến khối lượng không đổi thì thu được m gam chất rắn E . Tính giá trị của m .
Nhỏ từ từ dung dịch NaOH 1 m vào 50 ml vào dung dịch H2SO4 khi H2SO4 được trung hòa hoàn toàn thì thấy dùng hết 40 ml dung dịch NaOH A viết BTHH của phản ứng Tính nồng độ dung dịch H2SO4 ban đầu Nêu cách nhận biết thời điểm H2SO4 trung hòa hoàn toàn
\(A.2NaOH+H_2SO_4\rightarrow Na_2SO_4+H_2O\\ n_{NaOH}=0,04.1=0,04mol\\ n_{H_2SO_4}=0,04:2=0,02mol\\ C_{M\left(H_2SO_4\right)}=\dfrac{0,02}{0,05}=0,4M\)
Cho quỳ tím vào dd \(H_2SO_4\) rồi nhỏ từ từ dd \(NaOH\) vào. Đến khi thấy quỳ tím từ màu đỏ trở về màu tím thì đó là thời điểm \(H_2SO_4\) được trung hoà hoàn toàn.
Đúng 4
Bình luận (2)
Hòa tan hoàn toàn a gam Al trong dung dịch Ba(OH)2, thu được dung dịch X. Nhỏ rất từ từ dung dịch H2SO4 0,5M vào dung dịch X và lắc nhẹ để các phản ứng xảy ra hoàn toàn. Đồ thị biểu diễn sự phụ thuộc tổng khối lượng kết tủa (m gam) theo thể tích dung dịch H2SO4 (V ml) như sau: Giá trị của a là A. 8,10. B. 4,05. C. 5,40. D. 6,75.
Đọc tiếp
Hòa tan hoàn toàn a gam Al trong dung dịch Ba(OH)2, thu được dung dịch X. Nhỏ rất từ từ dung dịch H2SO4 0,5M vào dung dịch X và lắc nhẹ để các phản ứng xảy ra hoàn toàn. Đồ thị biểu diễn sự phụ thuộc tổng khối lượng kết tủa (m gam) theo thể tích dung dịch H2SO4 (V ml) như sau:
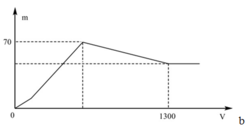
Giá trị của a là
A. 8,10.
B. 4,05.
C. 5,40.
D. 6,75.
Giải thích:
Giả sử số mol ban đầu: nAl = x mol, nBa(OH)2 = y mol
2Al + Ba(OH)2 + 2H2O→ Ba(AlO2)2 + 3H2
x 0,5x 0,5x
Dung dịch X: Ba(AlO2)2 (0,5x mol) và Ba(OH)2 dư (y-0,5x mol)
+ Khi kết tủa lớn nhất: m↓ = mAl(OH)3 max + mBaSO4 max = 78x + 233y = 70 (1)
+ Khi V= 1300 ml: Al(OH)3 vừa bị hòa tan hết. Khi đó ta có:
OH- + H+ → H2O
H+ + AlO2- + H2O → Al(OH)3
3H+ + Al(OH)3 → Al3+ + 3H2O
nH+ = nOH- dư + nAlO2- + 3nAl(OH)3 max => 2.1,3.0,5 = 2y – x + x + 3x <=> 3x + 2y = 1,3 (2)
Giải (1) và (2): x = 0,3; y = 0,2
=> a = 0,3.27 = 8,1 gam
Đáp án A
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn a gam Al trong dung dịch Ba(OH)2, thu được dung dịch X. Nhỏ rất từ từ dung dịch H2SO4 0,5M vào dung dịch X và lắc nhẹ để các phản ứng xảy ra hoàn toàn. Đồ thị biểu diễn sự phụ thuộc tổng khối lượng kết tủa (m gam) theo thể tích dung dịch H2SO4 (V ml) như sau: Giá trị của a là A. 8,10. B. 4,05. C. 5,40. D. 6,75.
Đọc tiếp
Hòa tan hoàn toàn a gam Al trong dung dịch Ba(OH)2, thu được dung dịch X. Nhỏ rất từ từ dung dịch H2SO4 0,5M vào dung dịch X và lắc nhẹ để các phản ứng xảy ra hoàn toàn. Đồ thị biểu diễn sự phụ thuộc tổng khối lượng kết tủa (m gam) theo thể tích dung dịch H2SO4 (V ml) như sau:
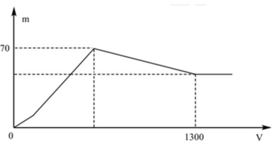
Giá trị của a là
A. 8,10.
B. 4,05.
C. 5,40.
D. 6,75.
Đáp án A
Quan sát nhanh: đoạn OAB có điểm gấp khúc tại A => Cho biết X gồm Ba(AlO2)2 và Ba(OH)2


Đúng 0
Bình luận (0)
Hòa tan hoàn toàn a gam Al trong dung dịch Ba(OH)2, thu được dung dịch X. Nhỏ rất từ từ dung dịch H2SO4 0,5M vào dung dịch X và lắc nhẹ để các phản ứng xảy ra hoàn toàn. Đồ thị biểu diễn sự phụ thuộc tổng khối lượng kết tủa (m gam) theo thể tích dung dịch H2SO4 (V ml) như sau: Giá trị của a là A. 8,10. B. 4,05. C. 5,40. D. 6,75
Đọc tiếp
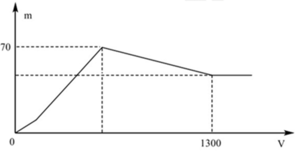
Hòa tan hoàn toàn a gam Al trong dung dịch Ba(OH)2, thu được dung dịch X. Nhỏ rất từ từ dung dịch H2SO4 0,5M vào dung dịch X và lắc nhẹ để các phản ứng xảy ra hoàn toàn. Đồ thị biểu diễn sự phụ thuộc tổng khối lượng kết tủa (m gam) theo thể tích dung dịch H2SO4 (V ml) như sau:
Giá trị của a là
A. 8,10.
B. 4,05.
C. 5,40.
D. 6,75
Đáp án B
Chọn n A g = 4
TN1: n f r u c t o z ơ = 2 → m1 = 360 gam
TN2: n g l u c o z ơ = n f r u c t o z ơ = 1 → n s a c c a r o z ơ = 1 → m2 = 1∙342/75% = 456 gam
→ m1/m2 = 15/19 → 19m1 = 15m2
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn a gam Al trong dung dịch Ba(OH)2, thu được dung dịch X. Nhỏ rất từ từ dung dịch H2SO4 0,5M vào dung dịch X và lắc nhẹ để các phản ứng xảy ra hoàn toàn. Đồ thị biểu diễn sự phụ thuộc tổng khối lượng kết tủa (m gam) theo thể tích dung dịch H2SO4 (V ml) như sau: Giá trị của a là A. 8,10 B. 4,05. C. 5,40. D. 6,75.
Đọc tiếp
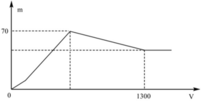
Hòa tan hoàn toàn a gam Al trong dung dịch Ba(OH)2, thu được dung dịch X. Nhỏ rất từ từ dung dịch H2SO4 0,5M vào dung dịch X và lắc nhẹ để các phản ứng xảy ra hoàn toàn. Đồ thị biểu diễn sự phụ thuộc tổng khối lượng kết tủa (m gam) theo thể tích dung dịch H2SO4 (V ml) như sau:
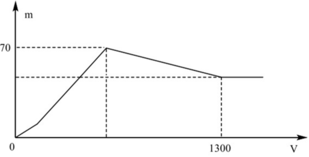
Giá trị của a là
A. 8,10
B. 4,05.
C. 5,40.
D. 6,75.
Đáp án A
Giả sử số mol ban đầu: nAl = x mol, nBa(OH)2 = y mol
2Al + Ba(OH)2 + 2H2O→ Ba(AlO2)2 + 3H2
x 0,5x 0,5x
Dung dịch X: Ba(AlO2)2 (0,5x mol) và Ba(OH)2 dư (y-0,5x mol)
+ Khi kết tủa lớn nhất: m↓ = mAl(OH)3 max + mBaSO4 max = 78x + 233y = 70 (1)
+ Khi V= 1300 ml: Al(OH)3 vừa bị hòa tan hết. Khi đó ta có:
OH- + H+ → H2O
H+ + AlO2- + H2O → Al(OH)3
3H+ + Al(OH)3 → Al3+ + 3H2O
nH+ = nOH- dư + nAlO2- + 3 nAl(OH)3 max => 2.1,3.0,5 = 2y – x + x + 3x <=> 3x + 2y = 1,3 (2)
Giải (1) và (2): x = 0,3; y = 0,2
=> a = 0,3.27 = 8,1 gam
Đúng 0
Bình luận (0)

















