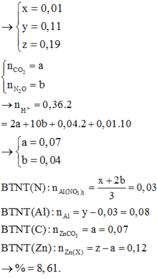Cho khí CO2(đktc) phản ứng với 80g dung dịch NaOH 25% tạo thành hỗn hợp muối và muối trung hòa theo tỉ lệ số mol là 2:3. Vậy thể tích CO2 cần dùng là bao nhiêu?

Những câu hỏi liên quan
Tính thể tích khí SO2 (đktc) cần thiết để khi tác dụng với 16 gam dung dịch NaOH 10% thì tạo thành dung dịch chứa hỗn hợp muối axit và muối trung hòa theo tỉ lệ mol là 2 : 3?
Đọc tiếp
Tính thể tích khí SO2 (đktc) cần thiết để khi tác dụng với 16 gam dung dịch NaOH 10% thì tạo thành dung dịch chứa hỗn hợp muối axit và muối trung hòa theo tỉ lệ mol là 2 : 3?
\(n_{NaOH}=\dfrac{16.10\%}{40}=0,04\left(mol\right)\\ 2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\\ NaOH+SO_2\rightarrow NaHSO_3\\ Đặt:n_{NaHSO_3}=a\left(mol\right);n_{Na_2SO_3}=1,5a\left(mol\right)\\ \Rightarrow n_{NaOH\left(tổng\right)}=3a+a=4a=0,04\left(mol\right)\\ \Leftrightarrow a=0,01\left(mol\right)\\ n_{SO_2\left(tổng\right)}=n_{Na_2SO_3}+n_{NaHSO_3}=2,5a=0,025\left(mol\right)\\ V_{SO_2\left(đktc\right)}=0,025.22,4=0,56\left(lít\right)\)
Đúng 0
Bình luận (0)
Tính thể tích CO2 cần thiết để khi tác dụng với 16 gam dung dịch NaOH 10% tạo thành
a/ Muối trung hoà
b/ Muối axit
c/ Hỗn hợp muối axit và muối trung hoà theo tỉ lệ số mol là 2:3
Cho hỗn hợp A gồm (CO, CO2, SO2) có tỉ khối vs H2là 20,5 . Biết số mol của SO2=số mol của CO2.Tính thành phần % theo thể tích của từng khí trong hỗn hợp
B tính thể tích dung dịch NaOH 1M ơ trong 2,24 lít hỗn hợp khí A thành muối trung hòa điều kiện chuaanr
Xem chi tiết
a)
Gọi \(n_{SO_2} = n_{CO_2} = a(mol)\\ n_{CO} = b(mol)\)
Ta có :
\(M_A = \dfrac{m_{CO}+m_{CO_2} + m_{SO_2}}{n_{CO} + n_{CO_2} + n_{SO_2}}\)
⇔ \(\dfrac{28b+ 44a + 64a}{b + a + a} = 20,5.2\)
⇔ 108a + 28b = 41b + 82a
⇔ 26a = 13b
⇔ \(\dfrac{a}{b} = \dfrac{13}{26} = \dfrac{1}{2}\)
Suy ra : Nếu thể tích khí A được chia làm 4 phần thì CO chiếm 2 phần , CO2 và SO2 chiếm 1 phần
\(\%V_{CO_2} = \%V_{SO_2} = \dfrac{1}{4}.100\% = 25\%\\ \%V_{SO_2} = \dfrac{2}{4}.100\% = 50\%\)
b)
Ta có :
\(n_{CO_2} + n_{SO_2} = n_A.50\% = \dfrac{2,24}{22,4}.50\% = 0,05(mol)\)
\(2NaOH + CO_2 \to Na_2CO_3 + H_2O\\ 2NaOH + SO_2 \to Na_2SO_3 + H_2O\)
Theo PTHH :
\(n_{NaOH} = 2(n_{SO_2} + n_{CO_2}) = 0,1(mol)\\ \Rightarrow V_{NaOH} = \dfrac{0,1}{1} = 0,1(lít)\)
Đúng 2
Bình luận (0)
Hỗn hợp T gồm hai este là đồng phân cấu tạo. Đốt cháy hoàn toàn m gam T cần dùng 8,96 gam O2, thu được 5,376 lít khí CO2 (đktc) và 4,32 gam H2O. Cho m gam T tác dụng hết với dung dịch NaOH (dùng dư 50% so với cần thiết), cô cạn dung dịch sau phản ứng thì thu được 7,74 gam chất rắn khan, trong đó có a mol muối Y và b mol muối Z
(
M
Y
M
Z
)
. Tỉ lệ a : b là A. 2 : 3 B. 4 : 3 C. 3 : 2 D. 3 : 5
Đọc tiếp
Hỗn hợp T gồm hai este là đồng phân cấu tạo. Đốt cháy hoàn toàn m gam T cần dùng 8,96 gam O2, thu được 5,376 lít khí CO2 (đktc) và 4,32 gam H2O. Cho m gam T tác dụng hết với dung dịch NaOH (dùng dư 50% so với cần thiết), cô cạn dung dịch sau phản ứng thì thu được 7,74 gam chất rắn khan, trong đó có a mol muối Y và b mol muối Z ( M Y < M Z ) . Tỉ lệ a : b là
A. 2 : 3
B. 4 : 3
C. 3 : 2
D. 3 : 5
Chọn đáp án D
♦ giải đốt m g a m T + 0 , 28 m o l O 2 → t 0 0 , 24 m o l C O 2 + 0 , 24 m o l H 2 O
tương quan n C O 2 = n H 2 O
⇒ T là hỗn hợp 2 este no, đơn chức, mạch hở dạng CnH2nO2
⇒ bảo toàn nguyên tố O có
nT = 1 2 .nO trong T
= (0,24 × 3 – 0,28 × 2) ÷ 2
= 0,08 mol.
⇒ n = 0,24 ÷ 0,08 = 3
⇒ T gồm 2 este đồng phân là HCOOC2H5 và CH3COOCH3.
Thủy phân m gam T (0,08 mol) cần 0,08 mol NaOH
⇒ dư 50% so với lượng cần là 0,04 mol
⇒ 7,74 gam chất rắn khan gồm 0,04 mol NaOH dư + a mol HCOONa (muối Y) + b mol CH3COONa (muối Z).
⇒ 68a + 82b = 7,74 – 0,04 × 40
= 6,14 gam.
Lại có a + b = nT = 0,08 mol
⇒ giải hệ ra a = 0,03 mol
và b = 0,05 mol
⇒ a : b = 3 : 5
Đúng 0
Bình luận (0)
1.Khối lượng dung dịch NaOH 25% cần dùng để hấp thụ 4,48 lít khí CO2 ở đktc tạo ra muối axit có khối lượng bao nhiêu ?
2. Đốt hỗn hợp gồm Cu và Ag trong khí oxi dư, phản ứng xong thu được chất rắn A. Cho chất rắn A tan trong dung dịch HCl dư, phản ứng xong thu được chất rắn B. Chất rắn B là gì ?
1) muối axit là NaHCO3
CO2 + NaOH → NaHCO3
nCO2 = 4,48/22,4 = 0,2 mol => nNaOH = 0,2 mol ,mNaOH =0,2.40 = 8 gam
C% =\(\dfrac{m_{ct}}{m_{dd}}\).100 => mdd NaOH = \(\dfrac{8.100}{25}\) = 32gam
2) Ag không bị oxi hóa bởi oxi ở nhiệt độ cao,đồng thì có nên hỗn hợp chất rắn A thu được gồm CuO và Ag
2Cu + O2 --> 2CuO
Cho A + HCl dư thì Ag cũng không phản ứng
CuO + HCl --> CuCl2 + H2O
=> Chất rắn B còn lại là Ag
Đúng 1
Bình luận (0)
1) muối axit là NaHCO3
CO2 + NaOH → NaHCO3
nCO2 = 4,48/22,4 = 0,2 mol => nNaOH = 0,2 mol ,mNaOH =0,2.40 = 8 gam
C% =8.100258.10025 = 32gam
2) Ag không bị oxi hóa bởi oxi ở nhiệt độ cao,đồng thì có nên hỗn hợp chất rắn A thu được gồm CuO và Ag
2Cu + O2 --> 2CuO
Cho A + HCl dư thì Ag cũng không phản ứng
CuO + HCl --> CuCl2 + H2O
=> Chất rắn B còn lại là Ag
Đúng 0
Bình luận (0)
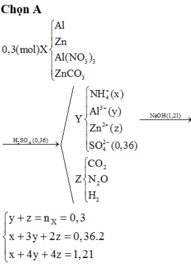
Hòa tan hết 0,3 mol hỗn hợp X gồm Al, Zn, Al(NO3)3, ZnCO3 trong dung dịch chứa 0,36 mol H2SO4 loãng, kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối trung hòa và 3,36 lít (đktc) hỗn hợp khí Z gồm CO2, N2O, H2. Tỉ khối của Z so với He bằng 8,2. Cho dung dịch NaOH dư vào Y, thấy lượng NaOH phản ứng là 48,4 gam. Phần trăm khối lượng của Al đơn chất trong hỗn hợp X là A. 8,6% B. 5,4% C. 9,7% D. 6,5%
Đọc tiếp
Hòa tan hết 0,3 mol hỗn hợp X gồm Al, Zn, Al(NO3)3, ZnCO3 trong dung dịch chứa 0,36 mol H2SO4 loãng, kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối trung hòa và 3,36 lít (đktc) hỗn hợp khí Z gồm CO2, N2O, H2. Tỉ khối của Z so với He bằng 8,2. Cho dung dịch NaOH dư vào Y, thấy lượng NaOH phản ứng là 48,4 gam. Phần trăm khối lượng của Al đơn chất trong hỗn hợp X là
A. 8,6%
B. 5,4%
C. 9,7%
D. 6,5%
Đáp án A
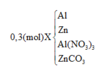
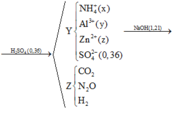
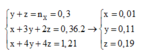
n C O 2 = a n N 2 O = b → a = 0 , 07 b = 0 , 04
B T N T ( N ) : n A l ( N O 3 ) 3 = x + 2 b 3 = 0 , 03
![]()
B T N T ( C ) : n Z n C O 3 = a = 0 , 07
B T N T ( Z n ) : n Z n ( X ) = z - a = 0 , 12
⇒ % = 8 , 61
Đúng 0
Bình luận (0)
Hòa tan hết 0,3 mol hỗn hợp X gồm Al, Zn, Al(NO3)3, ZnCO3 trong dung dịch chứa 0,36 mol H2SO4 loãng, kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối trung hòa và 3,36 lít (đktc) hỗn hợp khí Z gồm CO2, N2O, H2. Tỉ khối của Z so với He bằng 8,2. Cho dung dịch NaOH dư vào Y, thấy lượng NaOH phản ứng là 48,4 gam. Phần trăm khối lượng của Al đơn chất trong hỗn hợp X là A. 8,6% B. 5,4% C. 6,5% D. 9,7%
Đọc tiếp
Hòa tan hết 0,3 mol hỗn hợp X gồm Al, Zn, Al(NO3)3, ZnCO3 trong dung dịch chứa 0,36 mol H2SO4 loãng, kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối trung hòa và 3,36 lít (đktc) hỗn hợp khí Z gồm CO2, N2O, H2. Tỉ khối của Z so với He bằng 8,2. Cho dung dịch NaOH dư vào Y, thấy lượng NaOH phản ứng là 48,4 gam. Phần trăm khối lượng của Al đơn chất trong hỗn hợp X là
A. 8,6%
B. 5,4%
C. 6,5%
D. 9,7%
Hòa tan hết 0,3 mol hỗn hợp X gồm Al, Zn, Al(NO3)3, ZnCO3 trong dung dịch chứa 0,36 mol H2SO4 loãng, kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối trung hòa và 3,36 lít (đktc) hỗn hợp khí Z gồm CO2, N2O, H2. Tỉ khối của Z so với He bằng 8,2. Cho dung dịch NaOH dư vào Y, thấy lượng NaOH phản ứng là 48,4 gam. Phần trăm khối lượng của Al đơn chất trong hỗn hợp X là A. 8,6% B. 5,4% C. 9,7% D. 6,5%
Đọc tiếp
Hòa tan hết 0,3 mol hỗn hợp X gồm Al, Zn, Al(NO3)3, ZnCO3 trong dung dịch chứa 0,36 mol H2SO4 loãng, kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối trung hòa và 3,36 lít (đktc) hỗn hợp khí Z gồm CO2, N2O, H2. Tỉ khối của Z so với He bằng 8,2. Cho dung dịch NaOH dư vào Y, thấy lượng NaOH phản ứng là 48,4 gam. Phần trăm khối lượng của Al đơn chất trong hỗn hợp X là
A. 8,6%
B. 5,4%
C. 9,7%
D. 6,5%
Đáp án A
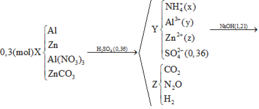
y + z = n X = 0 , 3 x + 3 y + 2 z = 0 , 36 . 2 x + 4 y + 4 z = 1 , 21 → x = 0 , 01 y = 0 , 11 z = 0 , 19
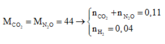
M C O 2 = M N 2 O = 44 → n C O 2 + n N 2 O = 0 , 11 n H 2 = 0 , 04
n C O 2 = a n N 2 O = b → n H + = 0 , 36 . 2 = 2 a + 10 b + 0 , 04 . 2 + 0 , 01 . 10
→ a = 0 , 07 b = 0 , 04
BTNT(N): n A l ( N O 3 ) 3 = x + 2 b 3 = 0 , 03
BTNT(Al): n A l = y - 0 , 03 = 0 , 08
BTNT(C): n Z n C O 3 = a = 0 , 07
BTNT(Zn): n Z n ( X ) = z - a = 0 , 12
=> %=8,61
Đúng 0
Bình luận (0)
Hòa tan hết 0,3 mol hỗn hợp X gồm Al, Zn, Al(NO3)3, ZnCO3 trong dung dịch chứa 0,36 mol H2SO4 loãng, kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối trung hòa và 3,36 lít (đktc) hỗn hợp khí Z gồm CO2, N2O, H2. Tỉ khối của Z so với He bằng 8,2. Cho dung dịch NaOH dư vào Y, thấy lượng NaOH phản ứng là 48,4 gam. Phần trăm khối lượng của Al đơn chất trong hỗn hợp X là A. 8,6% B. 5,4% C. 9,7% D. 6,5%
Đọc tiếp
Hòa tan hết 0,3 mol hỗn hợp X gồm Al, Zn, Al(NO3)3, ZnCO3 trong dung dịch chứa 0,36 mol H2SO4 loãng, kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối trung hòa và 3,36 lít (đktc) hỗn hợp khí Z gồm CO2, N2O, H2. Tỉ khối của Z so với He bằng 8,2. Cho dung dịch NaOH dư vào Y, thấy lượng NaOH phản ứng là 48,4 gam. Phần trăm khối lượng của Al đơn chất trong hỗn hợp X là
A. 8,6%
B. 5,4%
C. 9,7%
D. 6,5%
Đáp án A
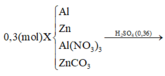
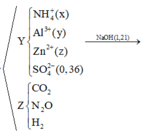
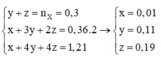
![]()
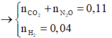
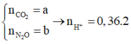
![]()
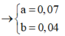
BTNT(N): 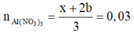
BTNT(Al): ![]()
BTNT(C): ![]()
BTNT(Zn): ![]()
=> % = 8,61
Đúng 0
Bình luận (0)