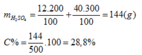trộn 200 gam dung dịch h2so4 19,6% với 150 gam dung dịch h2so4 9,8% thì thu được dung dịch A tính c% của dung dịch A thu được

Những câu hỏi liên quan
Bài 10: Hòa tan hoàn tòa 10,8 gam nhôm trong 200 gam dung dịch H2SO4 thì vừa đủ. Khi phản ứng kết thúc hãy tính:a. Thể tích H2 thu được ở đktc.b. C% dung dịch axit đã dùng.Bài 17: Trộn lẫn 150 gam dung dịch BaCl2 5,2% với 250gam dung dịch H2SO4 19,6%. Sau phản ứng được dung dịch A.a. Tính khối lượng kết tủa thu được sau phản ứng?b. Xác định chất tan có trong dung dịch A. Tính khối lượng chất tan đó?
Đọc tiếp
Bài 10: Hòa tan hoàn tòa 10,8 gam nhôm trong 200 gam dung dịch H2SO4 thì vừa đủ. Khi phản ứng kết thúc hãy tính:
a. Thể tích H2 thu được ở đktc.
b. C% dung dịch axit đã dùng.
Bài 17: Trộn lẫn 150 gam dung dịch BaCl2 5,2% với 250gam dung dịch H2SO4 19,6%. Sau phản ứng được dung dịch A.
a. Tính khối lượng kết tủa thu được sau phản ứng?
b. Xác định chất tan có trong dung dịch A. Tính khối lượng chất tan đó?
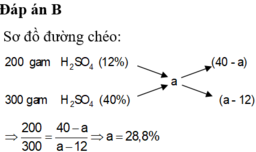
Trộn 200 gam dung dịch H2SO4 12% với 300 gam dung dịch H2SO4 40% thu được 500 gam dung dịch H2SO4 a%. Giá trị của a là:
A. 20,8%.
B. 28,8%.
C. 25,8%.
D. 30,8%.
Trộn 200 gam dung dịch H2SO4 12% với 300 gam dung dịch H2SO4 40% thu được 500 gam dung dịch H2SO4 a%. Gía trị của a là: A. 20,8% B. 28,8% C. 25,8% D. 30,8%
Đọc tiếp
Trộn 200 gam dung dịch H2SO4 12% với 300 gam dung dịch H2SO4 40% thu được 500 gam dung dịch H2SO4 a%. Gía trị của a là:
A. 20,8%
B. 28,8%
C. 25,8%
D. 30,8%
Trộn 200 gam dung dịch BaCl2 2,08% với 300 gam dung dịch H2SO4 9,8% được a gam kết tủa và dung dịch X. Viết PTPU, tính a? tính C% mỗi chất trong dung dịch X?
a, \(BaCl_2+H_2SO_4\rightarrow2HCl+BaSO_{4\downarrow}\)
b, \(m_{BaCl_2}=200.2,08\%=4,16\left(g\right)\Rightarrow n_{BaCl_2}=\dfrac{4,16}{208}=0,02\left(mol\right)\)
\(m_{H_2SO_4}=300.9,8\%=29,4\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,02}{1}< \dfrac{0,3}{1}\), ta được H2SO4 dư.
Theo PT: \(\left\{{}\begin{matrix}n_{BaSO_4}=n_{H_2SO_4\left(pư\right)}=n_{BaCl_2}=0,02\left(mol\right)\\n_{HCl}=2n_{BaCl_2}=0,04\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=0,3-0,02=0,28\left(mol\right)\)
Ta có: m dd sau pư = m dd BaCl2 + m dd H2SO4 - mBaSO4 = 200 + 300 - 0,02.233 = 495,34 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{HCl}=\dfrac{0,04.36,5}{495,34}.100\%\approx0,295\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{0,28.98}{495,34}.100\%\approx5,54\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Trộn 300 gam dung dịch H2SO4 9,8% với 200 gam dung dịch BaCl2 26%, thu được a gam kết tủa và dung dịch X.
a) Viết phương trình hóa học của phản ứng xảy ra. Tính a.
b) Xác định nồng độ phần trăm các chất trong dung dịch X.
Giúp mh đi mn.
\(a,PTHH:H_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2HCl\\ \left\{{}\begin{matrix}m_{H_2SO_4}=\dfrac{300\cdot9,8\%}{100\%}=29,4\left(g\right)\\m_{BaCl_2}=\dfrac{200\cdot26\%}{100\%}=52\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{H_2SO_4}=\dfrac{29,4}{98}=0,3\left(mol\right)\\n_{BaCl_2}=\dfrac{52}{208}=0,25\left(mol\right)\end{matrix}\right.\)
Vì \(\dfrac{n_{H_2SO_4}}{1}>\dfrac{n_{BaCl_2}}{1}\) nên H2SO4 dư
\(\Rightarrow n_{BaSO_4}=n_{BaCl_2}=0,25\left(mol\right)\\ \Rightarrow a=m_{BaSO_4}=0,25\cdot233=58,25\left(g\right)\\ b,n_{HCl}=n_{BaCl_2}=0,25\left(mol\right)\\ \Rightarrow m_{CT_{HCl}}=0,25\cdot36,5=9,125\left(g\right)\\ m_{dd_{HCl}}=300+200-58,25=441,75\left(g\right)\\ \Rightarrow C\%_{HCl}=\dfrac{9,125}{441,75}\cdot100\%\approx2,07\%\)
Đúng 4
Bình luận (0)
Bài 17: Trộn lẫn 150 gam dung dịch BaCl2 5,2% với 250gam dung dịch H2SO4 19,6%. Sau phản ứng được dung dịch A.a. Tính khối lượng kết tủa thu được sau phản ứng?b. Xác định chất tan có trong dung dịch A. Tính khối lượng chất tan đó? Bài 18: Cho m gam kẽm tác dụng với 250 gam dd axit HCl 7,3%.a. Tính thể tích khí hiđro thu được ở đktc.b. Xác định chất tan có trong dung dịch sau phản ứng. Tính khối lượng chất tan đó? Bài 19: Người ta cho 10,8 gam nhôm vào cốc đựng 300ml dung dịch H2SO4 3M. Sau phản...
Đọc tiếp
Bài 17: Trộn lẫn 150 gam dung dịch BaCl2 5,2% với 250gam dung dịch H2SO4 19,6%. Sau phản ứng được dung dịch A.
a. Tính khối lượng kết tủa thu được sau phản ứng?
b. Xác định chất tan có trong dung dịch A. Tính khối lượng chất tan đó?
Bài 18: Cho m gam kẽm tác dụng với 250 gam dd axit HCl 7,3%.
a. Tính thể tích khí hiđro thu được ở đktc.
b. Xác định chất tan có trong dung dịch sau phản ứng. Tính khối lượng chất tan đó?
Bài 19: Người ta cho 10,8 gam nhôm vào cốc đựng 300ml dung dịch H2SO4 3M. Sau phản ứng thu được dung dịch X.
a. Tính thể tích khí hiđro thu được ở đktc.
b. Xác định chất tan có trong dung dịch X. Tính khối lượng chất tan đó?
Bài 19 :
\(a) n_{Al} = \dfrac{10,8}{27} = 0,4(mol)\\ 2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\\ n_{H_2} = \dfrac{3}{2}n_{Al} = 0,6(mol)\\ V_{H_2} = 0,6.22,4 = 13,44(lít)\\ b) \text{Chất tan : }Al_2(SO_4)_3\\ n_{Al_2(SO_4)_3} = \dfrac{1}{2}n_{Al} = 0,2(mol)\\ m_{Al_2(SO_4)_3} = 0,2.342 = 68,4(gam)\)
Đúng 1
Bình luận (0)
Bài 18 :
\(a) n_{HCl} = \dfrac{250.7,3\%}{36,5 } = 0,5(mol)\\ Zn + 2HCl \to ZnCl_2 + H_2\\ n_{H_2} = \dfrac{1}{2}n_{HCl} = 0,25(mol) \Rightarrow V_{H_2} = 0,25.22,4 = 5,6(lít)\\ b) \text{Chất tan : } ZnCl_2\\ n_{ZnCl_2} = n_{H_2} = 0,25(mol)\\ m_{ZnCl_2} = 0,25.136 = 34(gam)\)
Đúng 1
Bình luận (0)
Trộn 200g dung dịch H2SO4 9,8% với 300g dung dịch H2SO4 19,6% thu được dung dịch X
a) tính C% dung dịch X
b) Tính V dung dịch KOH 1M cần để trung hòa dung dịch X
Với 200g dd H2SO4 9.8% ==> mH2SO4 = 200x9.8/100 = 19.6 (g)
Với 300g dd H2SO4 19.6% => mH2SO4 = 300x19.6/100 = 58.8 (g)
mdd H2SO4 = 200 + 300 = 500 (g)
C% X = (19.6+58.8)x100/500 = 15.68%
mH2SO4 = 19.6 + 58.8 = 78.4 (g)
===> nH2SO4 = m/M = 78.4/98 = 0.8 (mol)
H2SO4 + 2KOH => K2SO4 + 2H2O
==> nKOH = 0.8 x 2 = 1.6 (mol)
V = n/CM = 1.6/1 = 1.6 (l) = 1600ml
Đúng 0
Bình luận (0)
Hòa tan hoàn tàn CuO với 200 gam dung dịch H2SO4 19,6% thu được dung dịch A. Cho toàn bộ lượng A phản ứng với dung dịch NaOH thu được 29,4 gam kết tủa và dung dịch B. Tính nồng độ phần trăm chất tan có trong dung dịch B
\(n_{H_2SO_4}=\dfrac{200.19,6}{100.98}=0,4mol\\ CuO+H_2SO_4\rightarrow CuSO_4+H_2O\\ n_{CuSO_4\left(A\right)}=n_{CuO}=n_{H_2SO_4}=0,4mol\\ n_{Cu\left(OH\right)_2}=\dfrac{29,4}{98}=0,3mol\\ CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\\\Rightarrow\dfrac{0,4}{1}>\dfrac{0,3}{1}\Rightarrow CuSO_4.pư.không.hết\)
\(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
0,3mol 0,6mol 0,3mol
\(m_{ddB}=0,4.80+200+0,6.40-29,4=226,6g\\ C_{\%Na_2SO_4\left(B\right)}=\dfrac{0,3.142}{226,6}\cdot100=18,8\%\)
Đúng 3
Bình luận (5)
Trộn 100 gam dung dịch H2SO4 19,6% với 300 gam dung dịch BaCl2 20,8% thu được m gam kết tủa
và dung dịch Y.
1.Viết phương trình phản ứng? Tính m?
2.Tính nồng độ % của mỗi chất trong dung dịch Y?
\(\begin{cases} m_{H_2SO_4}=\dfrac{100.19,6\%}{100\%}=19,6(g)\\ m_{BaCl_2}=\dfrac{300.20,8\%}{100\%}=62,4(g) \end{cases} \Rightarrow \begin{cases} n_{H_2SO_4}=\dfrac{19,6}{98}=0,2(mol)\\ n_{BaCl_2}=\dfrac{62,4}{208}=0,3(mol) \end{cases}\\ a,PTHH:BaCl_2+H_2SO_4\to BaSO_4\downarrow +2HCl\)
Vì \(\dfrac{n_{H_2SO_4}}{1}<\dfrac{n_{BaCl_2}}{1}\) nên \(BaCl_2\) dư
\(\Rightarrow n_{BaSO_4}=0,2(mol)\\ \Rightarrow m_{BaSO_4}=0,2.233=46,6(g)\)
\(b,n_{HCl}=n_{BaSO_4}=0,2(mol)\\ \Rightarrow m_{CT_{HCl}}=0,2.36,5=7,3(g)\\ m_{dd_{HCl}}=100+300-46,6=353,4(g)\\ \Rightarrow C\%_{HCl}=\dfrac{7,3}{353,4}.100\%\approx 2,07\%\)
Đúng 1
Bình luận (0)