đốt 16l hỗn hợp X gồm COvà CO2 trong khí O2 dư nhận thấy thể tích chung của hỗn hợp giảm 2l
a) tính % thể tích các chất khí trong hỗn hợp X
b) để hỗn hợp hai khí CO và CO2 có khối lượng bằng nhau cần lấy chúng vóiư tỉ lệ thể tích như thế nào
1. Một hỗn hợp khí (X) gồm CO, CO2 và đơn chất (A). Biết % vể thể tích từng khí trong hỗn hợp khí (X) gồm CO, CO2 và đơn chất (A) tương ứng là 40%, 30% và 30%. Trong hỗn hợp khí CO2 chiếm 52,8% về khối lượng hỗn hợp khí (X).
a. Tìm công thức hóa học của khí (A). Các khí đo trong cùng điều kiện nhiệt độ và áp suất.
b. Có thể thu khí (A) vào bình (từ những thí nghiệm trong phòng thí nghiệm) bằng cách đặt bình thế nào (đứng bình,…)? Vì sao?
Nung m gam hỗn hợp X gồm KClO3 và KMnO4, thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là:
A. 8,77.
B. 8,53.
C. 8,70.
D. 8,91.
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là
A. 8,70.
B. 8,77.
C. 8,91.
D. 8,53.
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là
A. 8,77
B. 8,53
C. 8,70
D. 8,91
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là
A. 8,77.
B. 8,53.
C. 8,91.
D. 8,70.
Đáp án : A
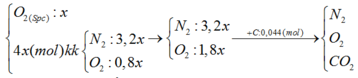
C + O2 à CO2 ( số mol khí trước và sau phản ứng không đổi)
=> nCO2 = nC = 0,044 = 5x.22% => x = 0,04 mol
m = mY + mO2 = mKCl. 100 19 , 893 + 32.0,04 = 8,77g
Nung hỗn hợp X gồm KClO3 và KMnO4, thu được hỗn hợp chất rắn Y và O2. Trong Y có 1,49 gam KCl chiếm 17,028% theo khối lượng. Lượng O2 ở trên đốt cháy hết 0,24 gam cacbon, sau phản ứng thu được hỗn hợp khí T gồm CO2 và O2 dư (CO2 chiếm 40% thể tích). Biết KClO3 bị nhiệt phân hoàn toàn, còn KMnO4 chỉ bị nhiệt phân một phần. Tính hiệu suất của phản ứng nhiệt phân KMnO4.
PT: \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\) (1)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\) (2)
\(C+O_2\underrightarrow{t^o}CO_2\) (3)
Ta có: \(n_{KCl}=\dfrac{1,49}{74,5}=0,02\left(mol\right)\)
\(n_C=\dfrac{0,24}{12}=0,02\left(mol\right)\)
\(m_Y=\dfrac{1,49}{17,028\%}=8,75\left(g\right)\), Y gồm: KCl, KMnO4 (dư), K2MnO4, MnO2.
Theo PT (3): \(n_{CO_2}=n_{O_2\left(pư\right)}=n_C=0,02\left(mol\right)\)
\(\Rightarrow n_{O_2\left(dư\right)}=\dfrac{0,02}{40\%}-0,02=0,03\left(mol\right)\)
⇒ ΣnO2 = 0,02 + 0,03 = 0,05 (mol)
Theo PT (1): \(n_{O_2\left(1\right)}=\dfrac{3}{2}n_{KCl}=0,03\left(mol\right)\)
\(\Rightarrow n_{O_2\left(2\right)}=0,05-n_{O_2\left(1\right)}=0,02\left(mol\right)\)
Theo PT (2): \(n_{K_2MnO_4}=n_{MnO_2}=n_{O_2\left(2\right)}=0,02\left(mol\right)\)
\(n_{KMnO_4\left(pư\right)}=2n_{O_2}=0,04\left(mol\right)\)
Mà: mKCl + mKMnO4 (dư) + mK2MnO4 + mMnO2 = 8,75
⇒ mKMnO4 (dư) = 1,58 (g) \(\Rightarrow n_{KMnO_4\left(dư\right)}=\dfrac{1,58}{158}=0,01\left(mol\right)\)
\(\Rightarrow H\%=\dfrac{0,04}{0,04+0,01}.100\%=80\%\)
Một hỗn hợp khí A gồm CO , CO2. Trộn A với không khí theo tỉ lệ thể tích 1:4, sau khi đốt cháy hết khí CO thì hàm lượng phần trăm (%) thể tịch của N2 trong hỗn hợp mới thu được tăng 3,36% so với hỗn hợp trước phản ứng. Tính % thể tích của hai khí trong hỗn hợp A.Giả thiết không khí chỉ có N2,O2 trong đó O2 chiếm 1/5 thể tích không khí.
Gọi thể tích của CO và CO2 trong hh A là x và y lít
=> thể tích không khí trộn với A là: 4(x+y)
Tổng thể tích của hh trộn: V = 5(x+y)
trong đó: V O2 = 4(x+y)/5 và V N2 = 16(x+y)/5
Ban đầu thì
%V N2 = 16(x+y)/5 : 5(x+y) = 64%
Phản ứng đốt:
2CO + O2 → 2CO2
x x/2 x
Tổng thể tích hh sau khi đốt = V CO2 (có sẵn và sinh ra từ pư) + V O2 còn lại + V N2 (không đổi)
V' = x+y + 16(x+y)/5 + 4(x+y)/5 - x/2 = 5(x+y) - x/2
%V N2 sau pư = 16(x+y)/5 : [5(x+y) - x/2] = 64% + 3,36% = 67,36 %
=> 16(x+y) = 0,6736 . [25(x+y) -5x/2]
<=> 0,84(x+y) = 1,684 x
=> x/(x+y) = 0,084/1,684 ≈ 49,88%
=> %V CO = %V CO2 = 50%
Cho e hỏi là bài này ở phần đầu lớp 9 ạ? Vì e thấy bài này ở đề thi học sinh giỏi huyện a lớp 8
Bài 9: Một hỗn hợp A gồm 2 khí CH4 và CO2 có thể thích bằng 8,96 lít và có khối lượng bằng 9,2 gam
a. Tính khối lượng và thể tích mỗi khí trong hỗn hợp A
b. Tính tỉ khối của hỗn hợp A so với khí O2
a. Gọi x, y lần lượt là số mol của CH4 và CO2
Ta có: \(n_A=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Theo đề, ta có:
- x + y = 0,4 (1)
- 16x + 44y = 9,2 (2)
Từ (1) và (2), ta có HPT:
\(\left\{{}\begin{matrix}x+y=0,4\\16x+44y=9,2\end{matrix}\right.\)
Giải ra, ta được:
x = 0,3, y = 0,1
=> \(m_{CH_4}=0,3.16=4,8\left(g\right);m_{CO_2}=0,1.44=4,4\left(g\right)\)
b. Ta có: \(\overline{M_A}=\dfrac{4,8+4,4}{0,3+0,1}=23\left(g\right)\)
=> \(d_{\dfrac{A}{O_2}}=\dfrac{\overline{M_A}}{M_{O_2}}=\dfrac{23}{32}=0,71875\left(lần\right)\)
đốt cháy 10,35 g hỗn hợp X gồm Mg và Al trong khí oxi dư thấy có 5,88 l O2 phản ứng thể tích khí đo ở điều kiện tiêu chuẩn . Tính khối lượng mỗi chất có trong hỗn hợp X
Gọi $n_{Mg} = a(mol) ; n_{Al} = b(mol) \Rightarrow 24a + 27b = 10,35(1)$
$2Mg + O_2 \xrightarrow{t^o} 2MgO$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$n_{O_2} = \dfrac{1}{2}a + \dfrac{3}{4}b = \dfrac{5,88}{22,4} = 0,2625(2)$
Từ (1)(2) suy ra a = 0,15 ; b = 0,25
$m_{Mg} = 0,15.24 = 3,6(gam)$
$m_{Al} = 0,25.27 = 6,75(gam)$