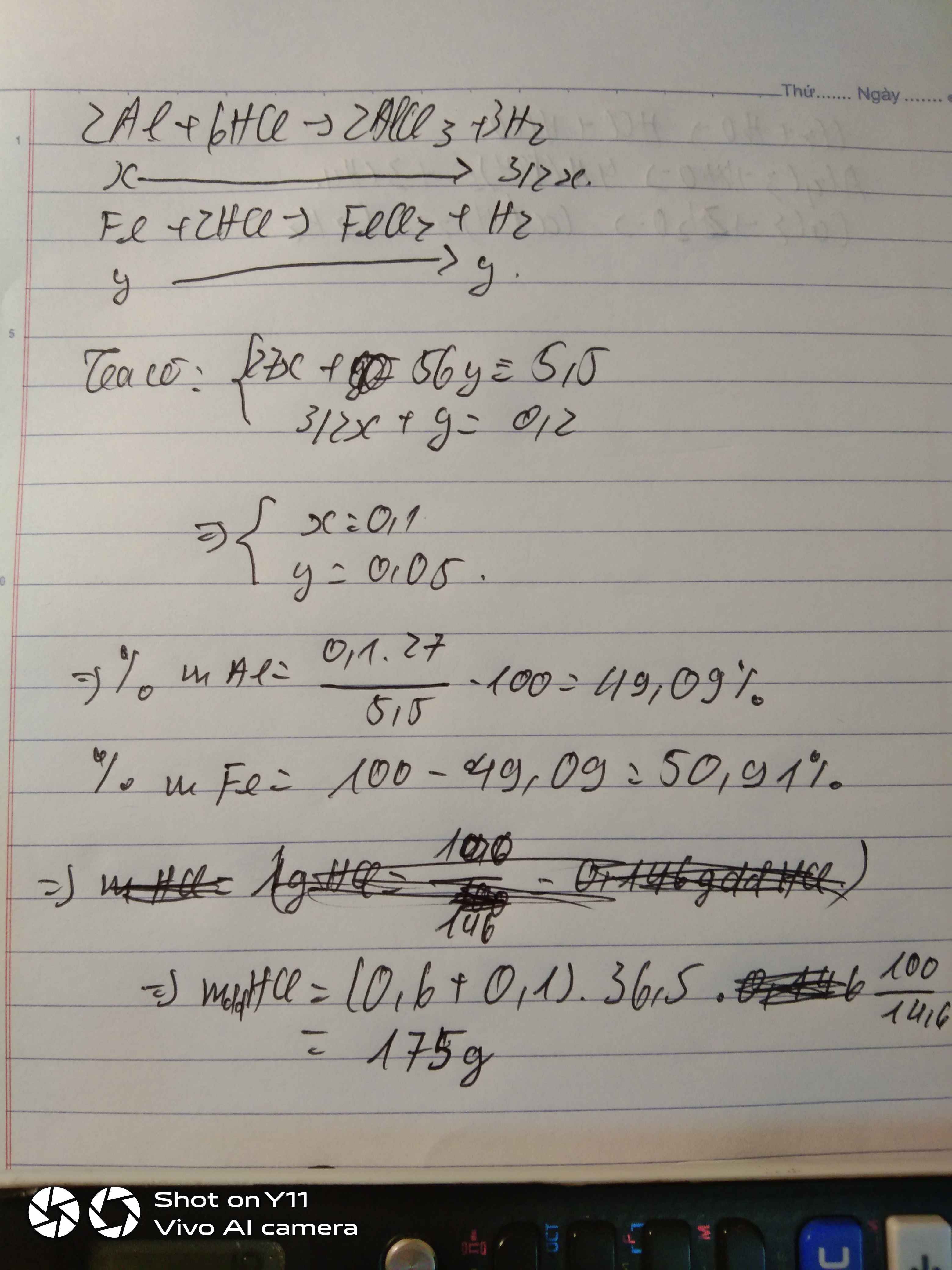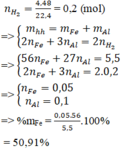hòa tan hoàn toàn 27,2g hỗn hợp Fe,Fe2O3 bằng dung dịch h2so4 24,5% (d=1,2g/ml) thu được 4,48 lít khí tính phần trăm khối lượng mỗi chất

Những câu hỏi liên quan
Hòa tan hoàn toàn 20 g hỗn hợp Zn ,FeO bằng dung dịch H2SO4 loãng, dư. Phản ứng kết thúc thu được 4,48 lít khí h2 ở điều kiện tiêu chuẩn. Tính thành phần trăm theo khối lượng của mỗi chất có trong hỗn hợp ban đầu
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\\ Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ FeO+H_2SO_4\rightarrow FeSO_4+H_2O\\ n_{Zn}=n_{H_2}=0,2mol\\ \%m_{Zn}=\dfrac{0,2.65}{20}\cdot100\%=65\%\\ \%m_{Fe}=100\%-65\%=35\%\)
Đúng 3
Bình luận (0)
1/. Hòa tan hoàn toàn 2,22 gam hỗn hợp A gồm ( Al ; Fe ) bằng dung dịch Axit H2SO4 dư . Sau pư thu được dung dịch B và có 1344 ml khí H2 ở ĐKTC bay ra .a. Tính phần trăm khối lượng mỗi chất có trong hỗn hợp X .b. Nếu cho dung dịch NaOH dư vào dung dịch B ở trên thì thu được kết tủa D . Nung D trong không khí đến khối lượng không đổi thì thu được m gam chất rắn E . Tính giá trị của m .
Đọc tiếp
1/. Hòa tan hoàn toàn 2,22 gam hỗn hợp A gồm ( Al ; Fe ) bằng dung dịch Axit H2SO4 dư . Sau pư thu được dung dịch B và có 1344 ml khí H2 ở ĐKTC bay ra .
a. Tính phần trăm khối lượng mỗi chất có trong hỗn hợp X .
b. Nếu cho dung dịch NaOH dư vào dung dịch B ở trên thì thu được kết tủa D . Nung D trong không khí đến khối lượng không đổi thì thu được m gam chất rắn E . Tính giá trị của m .
Bài 20. Hòa tan hoàn toàn 27,8 gam hỗn hợp X gồm Al và Fe vào 500 ml dung dịch H2SO4 loãng, vừa đủ thì thu được 17,353 lít khí thoát ra (ở đkc)
a. Tính thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp X
b. Tính nồng độ mol/lít của dung dịch H,SO, đã sử dụng.
a, Ta có: 27nAl + 56nFe = 27,8 (1)
PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{17,353}{24,79}=0,7\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,2\left(mol\right)\\n_{Fe}=0,4\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{27,8}.100\%\approx19,42\%\\\%m_{Fe}\approx80,58\%\end{matrix}\right.\)
b, \(n_{H_2SO_4}=n_{H_2}=0,7\left(mol\right)\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,7}{0,5}=1,4\left(M\right)\)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 24,4g hỗn hợp Fe và Fe2O3 vào 800ml dung dịch HCl 1,5M thu được dung dịch A và 3,36 lít khí (đktc).
a) Tính thành phần phần trăm theo khối lượng của mỗi chất trong hỗn hợp ban đầu.
b) Tính CM của các chất trong dung dịch A.
c) Để trung hòa dung dịch A cần dùng bao nhiêu ml dung dịch NaOH 1M?
mong mn giải giùm
nH2 = \(\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Fe + 2HCl ---> FeCl2 + H2
0,15 0,3 0,15 0,15
mFe = 0,15.56 = 8,4 (g)
mFe2O3 = 24,4 - 8,4 = 16 (g)
nFe2O3 = \(\dfrac{16}{160}=0,1\left(mol\right)\)
%mFe = \(\dfrac{8,4}{24,4}=34,42\%\)
%mFe2O3 = \(100\%-34,42\%=65,58\%\)
Fe2O3 + 6HCl ---> 2FeCl3 + 3H2O
0,1 0,6 0,2 0,3
nHCl (ban đầu) = 0,8.1,5 = 1,2 (mol)
nHCl (dư) = 1,2 - 0,3 - 0,6 = 0,3 (mol)
=> \(\left\{{}\begin{matrix}C_{MFeCl_3}=\dfrac{0,2+0,15}{0,8}=0,4375M\\C_{MHCl\left(dư\right)}=\dfrac{0,3}{0,8}=0,375M\end{matrix}\right.\)
PTHH:
FeCl3 + 3NaOH ---> Fe(OH)3 + 3NaCl
0,35 1,05
HCl + NaOH ---> NaCl + H2O
0,3 0,3
=> \(V_{ddNaOH}=\dfrac{1,05+0,3}{1}=1,35\left(l\right)=1350\left(ml\right)\)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 5,1 gam hỗn hợp gồm Mg và Al vào dung dịch HCl 7,3% (D=1,2g/ml) thì thu được 5,6l lít khí B (điều kiện tiêu chuẩn)
a) tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu
b) tính thể tích dung dịch HCl cần dùng
a) Đặt \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\) \(\Rightarrow24a+27b=5,1\) (1)
Ta có: \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Bảo toàn electron: \(2a+3b=0,5\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,1\cdot24}{5,1}\cdot100\%\approx47,06\%\\\%m_{Al}=52,94\%\end{matrix}\right.\)
b) Bảo toàn nguyên tố: \(n_{HCl}=2n_{H_2}=0,5\left(mol\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{0,5\cdot36,5}{7,3\%}=250\left(g\right)\)
\(\Rightarrow V_{HCl}=\dfrac{250}{1,2}\approx208,33\left(ml\right)\)
Đúng 1
Bình luận (0)
hòa tan hoàn toàn 5,5 gam hỗn hợp gồm Al, Fe bằng dung dịch HCl vừa đủ thu được 4,48 lít khí hidro dkc
a . tính phần trăm khối lượng mỗi kim loại trong hỗn hợp đồng
b. tính khối lượng dung dịch HCl cần dùng nếu cứ 100 gam dung dịch HCl có chứa 14,6 gam HCl nguyên chất
Gọi \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo pt: \(\Rightarrow\left\{{}\begin{matrix}3x+y=0,2\\27x+56y=5,5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=\dfrac{19}{470}\\y=\dfrac{37}{470}\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{\dfrac{19}{470}\cdot27}{5,5}\cdot100\%=19,84\%\)
\(\%m_{Fe}=100\%-19,84\%=80,16\%\)
Hòa tan hoàn toàn 49,6 gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 bằng H2SO4 đặc, nóng thu được dung dịch Y và 8,96 lít khí SO2 (đktc). Thành phần phần trăm về khối lượng của oxi trong hỗn hợp X và khối lượng muối trong dung dịch Y lần lượt là
Coi X gồm Fe và O.
Ta có: 56nFe + 16nO = 49,6 (1)
\(n_{SO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
BT e, có: 3nFe - 2nO = 2nSO2 = 0,8 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,7\left(mol\right)\\n_O=0,65\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m_O=\dfrac{0,65.16}{49,6}.100\%\approx20,97\%\)
Muối thu được là Fe2(SO4)3
BTNT Fe, có: \(n_{Fe_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Fe}=0,35\left(mol\right)\)
\(\Rightarrow m_{Fe_2\left(SO_4\right)_3}=0,35.400=140\left(g\right)\)
Đúng 4
Bình luận (0)
Hòa tan hoàn toàn 13,8 gam hỗn hợp A gồm hai kim loại Fe, Al vào 750 ml dung dịch HCl 1,6M (D = 1,1g/ml) thu được 10,08 lít khí (đktc) và dung dịch B.
Tính phần trăm về khối lượng mỗi kim loại trong hỗn hợp A.
Hòa tan hoàn toàn 5,5 gam hỗn hợp gồm Al và Fe vào lượng dư dung dịch H 2 SO 4 loãng, thu được 4,48 lít H 2 (đktc). Thành phần phần trăm khối lượng của Fe trong hỗn hợp đầu là
A. 50,91%
B. 76,36%
C. 25,45%
D. 12,73%