Viết các phương trình hoá học của các phản ứng xảy ra giữa các cặp chất sau đây:
a) Kẽm + Axit sunturic loãng ; b) Kẽm + Dung dịch bạc nitrat;
c) Natri + Lưu huỳnh ; d) Canxi + Clo.
Trong dung dịch, giữa các cặp chất nào sau đây có xảy ra phản ứng? Viết phương trình hoá học của các phản ứng đó.
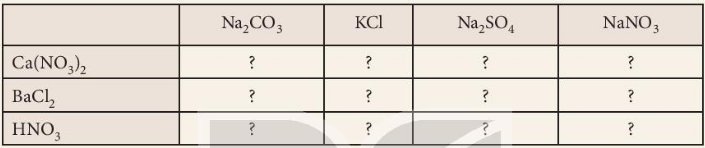
| Na2CO3 | KCl | Na2SO4 | NaNO3 | |
| Ca(NO3)2 | Có phản ứng (1) | Không phản ứng | Có phản ứng (2) | Không phản ứng |
| BaCl2 | Có phản ứng (3) | Không phản ứng | Có phản ứng (4) | Không phản ứng |
| HNO3 | Có phản ứng (5) | Không phản ứng | Không phản ứng | Không phản ứng |
Các PTHH:
\(\left(1\right)Ca\left(NO_3\right)_2+Na_2CO_3\rightarrow2NaNO_3+CaCO_3\downarrow\\ \left(2\right)Na_2SO_4+Ca\left(NO_3\right)_2\rightarrow CaSO_4+2NaNO_3\\ \left(3\right)Na_2CO_3+BaCl_2\rightarrow BaCO_3+2NaCl\\ \left(4\right)Na_2SO_4+BaCl_2\rightarrow BaSO_4+2NaCl\\ \left(5\right)2HNO_3+Na_2CO_3\rightarrow2NaNO_3+CO_2+H_2O\)
Cho các cặp chất sau đây phản ứng với nhau a, đồng oxit + axit sunfuric b, Fe3 sunfat + natri clorua c, kẽm +axit clohiđric Hãy nêu hiện tượng và viết phương trình hóa học xảy ra nếu có
\(a,CuO+H_2SO_4\rightarrow CuSO_4+H_2O\\ b,Fe_2\left(SO_4\right)_3+NaCl:Không.phản.ứng\\ c,Zn+2HCl\rightarrow ZnCl_2+H_2\)
Hiện tượng câu A: Dung dịch chuyển dần sang màu xanh lam.
Hiện tượng câu C: Kẽm tan, tạo thành dung dịch mới, có khí không màu thoát ra (sủi bọt khí)
Hãy viết PTHH của các phản ứng xảy ra giữa các cặp chất sau đây: a. Kẽm + Axitsunfuric b. Kẽm + dd bạc nitrat c. Natri + lưu huỳnh d. Canxi + Clo e. Magie oxit + axit nitric f. Sắt + axit clohidric g. Đồng(II) oxit + axit clohidric h. Nhôm + axitsunfuric loãng i. Clo + Natri hidroxit k. Magan(IV) oxit + axit clohidric
\(a.Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ b.Zn+2AgNO_3\rightarrow Zn\left(NO_3\right)_2+2Ag\\ c.2Na+S\xrightarrow[]{t^0}Na_2S\\ d.Ca+Cl_2\xrightarrow[]{t^0}CaCl_2\\ e.MgO+2HNO_3\rightarrow Mg\left(NO_3\right)_2+H_2O\\ f.Fe+2HCl\rightarrow FeCl_2+H_2\\ g.CuO+2HCl\rightarrow CuCl_2+H_2O\\ h.2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ i.Cl+2NaOH\rightarrow NaCl+NaClO+H_2O\\ k.MgO_2+4HCl_{đặc}\xrightarrow[nhẹ]{đun}MgCl_2+Cl_2+2H_2O\)
Bài 5. Trong dung dịch, giữa các cặp chất nào sau đây có xảy ra phản ứng? Viết phương trình hóa học của các phản ứng đó.
| Na2CO3 | KCl | Na2SO4 | NaNO3 |
Pb(NO3)2 |
|
|
|
|
BaCl2 |
|
|
|
|
HNO3 |
|
|
|
|
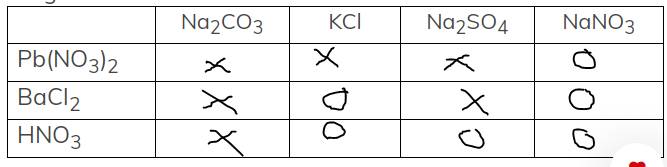
X : có phản ứng
O : không phản ứng
PTHH:
\(Pb\left(NO_3\right)_2+Na_2CO_3\rightarrow PbCO_3+2NaNO_3\\ Pb\left(NO_3\right)_2+2KCl\rightarrow PbCl_2+2KNO_3\\ Pb\left(NO_3\right)_2+Na_2SO_4\rightarrow PbSO_4+2NaNO_3\\ BaCl_2+Na_2CO_3\rightarrow BaCO_3+2NaCl\\ BaCl_2+Na_2SO_4\rightarrow BaSO_4+2NaCl\\ 2HNO_3+Na_2CO_3\rightarrow2NaNO_3+CO_2+H_2O\)
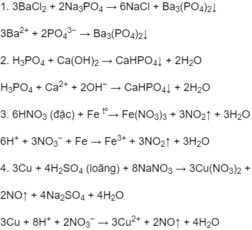
Viết phương trình hoá học ở dạng phân tử và dạng ion rút gọn của phản ứng xảy ra trong dung dịch giữa các chất sau:
1. bari clorua và natri photphat.
2. axit photphoric và canxi hiđroxit, tạo ra muối axit ít tan.
3. axit nitric đặc, nóng và sắt kim loại.
4. natri nitrat, axit sunfuric loãng và đồng kim loại.
Phương trình hoá học ở dạng phân tử và dạng ion rút gọn của các phản ứng xảy ra trong dung dịch :
VIẾT CÁC phương trình hoá học xảy ra giữa các cặp chất sau :A)O2vàFe ;B)O2và AL
\(3Fe+2O_2\underrightarrow{^{t^0}}Fe_3O_4\)
\(4Al+3O_2\underrightarrow{^{t^0}}2Al_2O_3\)
Có những chất sau: Sắt, lưu huỳnh, axit sunfuric loãng.
Viết các phương trình phản ứng xảy ra và cho biết vai trò của lưu huỳnh trong các phản ứng
Fe + S → FeS(1)
FeS + H2SO4 → FeSO4 + H2S (2)
Fe + H2SO4 → FeSO4 + H2 (3)
H2 + S → H2S (4)
Vai trò của S trong phản ứng (1), (4) : S là chất oxi hóa.
Cho các chất CuO, SO2, H2O, H2SO4 loãng, NAOH, CACO3, FESO4 chất nào tác dụng được với nhau từng đôi một. Viết các phương trình hoá học các phản ứng xảy ra?
Cho 6,5 g kẽm vào 300ml dung dịch H2SO4 loãng có nồng độ 1M
a. Viết phương trình phản ứng xảy ra.
b. Tính số mol các chất có trong dung dịch sau phản ứng.
c. Tính nồng độ mol của các chất sau phản ứng. Coi thể tích dung dịch không đổi.
Help. Mai thi hóa r :(
\(n_{Zn}=\dfrac{6.5}{65}=0.1\left(mol\right)\)
\(n_{H_2SO_4}=0.3\cdot1=0.3\left(mol\right)\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(0.1........0.1...........0.1.......0.1\)
\(\Rightarrow H_2SO_4dư\)
\(n_{H_2SO_4\left(dư\right)}=0.3-0.1=0.2\left(mol\right)\)
\(n_{ZnSO_4}=n_{H_2}=0.1\left(mol\right)\)
\(C_{M_{ZnSO_4}}=\dfrac{0.1}{0.3}=0.33\left(M\right)\)
\(C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0.2}{0.3}=0.66\left(M\right)\)
\(a) Zn + H_2SO_4 \to ZnSO_4 + H_2\\ b) n_{Zn} = \dfrac{6,5}{65} = 0,1 < n_{H_2SO_4} =0,3 \to H_2SO_4\ dư\\ n_{H_2SO_4\ pư} = n_{ZnSO_4} = n_{Zn} = 0,1(mol)\\ n_{H_2SO_4\ dư} = 0,3 - 0,1 = 0,2(mol)\\ c) C_{M_{ZnSO_4}} = \dfrac{0,1}{0,3} = 0,33M\\ C_{M_{H_2SO_4}} = \dfrac{0,2}{0,3} = 0,67M\)
\(n_{Zn}=\dfrac{m}{M}=0,1\left(mol\right)\)
\(n_{H2SO4}=C_M.V=0,3\left(mol\right)\)
a, \(PTHH:Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
b, Thấy 0,3 > 0,1
=> Sau phản ứng Zn hết, H2SO4 còn dư ( dư 0,3 - 0,1 = 0,2 mol )
- Theo PTHH : \(n_{ZnSO4}=n_{Zn}=0,1\left(mol\right)\)
c, Ta có : \(\left\{{}\begin{matrix}C_{MH2SO4}=\dfrac{n}{V}=\dfrac{2}{3}M\\C_{MZnSO4}=\dfrac{n}{V}=\dfrac{1}{3}M\end{matrix}\right.\)