Cho 9,6 gam bột kim loại M vào 500 ml dung dịch HCl 1M, khi phản ứng kết thúc thu được 5,376 lít H2 (đktc). Kim loại M là:
A.Mg
B.Ca
C.Fe
D.Ba
Cho 9,6 gam bột kim loại M vào 500 ml dung dịch HCI 1M, khi phản ứng kết thúc thu được 5,376 lít H2 (đktc). Kim loại M là
A. Mg. B. Ca.
C. Fe. D. Ba.
Số mol khí H2 là:
n(H2) = 5,376/22,4 = 0,24 (mol)
V(ddHCl) = 500ml = 0,5l
Số mol HCl là:
n(HCl) = V(ddHCl).1 = 0,5.1 = 0,5 (mol)
Pthh: 2M + (2x)HCl → 2MClx + (x)H2
Số mol HCl phản ứng:
n(HCl pứ) = 2. n(H2) = 2.0,24 = 0,48 (mol). So với ban đầu thì HCl phản ứng còn dư.
Theo pthh thì: n(M) = 0,48/x (mol)
Khối lượng mol của kim loại M là:
9,6/n(M) = 9,6/(0,48/x) = 20x
--> x = 2 --> 20x = 40 (g/mol)
Vậy M là Ca --> Chọn B.
Cho 9,6 gam bột kim loại M vào 500ml dung dịch HCl 1M, sau phản ứng kết thúc thu được 5,376 (lít) H2 (đktc). Kim loại M là kim loại nào sau đây.
A. Mg.
B. Cu.
C. Fe.
D. Cr.
Đáp án B.
Số mol H2 là:
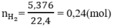
Số mol HCl nHCl = 0,5.1 = 0,5(mol)
2M + 2nHCl → 2MCln + nH2
Số mol HCl phản ứng: nHCl = 2. nH2 = 2.0,24 = 0,48(mol). So với ban đầu HCl phản ứng còn dư
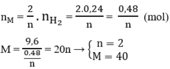
Vậy M là Ca
Cho 9,6 gam bột kim loại M vào 500 ml dung dịch HCl 1M, khi phản ứng kết thúc thu được 5,376 lít H2 (đktc). Kim loại M là
A. Mg. B. Ca. C. Fe. D. Ba.
Chọn B
Gọi hoá trị của kim loại M là n:
2M + 2nHCl → 2MCln + nH2 (1)
=
= 0,24 (mol)
Từ (1) => nM = =
(mol)
Ta có: .M = 96 => M =
Biên luận: n = 1 => M = 20 (loại)
n = 2 => M = 40 (Ca)
n = 3 => M = 60 (loại)
Cho 9,6 gam bột kim loại M vào 500 ml dung dịch HCl 1M, khi phản ứng kết thúc thu được 5,376 lít H2 (đktc). Kim loại M là
A. Mg. B. Ca. C. Fe. D. Ba.
Chọn B
Gọi hoá trị của kim loại M là n:
2M + 2nHCl → 2MCln + nH2 (1)
=
= 0,24 (mol)
Từ (1) => nM = =
(mol)
Ta có: .M = 96 => M =
Biên luận: n = 1 => M = 20 (loại)
n = 2 => M = 40 (Ca)
n = 3 => M = 60 (loại)
Cho 22,4 gam bột kim loại M vào dung dịch HCl dư, sau khi phản ứng kết thúc thu được 0,8 gam H2. Kim loại M là
A. Mg.
B. Ca
C. Fe
D. Zn
Đáp án C
Số mol H2 thu được là: n H 2 = 0 , 8 2 = 0 , 4 m o l
Gọi n là hóa trị của M
Phương trình hóa học:
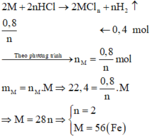
=> M là Fe
Hòa tan kim loại M vào 200 ml dung dịch HCl 1M, sau khi các phản ứng xảy ra hoàn toàn, thu được 3,36 lít khí H 2 (đktc) và dung dịch X chứa 29,35 gam chất tan. Kim loại M là
A. Na
B. Ba
C. K
D. Al
Cho 9,6 gam hỗn hợp kim loại Mg và Fe vào dung dịch H2SO4 dư thấy thoát ra 6,72 lít H2 (đktc). Mặt khác khi cho 9,6 gam hỗn hợp trên vào 500 ml dung dịch AgNO3 1,5M đến phản ứng hoàn toàn thu được m gam chất rắn. Giá trị của m là:
A. 81,0 gam
B. 56,7 gam
C. 48,6 gam
D. 72,9 gam
Chọn D
24nMg + 56nFe = 9,6g ; nMg + nFe = nH2 = 0,3 mol
=> nMg = 0,225 mol ; nFe = 0,075 mol
Mg + 2Ag+ -> Mg2+ + 2Ag
Fe + 2Ag+ -> Fe2+ + 2Ag
Fe2+ + Ag+ -> Fe3+ + Ag
=> mAg = 108.(2nMg + 3nFe) = 72,9g
Cho 5,04 gam bột Fe vào 300 ml dung dịch AgNO3 1M, sau khi kết thúc phản ứng, thu được m gam kim loại. Giá trị của m là
A. 32,96 gam
B. 19,44 gam
C. 29,16 gam
C. 29,16 gam
Cho 5,04 gam bột Fe vào 300 ml dung dịch AgNO3 1M, sau khi kết thúc phản ứng, thu được m gam kim loại. Giá trị của m là
A. 29,16 gam.
B. 19,44 gam
C. 32,40 gam
D. 32,96 gam.
Đáp án A
n F e = 0 , 09 ; n A g N O 3 = 0 , 3
Do vậy AgNO3 dư nên ta thu được 0,27 mol Ag.
=> m= 29,16 g