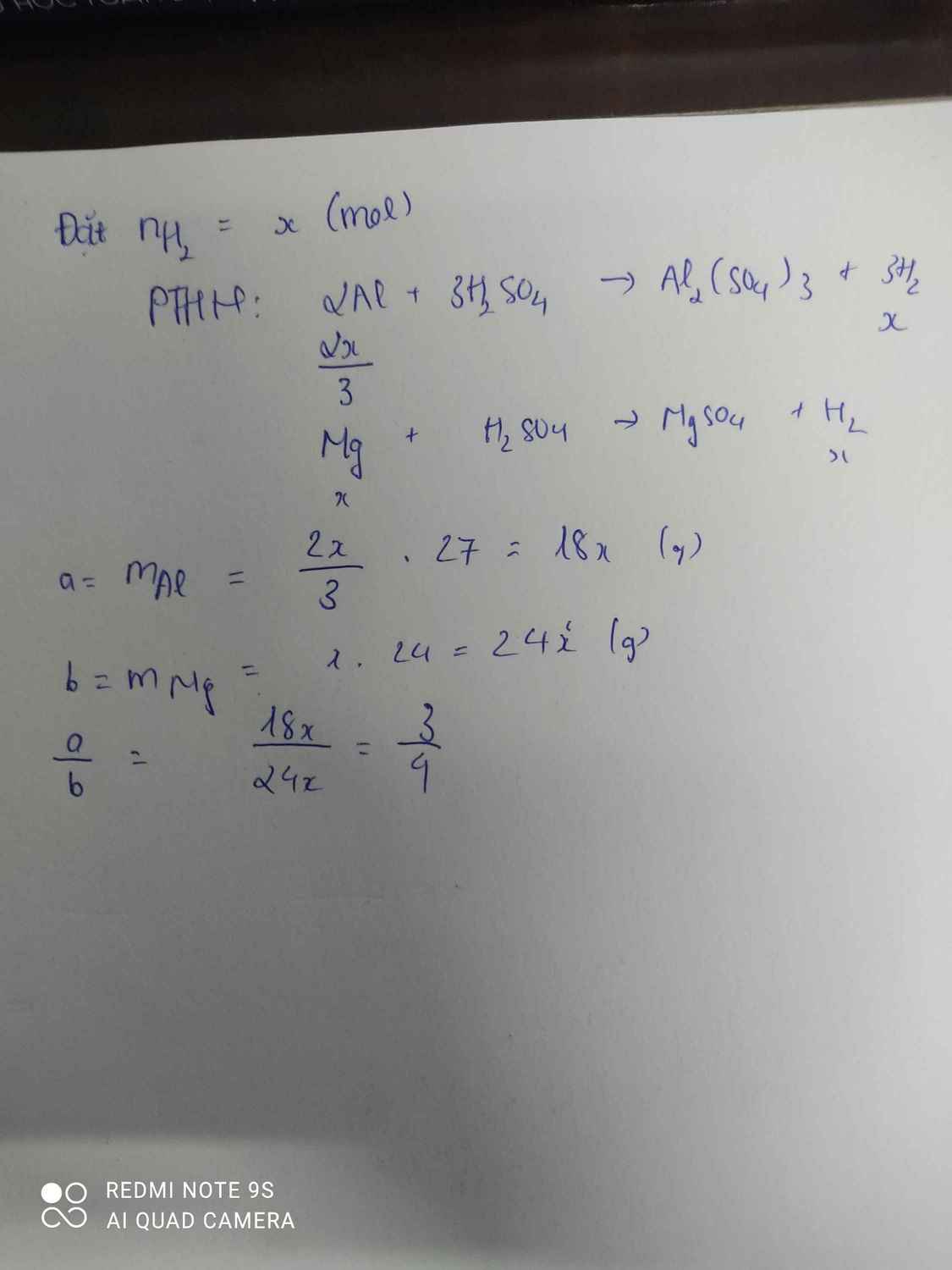Hoà tan a g Al và b g Zn cào dd H2SO4 dư thu được những thể tích khí H2 bằng nhau. Tính tỉ lệ a:b. Giúp vs mn

Những câu hỏi liên quan
Hòa tan a (g) Al và b (g) dd H2SO4 loãng, dư thu được thể tích H2 bằng nhau. Tính tỉ lệ a:b?
Giả sử có 1 mol \(H_2\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(\dfrac{2}{3}\) 1 1 ( mol )
\(m_{Al}=\dfrac{2}{3}.27=18g\)
\(m_{H_2SO_4}=1.98=98g\)
\(a:b=\dfrac{18}{98}=\dfrac{9}{49}\)
Đúng 1
Bình luận (0)
Hoà tan a g Al và b g Zn cào dd H2SO4 dư thu được những thể tích khí H2 bằng nhau. Tính tỉ lệ a:b. Giúp vs mn
Cô sẽ chữa bài này như sau:
2Al+ 3H2SO4-> Al2(SO4)3 +3H2
a/27 ------------------------------a/18 Zn+H2SO4 -> ZnSO4 +H2 b/65 ----------------------b/65 a/18=b/65 <=> a=18b/65
Đúng 0
Bình luận (6)
Hòa tan a gam Al và b gam Zn vào dung dịch axit H2SO4 dư thu được những thể tích khí H2 bằng nhau. Tính tỉ lệ a:b
Hãy cứu lấy tui~
Cảm ơn nhiềuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuu~
Gọi \(n_{H_2}=x\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(\dfrac{2}{3}x\) x ( mol )
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(x\) x ( mol )
\(a:b=\dfrac{\dfrac{2}{3}x.27}{65x}=\dfrac{18x}{65x}=\dfrac{18}{65}\)
Đúng 3
Bình luận (1)
Đặt nH2 là x(mol)
PTHH: 2Al + 3H2SO4 -----> Al2(SO4)3 + 3H2
2x/3 x
mAl= 2x/3 . 27= 18x (g)
PTHH: Mg + H2SO4 -------> MgSO4 + H2
x x
mMg= 1x . 24= 24x (g)
Theo tỉ lệ: a/b= 18x/24x= 3/4
Đúng 1
Bình luận (1)
Hòa tan a gam Al và b gam Zn vào dung dịch axit H2SO4 dư thu được những thể tích khí H2 bằng nhau . Tinh tỉ lệ a:b
Giả sự đều sinh ra 1 mol H2
2Al+3H2SO4--->Al2(SO4)3+3H2
2/3_______________________1
=>a=2/3.27=18
Zn+H2SO4--->ZnSO4+H2
1___________________1
=>b=65
===> a/b=18/65
Đúng 1
Bình luận (0)
Hòa tan m1 (g) Al và m2 (g) Zn bằng dd HCl dư thu được những thể tích H2 như nhau. Tính tỉ lệ m1: m2
giả sử đều sinh ra 1(mol) h2
pthh:
2Al+6HCl..==>2AlCl3.+3H2
2/3....................................1
Zn+2HCl...==>..ZnCl2.+.H2
1......................................1
m1:m2=18:65
Đúng 0
Bình luận (0)
4.2 Hòa tan a gam Al và b gam Mg vào dung dịch axit H2SO4 dư thu được những thể tích khí H2 bằng nhau trong cùng điều kiện. tính tỉ lệ a/b
Hòa tan a gam Al và b gam Zn bằng dung dịch HCl dư , thu được những thể tích khí H2 như nhau ( ở cùng điều kiện nhiệt độ và áp suất ) . Tính tỉ lệ a : b
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Zn + 2HCl \to ZnCl_2 + H_2$
$n_{Al} = \dfrac{a}{27} (mol) \Rightarrow n_{H_2} = \dfrac{3}{2}n_{Al} = \dfrac{a}{18}(mol)$
$n_{Zn} = \dfrac{b}{65}(mol) \Rightarrow n_{H_2} = n_{Zn} = \dfrac{b}{65}(mol)$
$\Rightarrow \dfrac{a}{18} = \dfrac{b}{65}$
$\Rightarrow \dfrac{a}{b} = \dfrac{18}{65}$
Đúng 2
Bình luận (0)
Trộn 2 dd H2SO4 2M với HCl 1,5M với nhau theo tỉ lệ thể tích 1:1 thu được dd X. Hoà tan hoàn toàn 5,1g hỗn hợp Y gồm Mg và Al trong 200ml dd X thu được 5,6 lít H2 (đktc) và dung dịch Z. a. CMR : dd Z còn dư axit b. Cho 300ml dd B gồm Ba(OH)2 0,6M và NaOH 1M vào dd Z. Tính khối lượng kết tủa thu được sau phản ứng.
Theo gt ta có: $n_{H_2SO_4}=0,2(mol);n_{HCl}=0,15(mol);n_{H_2}=0,25(mol)$
a, Bảo toàn H ta có: $n_{H^+/pu}=0,5(mol)< 0,55(mol)$
Do đó axit còn dư
b, Ta có: $n_{Ba(OH)_2}=0,18(mol);n_{NaOH}=0,3(mol)$
Gọi số mol Mg và Al lần lượt là a;b(mol)
$\Rightarrow 24a+27b=5,1$
Bảo toàn e ta có: $2a+3b=0,5$
Giải hệ ta được $a=b=0,1$
Lượng $OH^-$ tạo kết tủa là $0,18.2+0,3-0,05=0,61(mol)$
Kết tủa gồm 0,18 mol $BaSO_4$; 0,1 mol $Mg(OH)_2$ (Do Al(OH)3 tạo ra bị hòa tan hết)
$\Rightarrow m_{kt}=47,74(g)$
Đúng 2
Bình luận (0)
hoà tan hoàn toàn 6,5 gam zn bằng 200ml dd hc, thu được dd A và khí H2. tính thể tích khí h2 thu được và nồng độ mol của dd thu được sau phản ứng.
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo PT: \(n_{H_2}=n_{Zn}=0,1\left(mol\right)\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
\(n_{ZnCl_2}=n_{Zn}=0,1\left(mol\right)\Rightarrow C_{M_{ZnCl_2}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
Đúng 3
Bình luận (0)