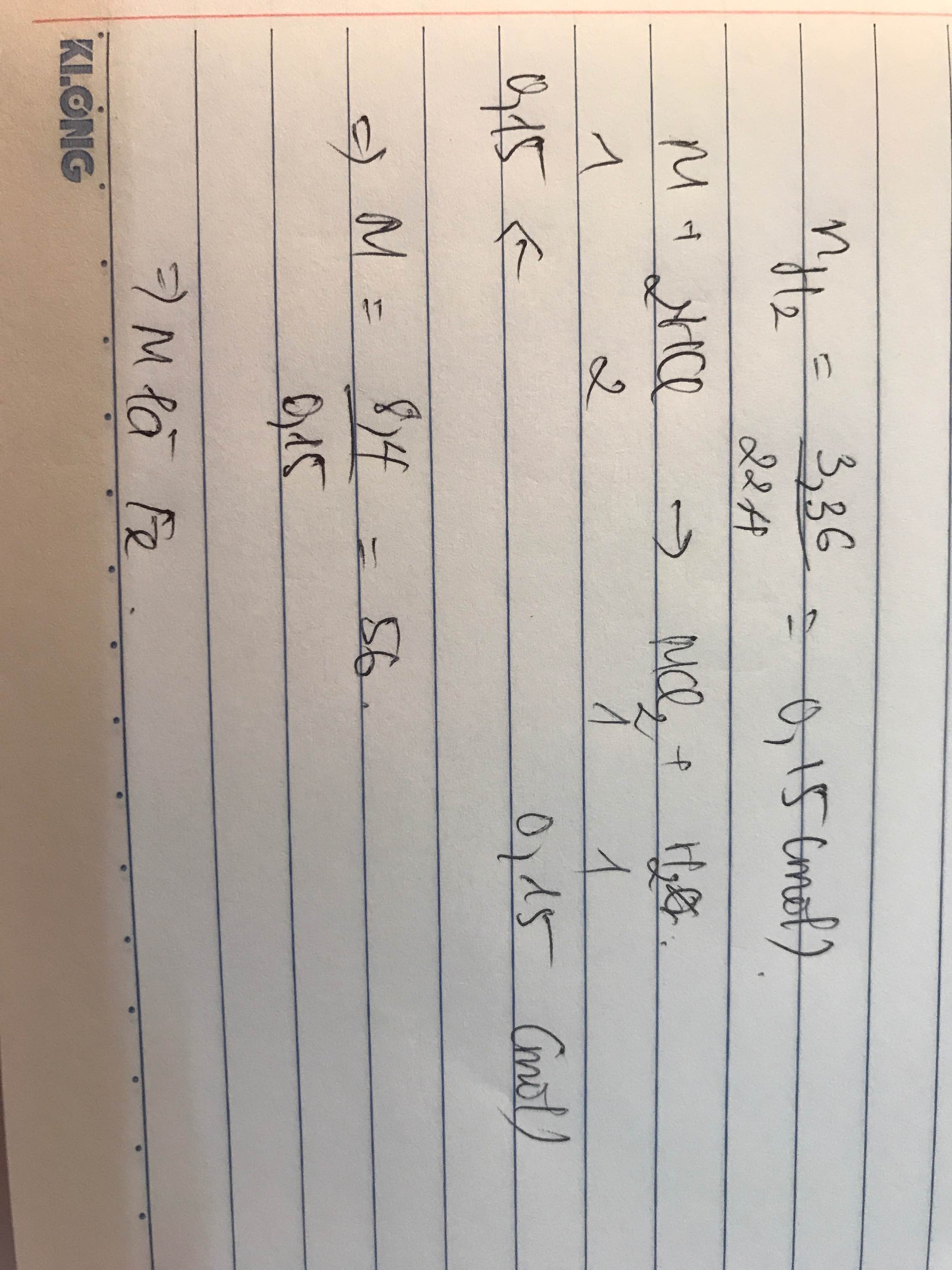hòa tan 16,25g một kim loại a hóa trị 2 bằng 2lit dung dịch hcl 0,3M thì thấy kim loại hòa tan hoàn toàn. sau phản ứng thu được 5,6l khí h2 và dung dịch b. xác định tên kim loại và nồng độ mol các chất có trong dung dịch B

Những câu hỏi liên quan
Hòa tan hoàn toàn 4g hỗn hợp X gồm Fe và kim loại hóa trị II vào dung dịch HCl dư thu được 2,24 lít khí H2 ở (đkt). Nếu dùng 2,4g kim loại hóa trị II hòa tan vào dung dịch HCl thì dùng không hết 0,5 mol dung dich HCl.
a. Xác định tên kim loại hóa trị II.
b. Tính thành phần % theo khối lượng của mỗi kim loại trong 4g hỗn hợp X
cho 8,4 gam một kim loại M hóa trị II vào dung dịch HCl 10% dư. Sau khi kim loại hòa tan hoàn toàn thu được 3,36 lít khí đo ở đktc và dung dịch A.
a. Xác định kim loại M
b.Để phản ứng hết dung dịch A cần 500ml dung dịch NaOH 1M. Tính nồng độ phần trăm các chất trong dung dịch A
dạ em làm xong câu B rồi mọi người khỏi cần trả lời nữa ạ
Đúng 0
Bình luận (2)
Hòa tan hoàn toàn 4,8 gam một kim loại R có hóa trị II vào 100 ml dung dịch HCl 5M. Sau phản ứng thu được 4,48 lít khí (đktc) và dung dịch A. Xác định R và tính nồng độ mol/lít các chất có trong dung dịch A.
PTHH: R + 2HCl ---> RCl2 + H2 (1)
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{100}{1000}.5=0,5\left(mol\right)\)
Ta thấy: \(\dfrac{0,2}{1}< \dfrac{0,5}{2}\)
Vậy HCl dư.
Theo PT(1): \(n_R=n_{H_2}=0,2\left(mol\right)\)
=> \(M_R=\dfrac{4,8}{0,2}=24\left(g\right)\)
Vậy R là magie (Mg)
PT: Mg + 2HCl ---> MgCl2 + H2 (2)
Ta có: \(m_{dd_{MgCl_2}}=4,8+\dfrac{100}{1000}-0,2.2=4,5\left(lít\right)\)
Theo PT(2): \(n_{MgCl_2}=n_{H_2}=0,2\left(mol\right)\)
=> \(C_{M_{MgCl_2}}=\dfrac{0,2}{4,5}=\dfrac{2}{45}M\)
Đúng 0
Bình luận (0)
Hòa tan 0,54g một kim loại R ( có hóa trị III ) bằng 50 ml dung dịch HCl 2M. Sau phản ứng thu được 0,672 lít khí ( ở đktc )
a) Xác định kim loại R
b) Tính nồng độ mol của dung dịch thu được sau phản ứng
a) \(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
nHCl = 0,05.2 = 0,1
Có 2.nH2 < nHCl => R phản ứng hết
PTHH: 2R + 6HCl --> 2RCl3 + 3H2
____0,02<-----------------------0,03
=> \(M_R=\dfrac{0,54}{0,02}=27\left(Al\right)\)
b)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
___________0,06<----0,02<---0,03
=> \(\left\{{}\begin{matrix}C_{M\left(HCldư\right)}=\dfrac{0,1-0,06}{0,05}=0,8M\\C_{M\left(AlCl_3\right)}=\dfrac{0,02}{0,05}=0,4M\end{matrix}\right.\)
Đúng 2
Bình luận (1)
1) Xác định tên kim loại A và M khi:a) Hòa tan hoàn toàn 2,7 gam kim loại A (hóa trị III) trong dung dịch HCl dư sau phản ứng thu được 13,35 gam muối.b) Hòa tan hoàn toàn 4,8 gam kim loại M trong dung dịch HCl dư sau phản ứng thu được 4,48 lit khí (đktc).
Đọc tiếp
1) Xác định tên kim loại A và M khi:
a) Hòa tan hoàn toàn 2,7 gam kim loại A (hóa trị III) trong dung dịch HCl dư sau phản ứng thu được 13,35 gam muối.
b) Hòa tan hoàn toàn 4,8 gam kim loại M trong dung dịch HCl dư sau phản ứng thu được 4,48 lit khí (đktc).
\(a,n_A=\dfrac{2,7}{M_A}\left(mol\right)\\ n_{ACl_3}=\dfrac{13,35}{M_A+106,5}\)
PTHH: \(2A+6HCl\rightarrow2ACl_3+3H_2\)
\(\dfrac{2,7}{M_A}\)-------------->\(\dfrac{2,7}{M_A}\)
\(\rightarrow\dfrac{2,7}{M_A}=\dfrac{13,35}{M_A+106,5}\\ \Leftrightarrow M_A=27\left(g\text{/}mol\right)\)
=> A là Al
\(b,n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: \(2M+2nHCl\rightarrow2MCl_n+nH_2\) (n là hoá trị của M, n ∈ N*)
\(\dfrac{0,4}{n}\)<---------------------------0,2
\(\rightarrow M_M=\dfrac{4,8}{\dfrac{0,2}{n}}=12n\left(g\text{/}mol\right)\)
Vì n là hoá trị của M nên ta có bảng
| n | 1 | 2 | 3 |
| MM | 12 | 24 | 36 |
| Loại | Mg | Loại |
Vậy M là Mg
Đúng 1
Bình luận (0)
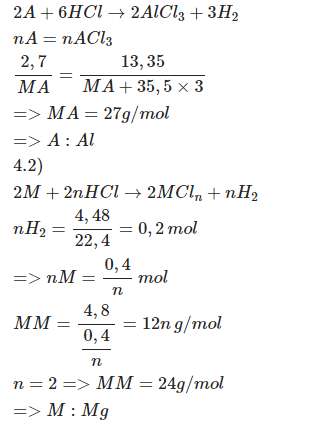
\(\Rightarrow\) \(M:mg\)
Cho 12,8 gam kim loại A hóa trị II phản ứng hoàn toàn với khí Cl2 thu muối B. Hòa tan B vào nước thu được 400ml dung dịch C. Nhúng thanh sắt nặng 11,2 gam vào dung dịch C, sau một thời gian thấy kim loại A bám vào thanh sắt và khối lượng thanh sắt là 12,0 gam, nồng độ FeCl2 trong dung dịch là 0,25M. Xác định kim loại A và nồng độ mol của kim loại B trong dung dịch C.
Đọc tiếp
Cho 12,8 gam kim loại A hóa trị II phản ứng hoàn toàn với khí Cl2 thu muối B. Hòa tan B vào nước thu được 400ml dung dịch C. Nhúng thanh sắt nặng 11,2 gam vào dung dịch C, sau một thời gian thấy kim loại A bám vào thanh sắt và khối lượng thanh sắt là 12,0 gam, nồng độ FeCl2 trong dung dịch là 0,25M. Xác định kim loại A và nồng độ mol của kim loại B trong dung dịch C.
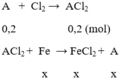
số mol FeCl2 là n = 0,25 . 0,4 = 0,1 (mol)
gọi x là số mol Fe phản ứng
khối lượng kim loại tăng là Δm = mA - mFe = Ax – 56x = 0,8
x = 0,1 → A.0,1 – 56.0,1 = 0,8 → A = 64. A là Cu
số mol Cu là nCu = 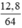 = 0,2 (mol)
= 0,2 (mol)
số mol CuCl2 → n(CuCl2) = nCu = 0,2 (mol)
nồng độ mol/l CuCl2 là C(M(CuCl2)) = 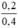 = 0,5M
= 0,5M
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 16,25g một kim loại hóa trị II bằng dd HCl 18,25%(D=1,2g/ml) thu được dd muối và 5,6l khí hiđrô
a)Xác định kim loại
b)Xác định khối lượng dd HCl 18,25% đã dùng
Tính nồng độ mol của dd HCl trên
c)Tìm nồng độ phần trăm của dd muối sau phản ứng
Giúp với nha m.n
a) Gọi KL cần tìm là X
nHCl=\(\frac{5,6}{22,4}\)=0,25
PTHH: X + HCl \(\rightarrow\) XCl2 + H2
0,25 0,5 0,25 0,25
\(\Rightarrow\)mX = \(\frac{16.25}{0,25}\)=65g ( Zn )
b) mHCl= \(0,5.36,5\)=18.25g
mdd= \(\frac{18.25}{0,1825}\)=100g
Cm = \(\frac{0,5}{\frac{0,1}{0,2}}\)=6 mol/l
c) C% = 0,25.(65+71)/(100+16,25-0,5).100=29.73%
Đúng 0
Bình luận (4)
a) Gọi kl cần tìm là X
nHCl= 5.6/22.4=0.25
PTHH: X + HCl -> XCl2 + H2
0.25 0.5 0.25 0.25
=>mX = 16.25/0.25=65g ( Zn )
b) mHCl= 0.5*36.5=18.25g
mdd= 18.25/0.1825=100g
Cm = 0.5/(0.1/1.2)=6 mol/l (lơn z tar)
c) C% = 0.25*(65+71)/(100+16.25-0.5)*100=29.73%
Đúng 0
Bình luận (0)
Hòa tan 14,4 gam kim loại R hóa trị II trong dung dịch HCl 29,2%. Sau khi phản ứng hoàn toàn thu được dung dịch mới có nồng độ HCl 5,456% và nồng độ muối clorua là 28,401%. Xác định kim loại R.
hòa tan hoàn toàn 7,8 gam kim loại kiềm trong dung dịch hcl 10% sau phản ứng thu được dung dịch x và 2,24 lít khí
a .xác định tên của kim loại trên
b. tìm nồng độ phần trăm của các chất trong dung dịch sau phản ứng biết HCl dùng dư 20% so với lượng phản ứng
Xem chi tiết
Gọi kim loại cần tìm là A
a) PTHH: \(A+H_2O\rightarrow AOH+\dfrac{1}{2}H_2\uparrow\)
\(AOH+HCl\rightarrow ACl+H_2O\)
b) Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\) \(\Rightarrow n_A=0,2mol\)
\(\Rightarrow M_A=\dfrac{7,8}{0,2}=39\) \(\Rightarrow\) Kim loại cần tìm là Kali
b) Ta có: \(\left\{{}\begin{matrix}n_{KCl}=0,2mol\\n_{HCl\left(pư\right)}=0,2mol\Rightarrow n_{HCl\left(dư\right)}=0,2\cdot20\%=0,04\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{KCl}=0,2\cdot74,5=14,9\left(g\right)\\m_{HCl\left(dư\right)}=0,04\cdot36,5=1,46\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{H_2}=2\cdot0,1=0,2\left(g\right)\)
\(\Rightarrow m_{dd}=m_K+m_{ddHCl}-m_{H_2}=7,8+\dfrac{0,24\cdot36,5}{10\%}-0,2=95,2\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{KCl}=\dfrac{14,9}{95,2}\cdot100\%\approx15,65\%\\C\%_{HCl\left(dư\right)}=\dfrac{1,46}{95,2}\cdot100\%\approx1,53\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)