Cho 5,4g kim loại có hóa trị không đổi phản ứng với O2 tạo ra 10,2g oxit. Xác định tên của kim loại và công thức oxit của nó.
( giải chi tiết- Thanks so much)
Cho 5,4g kim loại có hóa trị không đổi phản ứng với O2 tạo ra 10,2g oxit. Xác định tên của kim loại và công thức oxit của nó?
Cho 5,4g kim loại có hóa trị không đổi phản ứng với O2 tạo ra 10,2g oxit. Xác định tên của kim loại và công thức oxit của nó.
( giải chi tiết- Thanks so much)
Bài 7: Đốt cháy hết 5,4g một kim loại hóa trị (III) trong khí oxi dư, thu được 10,2g oxit. Xác định công thức hóa học và gọi tên oxit trên?
Gọi kim loại cần tìm là R
\(n_R=\dfrac{5,4}{M_R}\left(mol\right)\)
PTHH: 4R + 3O2 --to--> 2R2O3
\(\dfrac{5,4}{M_R}\)--------------->\(\dfrac{2,7}{M_R}\)
=> \(\dfrac{2,7}{M_R}\left(2.M_R+48\right)=10,2\)
=> MR = 27 (g/mol)
=> R là Al
CTHH của oxit: Al2O3 (Nhôm oxit)
Cho 3,36 lit khí oxi (ở đktc) phản ứng hoàn toàn với 1 kim loại hóa trị III thu được 10,2g oxit. Xác định tên kim loại.
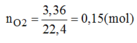
Gọi A là kí hiệu của kim loại có hóa trị III, M A là nguyên tử khối của A.
Ta có PTHH:

Theo PTHH trên ta có:
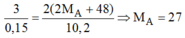
Vậy A là nhôm.
Câu 1: Cho 5,4g một kim loại R(hóa trị III) tác dụng với Oxi thu được 10,2g. Xác định khối lượng R và CTHH của oxit
Câu 2: Oxit hóa 16,8 lít khí SO2(ĐKTC) a) Viết PTHH b) Tính VO2 c)Tìm hiệu suất của phản ứng
Bài 1 :
\(m_{O_2}=10.2-5.4=4.8\left(g\right)\)
\(n_{O_2}=\dfrac{4.8}{32}=0.15\left(mol\right)\)
\(4R+3O_2\underrightarrow{^{^{t^0}}}2R_2O_3\)
\(0.2......0.15\)
\(M_R=\dfrac{5.4}{0.2}=27\left(\dfrac{g}{mol}\right)\)
=> R là : Al
CTHH : Al2O3
Câu 2:
a) nSO2=0,75(mol)
PTHH: \(SO2+\dfrac{1}{2}O2⇌\left(to,xt\right)SO3\)
nO2=nSO2/2=0,75/2=0,375(mol)
=>V(O2,ĐKTC)=0,375.22,4=8,4(l)
c) Tìm hiệu suất là sao em?
Đề chưa chặt chẽ
BÀI 1 CÁCH KHÁC:
PTHH: 4 R + 3 O2 -to-> 2 R2O3
Theo PT: 4M(R)________4M(R)+96(g)
Theo đề): 5,4__________10,2(g)
Theo PTHH và đề bài ta có:
10,2.4M(R)=5,4.(4M(R)+96)
<=>19,2M(R)=518,4
<=>M(R)=27(g/mol)
=>R(III) cần tím là Nhôm (Al=27)
=> CTHH oxit: Al2O3
Chúc em học tốt!
Cho 12,4 gam oxit của kim loại A có hóa trị I phản ứng vừa đủ với 200ml dung dịch axit nitric 2M. Viết phương trình phản ứng và xác định tên oxit kim loại đã sử dụng
\(A_2O+2HNO_3\rightarrow2ANO_3+H_2O\)
\(n_{A_2O}=\dfrac{1}{2}n_{HNO_3}=0,2\left(mol\right)\)
=> \(M_{A_2O}=\dfrac{12,4}{0,2}=62\)
Ta có : 2A + 16 =62
=> A=23 (Na)
Vậy oxit cần tìm là Na2O
cho 12,4 gam oxit của kim loại A có hóa trị I phản ứng vừa đủ với 200ml dung dịch axit nitric 2M . Viết phương trình phản ứng và xác định tên oxit kim loại đã sử dụng ?
$n_{HNO_3} = 0,2.2 = 0,4(mol)$
Gọi oxit cần tìm là $A_2O$
$A_2O + 2HNO_3 \to 2ANO_3 + H_2O$
$n_{oxit} = \dfrac{1}{2}n_{HNO_3} = 0,2(mol)$
$\Rightarrow M_{oxit} = 2A + 16 = \dfrac{12,4}{0,2} = 62$
$\Rightarrow A = 23(Natri)$
1. Cho 0,6g một kim loại hóa trị II tác dụng với nước tạo ra 0,336 l khí H2(đktc). Tìm tên kim loại.
2. Cho 4.48g một oxit kim loại hóa trị II, tác dụng hết với 100ml dung dịch H2SO4 0,8M. Xác định tên kim loại.
*trình bày chi tiết giúp mình với ạ
\(n_{H_2}=\dfrac{0.336}{22.4}=0.015\left(mol\right)\)
\(M+2HCl\rightarrow MCl_2+H_2\)
\(0.015........................0.015\)
\(M_M=\dfrac{0.6}{0.015}=40\left(\dfrac{g}{mol}\right)\)
\(M:Canxi\left(Ca\right)\)
\(n_{H_2SO_4}=0.1\cdot0.8=0.08\left(mol\right)\)
\(M+H_2SO_4\rightarrow MSO_4+H_2\)
\(0.08.....0.08\)
\(M_M=\dfrac{4.48}{0.08}=56\left(\dfrac{g}{mol}\right)\)
\(M:Sắt\left(Fe\right)\)
1/
nH2=0,336/22,4=0,015(mol)
gọi KL là M.
PTHH:M+2H2O-->M(OH)2+H2(1)
0,015 0,015 (mol)
Từ pt(1)-->nM=0,015(mol)
-->MM=0,6/0,015=40(g/mol)
-->M là Canxi(Ca)
2/
nH2SO4=0,1.0,8=0,08(mol)
gọi KL là R
PTHH:R+H2SO4-->RSO4+H2(2)
0,08 0,08 (mol)
từ pt (2)-->nR=0,08(mol)
-->MR=4,48/0,08=56(g/mol)
-->R là Sắt(Fe)
nhớ tích đúng cho mình nha!
Cho 9,4 gam oxit kim loại A có hóa trị I phản ứng hết với dung dịch axit clohidđric HCl, sau phản ứng thu được nước và 14,9 gam muối clorua (tạo bởi kim loại liên kết với clo). Xác định CTHH của oxit kim loại A
\(n_{A_2O}=\dfrac{9,4}{2M_A+16}\left(mol\right)\)
PTHH: A2O + 2HCl --> 2ACl + H2O
\(\dfrac{9,4}{2M_A+16}\)-->\(\dfrac{9,4}{M_A+8}\)
=> \(\dfrac{9,4}{M_A+8}\left(M_A+35,5\right)=14,9\Rightarrow M_A=39\left(g/mol\right)\)
=> A là K
CTHH: K2O