Khí metan CH4 cháy trong Oxi tạo ra khí cacbonic và hơi nước
a , tính thể tích Oxi cần dùng để đốt cháy hết 11,2 lít khí metan
b , muốn có thể tích Oxi nói trên cần phải phân hủy bao nhiêu gam kali clorat
a) PTHH: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
b+c)
Vì trong chất khí, tỉ lệ số mol cũng chính là tỉ lệ về thể tích
\(\Rightarrow\left\{{}\begin{matrix}V_{CO_2}=V_{CH_4}=11,2\left(l\right)\\V_{O_2}=2V_{CH_4}=22,4\left(l\right)\end{matrix}\right.\)
Khí metan tan cháy trong oxi tạo thành khí cacbonic và hơi nước
a.tính thể tích oxi cần thiết để đốt cháy 11,2 lít metan
b.tính thể tích khí cacbonic tạo thành trong phản ứng trên (các thể tích khí được đo ở dktc)
Đốt cháy hoàn toàn 11,2 lít khí Metan (CH4).
a. Viết phương trình phản ứng xảy ra
b. Tính thể tích Oxi cần dùng để đốt cháy lượng khí trên?
c. Dẫn toàn bộ khí sinh ra qua dung dịch nước vôi trong Ca(OH)2 dư thì thu được bao nhiêu gam kết tủa?
Thể tích các khí đo ở điều kiện tiêu chuẩn
(Cho biết : C=12; O=16; Ca=40; H=1; Br=80)
a, \(n_{CH_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH:
CH4 + 2O2 --to--> CO2 + 2H2O
0,5--->1------------->0,5
Ca(OH)2 + CO2 ---> CaCO3 + H2O
0,5----->0,5
b, \(V_{O_2}=1.22,4=22,4\left(l\right)\)
c, \(m_{CaCO_3}=0,5.100=50\left(g\right)\)
1)Đốt cháy hoàn toàn 12,395 lít khí metan. Hãy tính thể tích khí oxi cần dùng và thể tích khí cacbonic tạo thành. Biết các thể tích khí đo ở điều kiện chuẩn.
2) Để đốt cháy 4,958 lít khí etilen cần phải dùng:
a) Bao nhiêu lít ooxxi?
b) Bao nhiêu lít không khí chứa 20% thể tích oxi?
biết thể tích các khí đo ở điều kiện chuẩn.
Mình rất rất là cần gấp mấy bạn giúp mik lẹ nha
1)
$CH_4 +2 O_2 \xrightarrow{t^o} CO_2 + 2H_2O$
Theo PTHH :
$V_{O_2\ cần\ dùng} = 2V_{CH_4} = 24,79(lít)$
$V_{CO_2} = V_{CH_4} = 12,395(lít)$
2)
a)
$C_2H_4 + 3O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O$
$V_{O_2} = 3V_{C_2H_4} = 14,874(lít)$
b) $V_{không\ khí} = V_{O_2} : 20\% = 14,874 : 20\% = 74,37(lít)$
Đốt cháy 11,2 lít khí metan. Thể tích không khí cần dùng đế đốt cháy hết lượng metan trên là bao nhiêu (đktc)? Biết oxi chiếm 1/5 thể tích không khí. *
nCH4 =11,2/22,4 = 0,5 (mol)
PTHH CH4 + 2O2 -to-> CO2 + 2H2O
...........0,5.........1.............0,5............1
Vkk= 5. VO2 = 5. 22,4 .1 = 112 l
\(n_{CH_4}\)\(=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(CH_4+2O_2\xrightarrow[]{t^o}CO_2+2H_2O\)
\(0,5\) \(1\) \(\left(mol\right)\)
\(V_{O_2}=1.22,4=22,4\left(l\right)\)
\(V_{kk}=22,4:\dfrac{1}{5}=112\left(l\right)\)
Đốt cháy 6,72 lít khí metan (CH4) trong không khí . Tính thể tích không khí cần dùng để đốt cháy hết lượng metan trên ( biết rằng trong không khí oxi chiếm 21%)
nCH4 = 6,72/22,4 = 0,3 (mol)
PTHH: CH4 + 2O2 -> (t°) CO2 + 2H2O
Mol: 0,3 ---> 0,6
Vkk = 0,6 . 22,4 : 21% = 64 (l)
Đốt cháy hoàn toàn 4,48l khí metan a) viết pthh của phản ứng b) tính thể tích oxi tham gia phản ứng và thể tích khí cacbonic tạo thành c) tính thể tích k khí cần dùng để đốt cháy hết khí metan trên
nCH4 = 4,48/22,4 = 0,2 (mol)
PTHH: CH4 + 2O2 -> (t°) CO2 + 2H2O
Mol: 0,2 ---> 0,4 ---> 0,2 ---> 0,4
VO2 = 0,4 . 22,4 = 8,96 (l)
VCO2 = 0,2 . 22,4 = 4,48 (l)
Vkk = 8,96 . 5 = 44,8 (l)
a. \(n_{CH_4}=\dfrac{4.48}{22,4}=0,2\left(mol\right)\)
PTHH : CH4 + 2O2 ---to---> CO2 + 2H2O
0,2 0,4 0,2
b. \(V_{O_2}=0,4.22,4=8,96\left(l\right)\)
\(V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
c. \(V_{kk}=8,96.5=44,8\left(l\right)\)
Đốt cháy hoàn toàn 11,2 lít khí metan cần phải dùng: a/ Bao nhiêu lít khí oxi? b/ Bao nhiêu lít không khí chứa 20% thể tích oxi? (Thể tích các khí đo ở đktc)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
Ta có: \(n_{CH_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
a, Theo PT: \(n_{O_2}=2n_{CH_4}=1\left(mol\right)\)
\(\Rightarrow V_{O_2}=1.22,4=22,4\left(l\right)\)
b, \(V_{kk}=\dfrac{22,4}{20\%}=112\left(l\right)\)
Đốt cháy hoàn toàn 4,48 lít khí metan
a) viết phương trình hóa học của phản ứng
b) tính thể tích khí oxi tham gia phản ứng và thể tích khí cacbonic tạo thành
c) tính thể tích không khí cần dùng để đốt cháy hết lượng khí metan trên
a. \(n_{CH_4}=\dfrac{4.48}{22,4}=0,2\left(mol\right)\)
PTHH : CH4 + 2O2 ---t0---> CO2 + 2H2O
0,2 0,4 0,2
b. \(V_{O_2}=0,4.22,4=8,96\left(l\right)\)
\(V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
c. \(V_{kk}=8,96.5=44,8\left(l\right)\)
Khí metan CH4 có trong khí tự nhiên hoặc trong khí bioga. Khí metan cháy trong không khí sinh ra khí cacbon đioxit và nước:
CH4 + 2O2 → CO2 + 2H2O.
a) Tính thể tích khí oxi cần dùng để đốt cháy hoàn toàn 2 khí metan. Các thể tích khí đo cùng điều kiện to và p.
b) Tính thể tích khí CO2 (đktc) thu được sau khi đốt cháy hoàn toàn 0,15 mol khí metan.
c) Khí metan nặng hay nhẹ hơn không khí bằng bao nhiêu lần?
a) Theo phương trình hóa học, ta thấy nếu đốt cháy hết 1 mol phân tử khí CH4 thì phải cần 2 mol phân tử khí O2. Do đó thể tích khí oxi cần dùng để đốt cháy hoàn toàn 2 lít khí metan là:
VO2 = 2 . 2 = 4 lít.
b) Theo phương trình phản ứng, khi đốt cháy hoàn toàn 0,15 mol khí metan thì cũng sinh ra 0,15 mol khí cacbon đioxit. Do đó thể tích khí CO2 thu được là:
VCO2 = 0,15 . 22,4 = 3,36 lít.
c) Tỉ khối của khí metan và không khí là:
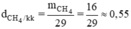
Vậy khí metan nhẹ hơn không khí 0,55.