Cân bằng phương trình:
M2(CO3)n+HNO3->M(NO3)m
+NO+CO2+H2O
Câu3:Có 13,38g chì Oxit đc nung nóng dưới dòng khí Hidro Sau p/ứng thu đc 12,58g chất rắn A.Tính tp % các chất trong A
Nung nóng mạng hh X gồm zn , feco3,mg(no3)2 (trong đó % Mg nhỏ hơn 40%) đến khối lượng không đổi thu đc chất rắn B gồm 2 oxit và 1.2 mol khí C gồmn2 khí có M=136/3 A) tính m B) hòa tan hoàn toàn A vào 1.82 mol hh vừa đủ HCl và hno3 thu đc hh E gồm NO2 , N2O và Co2 và dd D(bkhoong có fe2+). Để tác dụng tối đa các chất trong D cần 2.45bmol NaOH . Tính phần trăm các chất trong E
Có 11,15 gam chì oxit(M=223) được nung nóng dưới dòng khí hidro. Sau khi ngừng nung nóng, sản phẩm rắn A thu được có khối lượng là 10,38 gam. Tính thành phần khối lượng A
n pbo=11.15/223=0.05(mol)
pbo + h2----> pb + h2o
Gọi n pbo phản ứng là x
Chất rắn gồm pbo dư và pb
=) (0.05-x)223 + 207x=10.38
=) x=0.048 (xấp xỉ)
=) %m pb= 0.048*207/10.38=95.7%
=) %m pbo dư =100-95.7=4.3%
Có 11,15 gam chì oxit được nung nóng dưới dòng khí hidro. Sau khi ngừng nung nóng, sản phẩm rắn A thu được có khối lượng là 10,38 gam. Tính thành phần khối lượng A
Bạn check lại khối lượng của chì (II) oxit cho mình
có 11,15 gam chì oxit được nung nóng dưới dòng khí hidro. Sau khi ngừng nung nóng, sản phẩm rắn A thu được có khối lượng là 10,38 gam. Tính thành phần khối lượng A
PbO+H2--->Pb+H2O
a--------------->a
m O=11,15 - 10,3=0,77
--> n PbO phản ứng=0,048125
m PbO phản ứng=10,73
A có PbO và Pb
m PbO trong A=0,42 gam
m Pb=9,96 gam
Cho hơi nước đi qua than nóng đỏ thu đc hh khí A khô gồm CO,H2 và CO2. Cho A qua bình đựng dd Ba(OH)2 dư thu đc m g kết tủa . Khí còn lại cho từ từ qua ống đựng FeO nung nóng, sau phản ứng đc chất rắn B và khí C. Hoàn tan hết B bằng dd H2SO4 đặc nóng thấy thoát ra 1.456 lít khí SO2(đktc) và số mol H2SO4 đã phản ứng là 0.14 mol. Khí C được hấp thụ bằng dd Ca(OH)2 dư đc 1 g kết tủa. Biết H=100% a) tính khối lượng FeO ban đầu b) tính m và % theo thể tích các khí trong A
\(n_{SO2}=\dfrac{1,456}{22,4}=0.065\left(mol\right);n_{CaCO_3}=\dfrac{1}{100}=0,01\left(mol\right)\)
Ta có : PTHH
\(2Fe+6H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
Thấy \(n_{H_2SO_4}:n_{SO_2}=\dfrac{0,14}{6}>\dfrac{0,065}{3}\Rightarrow\) chất rắn B có FeO dư
PTHH \(2FeO+4H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+SO_2+4H_2O\)
Đặt số mol Fe và FeOdư lần lượt là a và b (a,b>0)
có \(\left\{{}\begin{matrix}3a+2b=0,14\\1,5a+0,5b=0,065\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,04\\b=0,01\end{matrix}\right.\)
\(\Rightarrow\sum n_{FeO}=n_{Fe}+n_{FeOdu}=0,05\left(mol\right)\) (bảo toàn nguyên tố Fe)
\(\Rightarrow m_{FeO}=0,05\times56=2,8\left(g\right)\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\) \(\Rightarrow n_{CO_2}=n_{CaCO_3}=0,01\left(mol\right)\)
\(FeO+CO\rightarrow Fe+CO_2\) \(\Rightarrow n_{CO}=n_{CO_2}=0,01mol\)
bạn xem lại đề bài nhé ý b không giải đc đâu
Giúp mh với, mh cần gấp =)))
nung nóng m g hỗn hợp Al và Fe3O4 trong điều kiện không có không khí. sau khi các phản ứng xảy ra hoàn toàn thu đc hh rắn X. Cho X td vs đ NaOH thu đc đ Y, chất rắn Z và 3,36l H2 đktc. Sục khí CO2 dư vào đ Y thu được 39 g kết tủa. Giá trị của M là?
8Al + 3Fe3O4 = 4Al2O3 + 9Fe (1)
Khi tác dụng với NaOH tạo khí H2 chứng tỏ Al dư và Fe3O4 hết (vì phản ứng xảy ra hoàn toàn).
Al + NaOH + H2O =NaAlO2 + 3/2H2 (2)
Al2O3 + 2NaOH = 2NaAlO2 + H2O (3)
Suy ra: nAl dư = 2/3nH2 = 0,1 mol.
CO2 + NaAlO2 + 2H2O = Al(OH)3 + NaHCO3 (4)
Số mol NaAlO2 = nAl(OH)3 = 39/78 = 0,5 mol.
Theo pt (2), (3) nAl2O3 = 1/2(0,5 - nAl) = 0,2 mol.
Theo (1): nAl = 2nAl2O3 = 0,4 mol, nFe3O4 = 3/4nAl2O3 = 0,15 mol.
Vậy: nAl ban đầu = 0,4 + 0,1 = 0,5 mol.
Do đó: m = 0,5.27 + 0,15.232 = 48,3 g.
NÂNG CAO
Thổi khí CO đi qua ống sứ đựng m gam Fe2O3 nung nóng. Sau phản ứng thu được 10,88 gam chất rắn A gồm 4 chất và 2,668l khí CO2 ( đktc )
a) Tính m
b) Lấy 1/10 lượng CO2 ở trên cho vào 0,4l Ca(OH)2 thu đc 0,2g kết tủa và khi nung nóng đ tạo thành ktủa lại tăng thêm p gam. Tính nồng độ mol của dd Ca(OH)2 và p
a: \(CO+Fe_2O_3\rightarrow A+CO_2\)
\(n_{CO}=n_{CO_2}=\dfrac{2.668}{22.4}=0.12\left(mol\right)\)
m Fe2O3=mA+mCO2-mCO=12,8(g)
\(n_{Ca\left(OH\right)_2}=0.1\left(mol\right)\)
=>Tỉ lệ \(\dfrac{n_{Ca\left(OH\right)_2}}{n_{CO_2}}=\dfrac{0.1}{0.12}>1\)
=>Tạo 2 muối, có kết tủa
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
a a a
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\)
2b b b
Theo đề, ta có hệ:
a+2b=0,12 và a+b=0,1
=>a=0,08 và b=0,02
=>m CaCO3=8(g)
Nung nóng m gam hỗn hợp gồm Al và CuO trong điều kiện không có không khí. Cho chất rắn sau phản ứng vào dung dịch NaOH (dư) thu được 672 ml khí H2 và chất rắn X. Hoà tan hết X trong dung dịch HNO3 loãng (dư) thấy có 448 ml khí NO (các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở đktc. m là
A. 2,94
B. 3,48
C. 34,80
D. 29,40
Đáp án B
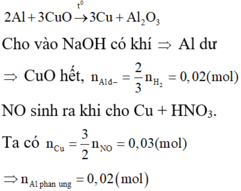
Hỗn hợp đầu gồm 0,04 mol Al và 0,03 mol CuO
1. Nêu khái niệm, định nghĩa về oxit, sự oxi hóa, 3 loại phản ứng đã học. CHO VD 2. Nêu nguyên liệu điều chế oxi, hidro trong PTN. Viết PTHH minh họa 3. Nung nóng hoàn toàn49g kaliclorat có xúc tác mangandioxit, sau phản ứng thu đc m g chất rắn và V lít khí(dktc). Tính giá trị của m, v
1,
- Oxit là hợp chất của hai nguyên tố, trong đó có một nguyên tố là oxi
Ví dụ: CO2, SO2, CuO,...
- Sự tác dụng của oxi với một chất là sự oxi hóa
Ví dụ: Sắt tác dụng với oxi => sắt bị oxi hóa
2,
- Nguyên liệu để điều chế Oxi trong phòng thí nghiệm là: K