1/Cần bao nhiêu gam Oxi để đốt cháy hoàn toàn:
+ 5mol Cacbon
+ 5mol Lưu huỳnh
2/ Trong giờ thực hành thí nghiệm, một HS đốt cháy 3,2g lưu huỳnh trong 1,12 lít Oxi (đktc). Vậy theo em lưu huỳnh cháy hết hay còn dư.
Trong giờ thực hành thí nghiệm, một em học sinh đốt cháy 3,2g lưu huỳnh trong 1,12 lit oxi (đktc). Vậy theo em lưu huỳnh cháy hết hay còn dư?
Cần bao nhiêu gam oxi để đốt cháy hoàn toàn 5 mol cacbon? 5mol lưu huỳnh?
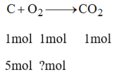
Số mol O 2 :
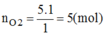
Khối lượng O 2 :
m O 2 = n O 2 . M O 2 = 5.32 = 160(g)
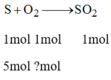
Số mol O 2 :
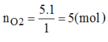
Khối lượng O 2 :
m O 2 = n O 2 . M O 2 = 5.32 = 160(g)
a) Cần bao nhiêu gam khí oxi để đốt cháy hoàn toàn 3 mol cacbon? 5mol lưu huỳnh?
b) Trong giờ thực hành thí nghiệm, một học sinh đốt cháy 3,2gam lưu huỳnh trong 1,12 lít khí oxi (đktc). Vậy theo em lưu huỳnh cháy hết hay còn dư?
a/ Cần bao nhiêu gam oxi để đốt cháy hoàn toàn 5 mol cacbon? 5 mol lưu huỳnh?
b/ Trong giờ thực hành thí nghiệm, một em học sinh đốt cháy 3,2g lưu huỳnh trong 1,12 lít oxi (đktc). Vậy theo em, chất nào còn dư và dư bao nhiêu gam?
a/ Cần bao nhiêu gam oxi để đốt cháy hoàn toàn 5 mol cacbon? 5 mol lưu huỳnh?
b/ Trong giờ thực hành thí nghiệm, một em học sinh đốt cháy 3,2g lưu huỳnh trong 1,12 lít oxi (đktc). Vậy theo em, chất nào còn dư và dư bao nhiêu gam?
a, PTHH: C + O2 ➝ CO2
Theo pt: 1 1 1 (mol)
Theo bài ra: 5 → 5 (mol)
⇒mO2= 5x32= 160(g)
PTHH: S + O2 ➞ SO2
Theo pt: 1 1 1 (mol)
Theo bài ra: 5 → 5 (mol)
⇔mO2= 5x32=160(g)
b, nO2= 1,12/22,4=0,05(mol)→mO2=1,6(g)
PTHH: S + O2 ➝ SO2
Theo pt: 32 32 64 (g)
Theo bài ra: 3,2 1,6 (g)
Phản ứng: dư hết
⇒mS dư = 3,2 - 1,6=1,6(g)
Vậy lưu huỳnh dư và dư 1,6g
TICK CHO MIK NHOA!!!
a, \(C+O_2\underrightarrow{^{to}}CO_2\)
\(n_{O2}=5\left(mol\right)\rightarrow m_2=160\left(g\right)\)
\(S+O_2\underrightarrow{^{to}}SO_2\)
\(n_{O2}=5\left(mol\right)\rightarrow m_{O2}=160\left(g\right)\)
b, \(n_S=0,1\left(mol\right);n_{O2}=0,05\left(mol\right)\)
Nên S dư 0,05 (mol) \(\rightarrow m_{S_{du}}=1,6\left(g\right)\)
a) C+ O2 -to-> CO2
5_____5
mO2 = 5 * 32 = 160 g
S + O2 -to-> SO2
5___5
mO2 = 5 * 32 = 160 g
b) nS = 0.1 mol
nO2 = 0.05 mol
S + O2 -to-> SO2
0.1__0.05
LTL : 0.1/1 > 0.05/1 => S dư
mS dư = 0.05*32 = 1.6 g
a/ Cần bao nhiêu gam oxi để đốt cháy hoàn toàn 5 mol cacbon? 5 mol lưu huỳnh?
b/ Trong giờ thực hành thí nghiệm, một em học sinh đốt cháy 3,2g lưu huỳnh trong 1,12 lít oxi (đktc). Vậy theo em, chất nào còn dư và dư bao nhiêu gam?
Đốt chày hoàn toàn 9,6g lưu huỳnh trong lọ chưa khí Oxi
a) Tính khối lượng KClO₃ cần dùng để điểu chế khí Oxi cần dùng cho thí nghiệm trên
b) Nếu đốt cháy lượng lưu huỳnh trong bình chứa không khí thì phải cần bao nhiêu lít không khí ở đktc
\(a,PTHH:S+O_2\underrightarrow{t^o}SO_2\left(1\right)\)
\(n_S=\dfrac{m}{M}=\dfrac{9,6}{32}=0,3\left(mol\right)\)
\(Theo.PTHH\left(1\right):n_O=n_S=0,3\left(mol\right)\)
\(PTHH:2KClO_3\underrightarrow{t^o}2KCl+3O_2\\ Theo.PTHH\left(2\right):n_{KClO_3}=\dfrac{2}{3}.n_{O_2}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ m_{KClO_3}=n.M=0,2.122,5=24,5\left(g\right)\)
\(b,V_{O_2\left(đktc\right)}=n.22,4=0,2.22,4=4,48\left(l\right)\\ \Rightarrow V_{kk\left(đktc\right)}=5.V_{O_2}=5.4,48=22,4\left(l\right)\)
Bài 1: Đốt cháy 3,2g lưu huỳnh trong bình chứa 1,121khí oxi (đktc).
a/ Lưu huỳnh hay oxi, chất nào còn dư và dư bao nhiêu gam hoặc lít?
b/ Tính khối lượng khí sunfurơ tạo thành?
nS=mS/MS=3,2/32=0,1(mol)
nO2=VO2/22,4=32/22,4=1,42(mol)
PTHH: S + O2 --> SO2 (1)
BĐ: 0,1 1,42
PỨ: 0,1-->0,1-->0,1
SPỨ: 0--->0,32-->0,1
a) Từ PT(1)=>O2 dư
VO2(dư)=nO2(dư) .22,4=0,32 .22,4=7,168(l)
b) Từ PT(1)=>nSO2=0,1(mol)
=>mSO2=n.M=0,1 .64=6,4(g)
Đốt cháy hoàn toàn 12 gam hỗn hợp bột lưu huỳnh và cacbon trong không khí thu được 28 gam hỗn hợp khí lưu huỳnh đioxit và cacbon đioxit. Thể tích oxi (ở đktc) cần dùng trong phản ứng trên là .
Gọi nC = a (mol); nS = b (mol)
12a + 32b = 12 (1)
PTHH:
C + O2 -> (t°) CO2
a ---> a ---> a
S + O2 -> (t°) SO2
b ---> b ---> b
44a + 64b = 28 (2)
Từ (1)(2) => a = 0,2 (mol); b = 0,3 (mol)
nO2 = 0,2 + 0,3 = 0,5 (mol)
VO2 = 0,5 . 22,4 = 11,2 (l)