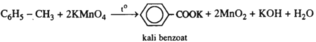
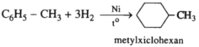Giúp mih câu này ạ hoá lớp 7 bài 7 tính theo công thức hoá học và phương trình hoá học theo chương trình mới khtn trang 56

Những câu hỏi liên quan
Câu 1: Khi đốt cháy một loại gluxit ( công thức chung Cn(H2O)m) thu được khối lượng nước và CO2 theo tì lệ : 33: 88. Xác định công thức của gluxit trên
Câu 2: Viết các phương trình hoá học thực hiện dãy chuyển đổi hoá học sau:
a) Tinh bột (1) Glucozơ (2) Rượu etylic (3) Axit axetic (4) Etyl axetat
(5) (6)...
Đọc tiếp
Câu 1: Khi đốt cháy một loại gluxit ( công thức chung Cn(H2O)m) thu được khối lượng nước và CO2 theo tì lệ : 33: 88. Xác định công thức của gluxit trên Câu 2: Viết các phương trình hoá học thực hiện dãy chuyển đổi hoá học sau: a) Tinh bột (1) Glucozơ (2) Rượu etylic (3) Axit axetic (4) Etyl axetat (5) (6) Natrietylat Canxiaxetat b) Saccarozo (1) Glucozơ (2) Ancol etylic (3) Etyl axetat (4)Natri axetat
Câu 1 :
Coi n gluxit = 1(mol)
Bảo toàn nguyên tố với C,H .Ta có :
n CO2 = n(mol)
n H2O = m(mol)
Suy ra :
18m/44n= 33/88
<=> m/n = 11/12
Với m = 11 ; n = 12 thì thỏa mãn
Vật CT của gluxit là C12(H2O)11 hay C12H22O11
Đúng 1
Bình luận (1)
Câu 2 :
a)
\((1) C_6H_{12}O_6 \xrightarrow{t^o,xt} 2CO_2 + 2C_2H_5OH\\ (2) C_2H_5OH + O_2 \xrightarrow{men\ giấm} CH_3COOH + H_2O\\ (3) CH_3COOH + C_2H_5OH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_3COOC_2H_5 + H_2O\\ (5)CH_3COO_2H_5 + NaOH \to CH_3COONa + C_2H_5OH\\ (6) 2C_2H_5OH + 2Na \to 2C_2H_5ONa + H_2\)
b)
\((1)C_{12}H_{22}O_{11} + H_2O \xrightarrow{t^o,H^+} C_6H_{12}O_6 + C_6H_{12}O_6\\ (2)C_6H_{12}O_6 \xrightarrow{t^o,xt} 2CO_2 + 2C_2H_5OH\\ (3)C_2H_5OH + CH_3COOH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_3COOC_2H_5 + H_2O\\ (4)CH_3COOC_2H_5 + NaOH \to CH_3COONa + C_2H_5OH\)
Đúng 1
Bình luận (0)
các bạn giúp mik câu 8 9 10 ở trên dạng 7 với
chủ đề là viết và tính theo công thức hoá học

8) PTK của \(Cu\left(NO_3\right)_x=188\) đvC
\(\Leftrightarrow64+\left(14+3.16\right).x=188\)
\(\Leftrightarrow x=2\)
9) PTK của \(K_xPO_4=203\) đvC
\(\Leftrightarrow39.x+31+4.16=203\)
\(\Leftrightarrow x=...\)
-> Xem lại đề bài câu này, 212 mới đúng
10) PTK của \(Al\left(NO_3\right)_x=213\) đvC
\(\Leftrightarrow27+\left(14+3.16\right).x=213\)
\(\Leftrightarrow x=3\)
Đúng 2
Bình luận (0)
Chất hữu cơ X khi đốt cháy tuân theo phương trình hoá học :
aX + 3 O 2 → 2C O 2 + 2 H 2 O
Hãy xác định công thức phân tử của X và viết phương trình hoá học. Biết a là số nguyên, dương.
Áp dụng nguyên tắc bảo toàn đối với nguyên tố oxi => trong X không có oxi. Vậy X là hiđrocacbon, có công thức phân tử C n H m . Từ phương trình hoá học của phản ứng cháy, ta có :
=> an = 2; am = 4
Nếu a = 1 thì n = 2; m = 4 → C 2 H 4 (phù hợp)
Nếu a = 2 thì n = 1; m = 2 → CH 2 ( không phù hợp)
Vậy công thức phân tử của X là C 2 H 4
Đúng 0
Bình luận (0)
Nhôm hiđrôxit có thể tồn tại ở dạng axit và bazơ. Viết công thức hoá học của 2 dạng này, viết phương trình hoá học thể hiện tính axit và bazơ của nhôm hiđrôxit
Dạng axit - bazơ của nhôm hiđrôxit:
Al(OH)3 -→ HAlO2.H2O
Dạng Bazơ - Dạng axit( Axit aluminic )
PTHH: Al(OH)3 + NaOH → NaAlO2 + 2H2O
Axit - Bazơ
Al(OH)3 + 3HCl → AlCl3 + 3H2O
Bazơ - Axit
Đúng 0
Bình luận (0)
giúp mik câu 4 và 5 với
chủ đề là tính theo công thức hoá học

4) \(M_{NH_3}=8,5.2=17\) g/mol
mN = 17.82,35% = 14 (g)
mH = 17 - 14 = 3 (g)
\(n_N=\dfrac{14}{14}=1\left(mol\right)\)
\(n_H=\dfrac{3}{1}=3\left(mol\right)\)
=> Trong 1 mol phân tử có 1 mol nguyên tử N và 3 mol nguyên tử H
=> \(NH_3\)
Đúng 2
Bình luận (0)
Câu 4 :
Ta có : MX = \(M_{H_2}.8.5=17\) (g/mol)
Có N chiếm 82.35% , H chiếm 17.65%
Nên khối lượng của mỗi nguyên tố có trong 1 mol hợp chất là
mN = \(\dfrac{17.82,35}{100}=13.995\left(g\right)\)
=> mH = mX - mN = 3.005 (g)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất là
nN = \(\dfrac{13.995}{23}\approx0.6\left(mol\right)\)
nH = \(\dfrac{3.005}{1}\approx3\left(mol\right)\)
=> CTHH của hợp chất X là NH3
Câu 5:
a) MX = 2.207 x 29 = 64.003 \(\approx64\left(đvC\right)\)
b) Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất là
mS = \(\dfrac{64.50}{100}=32\left(g\right)\)
mO = 64 - 32 = 32 (g)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất là
nS = \(\dfrac{32}{32}=1\left(mol\right)\)
nO = \(\dfrac{32}{16}=2\left(mol\right)\)
=> CTHH của hợp chất X là \(SO_2\)
Đúng 2
Bình luận (0)
5)
a) \(M_X=2,207.29\approx64\) (g/mol)
b) \(m_S=50\%.64=32\left(g\right)\)
\(m_O=64-32=32\left(g\right)\)
\(n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> \(SO_2\)
Đúng 2
Bình luận (0)
Trong công nghiệp, amoniac được điều chế từ nitơ và hiđro bằng phương pháp tổng hợp theo phương trình hoá học sau: N2(k) + 3H2(k) ⇌ 2NH3(k) DH 0 Để cân bằng hoá học trên chuyển dịch theo chiều thuân ta phải A. Giảm nhiệt độ, tăng áp suất B. Tăng nhiệt độ, giảm áp suất C. Giảm nhiệt độ, giảm áp suất D. Tăng nhiệt độ, tăng áp suấ
Đọc tiếp
Trong công nghiệp, amoniac được điều chế từ nitơ và hiđro bằng phương pháp tổng hợp theo phương trình hoá học sau: N2(k) + 3H2(k) ⇌ 2NH3(k) DH <0
Để cân bằng hoá học trên chuyển dịch theo chiều thuân ta phải
A. Giảm nhiệt độ, tăng áp suất
B. Tăng nhiệt độ, giảm áp suất
C. Giảm nhiệt độ, giảm áp suất
D. Tăng nhiệt độ, tăng áp suấ
Câu 9:Cho các chất có công thức hoá học sau:K,MgO,Na2O,SO3a.Chất nào tác dụng được với nước?b.Viết các phương trình hoá học xảy ra?Câu 10:Phân loại và gọi tên các hợp chất có công thức hoá học sau:Mg(OH)2,NaCl,H2SO4,Ca(HCO3)2Câu 11:Khí oxi trong không khí là đơn chất hay hợp chất?Vì sao cá sống được trong nước?Những lĩnh vực hoạt động nào của con người cần thiết phải dùng bình nén oxi để hô hấp?Câu 12:Cho 4,8 gam kim loại magie phản ứng hoàn toàn với dung dịch axit clohidric(HCl),sau phản ứng th...
Đọc tiếp
Câu 9:Cho các chất có công thức hoá học sau:K,MgO,Na2O,SO3
a.Chất nào tác dụng được với nước?
b.Viết các phương trình hoá học xảy ra?
Câu 10:Phân loại và gọi tên các hợp chất có công thức hoá học sau:Mg(OH)2,NaCl,H2SO4,Ca(HCO3)2
Câu 11:Khí oxi trong không khí là đơn chất hay hợp chất?Vì sao cá sống được trong nước?Những lĩnh vực hoạt động nào của con người cần thiết phải dùng bình nén oxi để hô hấp?
Câu 12:Cho 4,8 gam kim loại magie phản ứng hoàn toàn với dung dịch axit clohidric(HCl),sau phản ứng thu được muối magie clorua và khí Hidro
a.Viết phương trình hoá học xảy ra?
b.Tính thể tích khí Hidro sinh ra(ở đktc)
c.Nếu đốt cháy toàn bộ lượng khí Hidro sinh ra ở trên trong không khí.Tính thể tích không khí cần dùng?(Biết Vkk=5.Vo2)
Câu 9:
\(a,K,Na_2O,SO_3\\ b,K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\\ Na_2O+H_2O\rightarrow2NaOH\\ SO_3+H_2O\rightarrow H_2SO_4\)
Câu 10:
Mg(OH)2 - bazo - magie hidroxit
NaCl - muối - natri clorua
H2SO4 - axit - axit sunfuric
Ca(HCO3)2 - muối - canxi hidrocacbonat
Câu 11:
- Khí oxi là đơn chất
- Vì trong nước có cả khí oxi
- Dùng trong lĩnh vực y học, ...
Câu 12:
\(a,n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2--------------------------->0,2
b, VH2 = 0,2.22,4 = 4,48 (l)
c, PTHH: \(2H_2+O_2\xrightarrow[]{t^o}2H_2O\)
0,2-->0,1
=> Vkk = 0,1.22,4.5 = 11,2 (l)
Đúng 5
Bình luận (0)
9
a) K , Na2O , SO3 là những chất td với H2O
b)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\\
Na_2O+H_2O\rightarrow2NaOH\\
SO_3+H_2O\rightarrow H_2SO_4\)
10
Mg(OH)2 -Magie hidroxit - bazo
NaCl - natri clorua - muối
H2SO4 - axit sunfuric - axit
Ca(HCO3)2 - canxi hidrocacbonat - muối
11
a)đơn chất
b) vì trong nước có chứa nguyên tử Oxi
c) Thợ lặn
12
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\
pthh:Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,2
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\\
pthh:2H_2+O_2\underrightarrow{t^o}2H_2O\)
0,2 0,1
\(V_{KK}=\left(0,1.22,4\right).5=11,2\left(l\right)\)
Đúng 2
Bình luận (1)
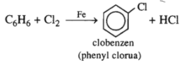
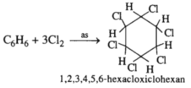
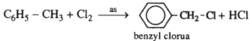
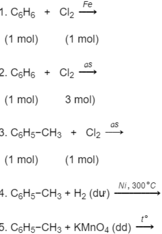
Hoàn thành các phương trình hoá học dưới đây. Viết các chất sản phẩm hữu cơ ở dạng công thức cấu tạo và kèm theo tên.
Ở TRONG TRANG NÀY KHÔNG CÓ BÁI GIẢNG CỦA MÔN KHOA HỌC TỰ NHIÊN 6, BỘ SÁCH CHÂN TRỜI SÁNG TẠO VÀ Ở MÔN HỌC CŨNG KHÔNG CÓ MÔN KHAO HỌC TỰ NHIÊN, TRONG MÔN HỌC KHÔNG CÓ MÔN HOÁ HỌC MÀ TRONG MÔN HỌC KHTN 6 CÓ CẢ BÀI VỀ KIẾN THỨC HOÁ HỌC NỮA.. VẬY NHỮNG GIÁO VIÊN DẠY MÔN KHTN ĐĂNG KÝ DẠY NHƯ NÀO VÌ