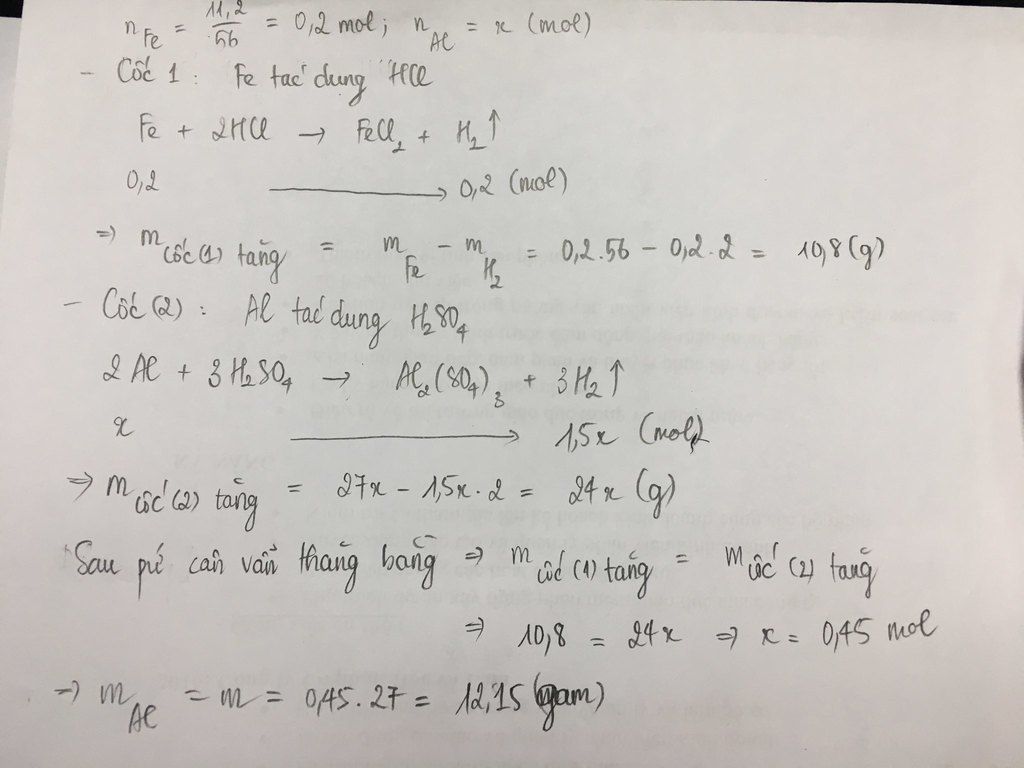tại sao người ta có thể dùng các thùng bằng Al hoặc Fe để đựng H2SO4 đặc mà không dùng để đựng dung dịch H2SO4 loãng

Những câu hỏi liên quan
Câu 7: Trình bày phương pháp nhận biết các dãy chất đựng trong các lọ riêng biệt sau :
a) Na, Al, Mg.
b) Na, Ca, Al, Fe (chỉ dùng nước).
c) Có các mẫu chất rắn riêng biệt: Ba, Mg, Fe, Al, MgO, Al2O3, Fe2O3, Ag. Chỉ dùng thêm dung dịch H2SO4 loãng có thể nhận ra nhiều nhất bao nhiêu chất
trong số các chất trên ?
d) Mg, Zn, Fe, Ba (chỉ dùng một thuốc thử) e) Fe, (Fe + FeO), (FeO + Fe2O3)
Đặt cốc A đựng dung dịch HCl và cốc B đựng dung dịch H2SO4 loãng vào 2 đĩa cân sao cho cân ở vị trí cân bằng. Sau đó làm thí nghiệm như sau:
Cho 11,2g Fe vào cốc đựng dung dịch HCl.
Cho m gam Al vào cốc đựng dung dịch H2SO4.
Khi cả Fe và Al đều tan hoàn toàn thấy cân ở vị trí thăng bằng. Tính m?
\(Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = n_{Fe} = \dfrac{11,2}{56} =0,2(mol)\\ \Rightarrow m_{tăng} = 11,2 - 0,2.2 = 10,8(gam)\\ 2Al +3 H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\\ n_{Al} = \dfrac{m}{27}(mol)\\ \Rightarrow n_{H_2} = \dfrac{3}{2}n_{Al} = \dfrac{m}{18}(mol)\)
Vì cân ở vị trí thăng bằng nên :
\(m - \dfrac{m}{18}.2 = 10,8\Rightarrow m =12,15(gam)\)
Đúng 3
Bình luận (0)
Câu 12: Để phân biệt hai lọ đựng chất khí mất nhãn đựng SO2 hoặc O2 ta không thể dùngthuốc thử làA. dung dịch Ca(OH)2. B. quỳ tím ẩm C. tàn đóm đỏ D. dung dịch H2SO4Câu 13: Để phân biệt hai lọ đựng dung dịch HCl và H2SO4 mất nhãn ta dùng thuốc thử nàosau đây?A. Quỳ tím. B. H2O. C. dung dịch BaCl2 D. Zn.Câu 14: Để thu được khí O2 từ hỗn hợp khí CO2 và O2 ta sục hỗn hợp khí trên vào dung dịchA. Ca(OH)2 dư. B. HCl dư. C. H2O dư. D. dung dịch Na2SO4 dư.Câu 15: Có những chất sau: CO2, H2O, KOH, K2O....
Đọc tiếp
Câu 12: Để phân biệt hai lọ đựng chất khí mất nhãn đựng SO2 hoặc O2 ta không thể dùng
thuốc thử là
A. dung dịch Ca(OH)2. B. quỳ tím ẩm C. tàn đóm đỏ D. dung dịch H2SO4
Câu 13: Để phân biệt hai lọ đựng dung dịch HCl và H2SO4 mất nhãn ta dùng thuốc thử nào
sau đây?
A. Quỳ tím. B. H2O. C. dung dịch BaCl2 D. Zn.
Câu 14: Để thu được khí O2 từ hỗn hợp khí CO2 và O2 ta sục hỗn hợp khí trên vào dung dịch
A. Ca(OH)2 dư. B. HCl dư. C. H2O dư. D. dung dịch Na2SO4 dư.
Câu 15: Có những chất sau: CO2, H2O, KOH, K2O. Số cặp chất có thể tác dụng với nhau là
A. 1. B. 2. C. 3. D. 4.
Câu 16: Cho 2,24 lít khí CO2 (ở đktc) tác dụng vừa đủ với 100 ml dung dịch KOH tạo thành
muối K2CO3. Nồng độ mol/l của dung dịch KOH là:
A. 1,5 M B. 2M C. 1M D. 3M
Câu 17:. Axit sunfuric đặc, dư tác dụng với 10 gam hỗn hợp CuO và Cu thì thu được 2,24
lít khí (đktc). Khối lượng ( gam) của CuO và Cu trong hỗn hợp lần lượt là:
A. 3,6 và 6,4 B. 6,8 và 3,2
C. 0,4 và 9,6 D. 4,0 và 6,0
Câu 18: Để hòa tan hết m gam Zn cần vừa đủ 200 ml dung dịch H2SO4 1M. Giá trị của m
làA. 6,5. B. 13,0. C. 19,5. D. 26,0.
Câu 19: Trộn 100 gam dung dịch NaOH 10% với 150 gam dung dịch HCl 7,3% thu được
dung dịch X chứa chất tan Y. Chất Y làm đổi màu quỳ tím. Nồng độ C% của Y trong dung
dịch X là
A. 7,3%. B. 0,73%. C. 1,46%. D. 2,19%.
Câu 20: Để hòa tan hết 10 gam hỗn hợp hai oxit CuO và Fe2O3 cần dùng 100 ml dung dịch
HCl có nồng độ 3,5M. Khối lượng của CuO và Fe2O3 có trong hỗn hợp ban đầu lần lượt là
A. 3 gam, 7 gam B. 8 gam, 2 gam C. 2 gam, 8 gam D. 4 gam, 6 gam
Câu 35: Có 3 lọ đựng 3 chất riêng biệt Fe, Al, Al2O3 để nhận biết chất rắn trong từng lọ chỉ dùng 1 thuốc thử là:😶 a.Nước 😶B. Dung dịch HCl 😶C. Dung dịch KOH 😶D. Dung dịch H2SO4 loãng😶( nếu được mọi người chỉ mình cách nhận biết vớiiii )
C
- Cho 3 chất rắn tác dụng với dd KOH
+ Chất rắn tan, sủi bọt khí: Al
2Al + 2KOH + 2H2O --> 2KAlO2 + 3H2
+ Chất rắn tan, không sủi bọt khí: Al2O3
Al2O3 + 2KOH --> 2KAlO2 + H2O
+ Chất rắn không tan: Fe
Đúng 2
Bình luận (0)
Để phân biệt các dung dịch không màu đựng trong các lọ riêng biệt sau: H2SO4, NaOH, HCl, người ta dùng?
- Trích mẫu thử
- Cho quỳ tím vào các mẫu thử:
+ Nếu quỳ tím hóa đỏ là H2SO4 và HCl
+ Nếu quỳ tím hóa xanh là NaOH
- Cho BaCl2 vào 2 mẫu thử còn lại:
+ Nếu có kết tủa trắng là H2SO4
\(BaCl_2+H_2SO_4--->BaSO_4\downarrow+2HCl\)
+ Nếu không có hiện tượng là HCl.
Đúng 1
Bình luận (0)
+ NaOH làm quỳ chuyển màu xanh
+ H2SO4, HCl làm quỳ chuyển màu đỏ
Dùng BaCl2 nhận 2 dung dịch axit:
+ Có kết tủa trắng là H2SO4
H2SO4 + BaCl2 → BaSO4 +2HCl
+ Không có hiện tượng gì là HCl
Đúng 0
Bình luận (1)
Cho các phát biểu sau: (1) Để làm sạch lớp cặn trong các dụng cụ đun và chứa nước nóng, người ta dùng giấm ăn. (2) Cho CrO vào dung dịch KOH dư tạo ra K2Cr2O7. (3) Cho bột Al dư vào dung dịch FeCl3 đến phản ứng hoàn toàn thu được dung dịch chứa AlCl và FeCl2. (4) Có thể dùng thùng bằng Al, Fe, Cr để vận chuyển các axit H2SO4 đặc, nguội hoặc HNO3 đặc, nguội. (5) Cho Ba vào dung dịch CuSO4 thì giải phóng ra kim loại Cu. (6) Cho CrO3 vào nước thu được hỗn hợp axit. (7) Nước cứng làm hỏng các...
Đọc tiếp
Cho các phát biểu sau:
(1) Để làm sạch lớp cặn trong các dụng cụ đun và chứa nước nóng, người ta dùng giấm ăn.
(2) Cho CrO vào dung dịch KOH dư tạo ra K2Cr2O7.
(3) Cho bột Al dư vào dung dịch FeCl3 đến phản ứng hoàn toàn thu được dung dịch chứa AlCl và FeCl2.
(4) Có thể dùng thùng bằng Al, Fe, Cr để vận chuyển các axit H2SO4 đặc, nguội hoặc HNO3 đặc, nguội.
(5) Cho Ba vào dung dịch CuSO4 thì giải phóng ra kim loại Cu.
(6) Cho CrO3 vào nước thu được hỗn hợp axit.
(7) Nước cứng làm hỏng các dung dịch pha chế.
(8) Hợp kim K và Na dùng làm chất làm chậm trong lò phản ứng hạt nhân.
Số phát biểu đúng là:
A. 6
B. 3
C. 4
D. 5
Chọn C.
Các phát biểu đúng: 1, 4, 6, 7.
+ Cho CrO3 vào dung dịch KOH dư tạo ra K2CrO4.
+ Cho bột Al dư vào dung dịch FeCl3 đến phản ứng hoàn toàn thu được dung dịch chứa AlCl3.
+ Cho Ba vào dung dịch CuSO4 thì giải phóng ra H2 và cho kết tủa BaSO4; Cu(OH)2
Đúng 0
Bình luận (0)
Câu 7: Trình bày phương pháp nhận biết các dãy chất đựng trong các lọ riêng biệt sau :
a) Na, Al, Mg. b) Na, Ca, Al, Fe (chỉ dùng nước).
c) Có các mẫu chất rắn riêng biệt: Ba, Mg, Fe, Al, MgO, Al2O3, Fe2O3, Ag. Chỉ dùng thêm dung dịch H2SO4 loãng có thể nhận ra nhiều nhất bao nhiêu chất
trong số các chất trên ?
d) Mg, Zn, Fe, Ba (chỉ dùng một thuốc thử) e) Fe, (Fe + FeO), (FeO + Fe2O3)
a.
- Trích mẫu thử
- Cho nước vào các mẫu thử:
+ Nếu tan và có khí bay ra là Na
\(2Na+2H_2O--->2NaOH+H_2\)
+ Không tan là Al và Mg
- Cho NaOH vừa thu được sau phản ứng của Na và H2O vào 2 mẫu thử còn lại:
+ Nếu tan và có khí thoát ra là Al
\(Al+NaOH+H_2O--->NaAlO_2+\dfrac{3}{2}H_2\)
+ Không có hiện tượng là Mg
Đúng 2
Bình luận (0)
Đặt cốc A đựng dung dịch HCl và cốc B đựng dung dịch H2SO4 loãng vào 2 đĩa cân sao cho cân ở vị trí cân bằng. Sau đó làm thí nghiệm như sau:
- Cho 11,2g Fe vào cốc đựng dung dịch HCl.
- Cho m gam Al vào cốc đựng dung dịch H2SO4.
Khi cả Fe và Al đều tan hoàn toàn thấy cân ở vị trí thăng bằng. Tính m?
\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 0,2
\(\Rightarrow m_{Fe}+m_{H_2SO_4}=0,2\cdot56+0,2\cdot98=30,8g\)
Cả hai đĩa cân thăng bằng:
\(m_{Fe}+m_{H_2SO_4}=m_{Al}+m_{H_2SO_4}\)
\(\Rightarrow m_{Fe}=m_{Al}=11,2g\)
Đúng 3
Bình luận (0)
Bài 1. Đặt cốc A đựng dung dịch HCl và cốc B đựng dung dịch H2SO4 loãng vào 2 đĩa cân sao cho cân ở vị trí cân bằng. Sau đó làm thí nghiệm như sau:
Cho 11,2g Fe vào cốc đựng dung dịch HCl.
Cho m gam Al vào cốc đựng dung dịch H2SO4.
Khi cả Fe và Al đều tan hoàn toàn thấy cân ở vị trí thăng bằng. Tính m?
Xem chi tiết