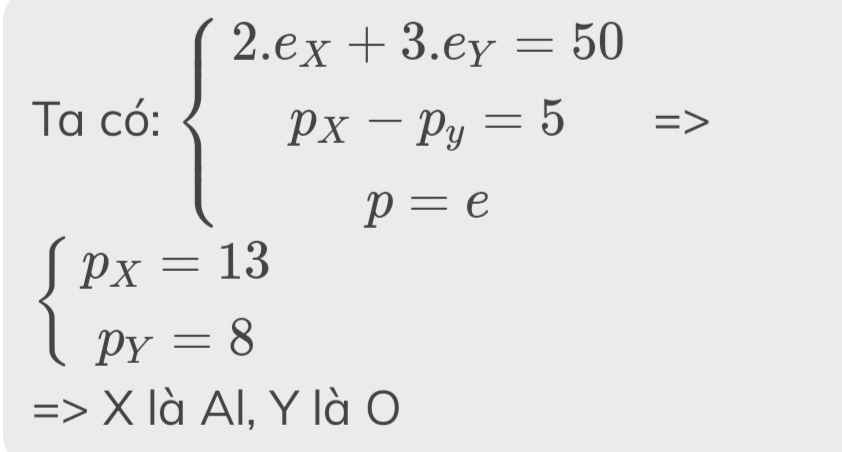Phân tử X2Y3 có tổng số hạt electron là 50 ,số e trong nguyên tử X nhiều hơn trong nguyên tử Y là 5. Xác định số hiệu nguyên tử, viết cấu hình e của X , Y và sự phân bố theo obitan

Những câu hỏi liên quan
Phân tử X2Y3 có tổng số hạt electron là 50, số e trong ngtử X nhiều hơn trong ngtử Y là 5. Xác định số hiệu ngtử, viết cấu hình e của X, Y và sự phân bố theo obitan ?
Ta có : \(\left\{{}\begin{matrix}2Z_X+3Z_Y=50\\Z_X-Z_Y=5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}Z_X=13\left(Al\right)\\Z_Y=8\left(O\right)\end{matrix}\right.\)
=> CHe của X \(1s^22s^22p^63s^23p^1\)
CHe của Y : \(1s^22s^22p^4\)
Đúng 1
Bình luận (0)
Câu 1: Nguyên tử của nguyên tố X có tổng số hạt electron trong các phân lớp p là 7. Số hạt mang điện của 1 nguyên tử Y nhiều hơn số hạt mang điện của 1 nguyên tử X là 8 hạt.
a) Viết cấu hình electron nguyên tử cua X,Y
b) Xác định vị trí X,Y trong bảng tuần hoàn
Câu 2: Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là ns^2np^3. Trong hợp chất khí của nguyên tố X với hiđro, X chiếm 91,18% khối lượng
a) Xác định nguyên tố X
b) Tính % khối lượng của nguyên tố X trong oxit cao nhấ...
Đọc tiếp
Câu 1: Nguyên tử của nguyên tố X có tổng số hạt electron trong các phân lớp p là 7. Số hạt mang điện của 1 nguyên tử Y nhiều hơn số hạt mang điện của 1 nguyên tử X là 8 hạt.
a) Viết cấu hình electron nguyên tử cua X,Y
b) Xác định vị trí X,Y trong bảng tuần hoàn
Câu 2: Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là \(ns^2np^3\). Trong hợp chất khí của nguyên tố X với hiđro, X chiếm 91,18% khối lượng
a) Xác định nguyên tố X
b) Tính % khối lượng của nguyên tố X trong oxit cao nhất
Câu 3: Cho các chất sau: MgO, \(N_2, CO_2, HCl, FeCl_2, H_2O, NaF\)
a) Dựa vào tính chất các nguyên tố cấu tạo nên các phân tử, hãy cho biết phân tử nào các liên kết cộng hóa trị, phân tử nào có liên kết ion
b) Hãy viết công thức electron, công thức cấu tạo của các phân tử có liên kết cộng hóa trị
c) Mô tả sử hình thành liên kết trong các hợp chất được tạo bởi liên kết ion
Câu 4: Cho 8 gam 1 kim loại A( thuộc nhóm IIA) tác dụng hết với 200ml nước thì thu được 4,48 lít khí hiđro(đktc)
a) Hãy xác định tên kim loại đó( Biết nhóm IIA gồm: Be=9, Mg=24, Ca=40, Sr=88, Ba=137, Ra=226)
b) Tính nồng độ \(C_M\) của dung dịch thu được sau phản ứng? ( Bỏ qua thể tích của chất khí, chất rắn và coi thể tích là dung dịch sau phản ứng thay đổi không đáng kể)
Hợp chất M có công thức X2Y3. Tổng số electron trong phân tử M là 50. Hiệu số proton của hai nguyên tử X và Y là 5. Xác định hai nguyên tố X, Y.
Hợp chất X2Y3 có tổng số hạt cơ bản( proton,nơtron,electron) trong 1 phân tử là 152, trong đó số hạt không mang điện kém số hạt mang điện là 48. Nguyên tử khối của X lớn hơn nguyên tử khối của Y là 11.Xác định 2 nguyên tố X,Y và công thức X2Y3.
Có
+) 2(2pX + nX) + 3(2pY + nY) = 152
=> 4pX + 2nX + 6pY + 3nY = 152 (1)
+) (4.pX +6.pY)- (2nX + 3nY) = 48 (2)
+) pX + nX - pY - nY = 11 (3)
(1)(2) => \(\left\{{}\begin{matrix}2p_X+3p_Y=50\\2n_X+3n_Y=52\end{matrix}\right.\)
=> 2(pX + nX) + 3(pY + nY) = 102 (4)
(3)(4) => \(\left\{{}\begin{matrix}p_X+n_X=27=>A_X=27\left(Al\right)\\p_Y+n_Y=16=>A_Y=16\left(O\right)\end{matrix}\right.\)
=> CTHH: Al2O3
Đúng 1
Bình luận (0)
Nguyên tử X có tổng các hạt là 52 trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt . Hãy xác định số p,n,e , viết kí hiệu nguyên tử , viết cấu hình electron của X
\(\left\{{}\begin{matrix}2Z+N=52\\2Z-N=16\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}Z=17\\N=18\end{matrix}\right.\)
p=e=17
n=18
Cấu hình là: \(1s^22s^22p^63s^23p^5\)
Đúng 1
Bình luận (0)
Nguyễn Lê Phước Thịnh CTV : bạn có thế làm hẳn ra 1 tí nữa được không chứ tắt quá mình không hiểuu =))
Đúng 0
Bình luận (0)
Bài 1: Tổng số hạt proton, nơtron, electron của nguyên tử nguyên tố X là 58 . Trong ng/tử tỉ lệ hạt mang điện và không mang điện là 19 : 10.a/ Xác định số e, số khối và viết kí hiệu của nguyên tử nguyên tố X. b/ Viết cấu hình e của ng/tử X? Cho biết X là kim loại, phi kim hay khí hiếm và loại ng/tố s, p, d, hay f? Giải thích?Giúp em với ạ!!!!!!!
Đọc tiếp
Bài 1: Tổng số hạt proton, nơtron, electron của nguyên tử nguyên tố X là 58 . Trong ng/tử tỉ lệ hạt mang điện và không mang điện là 19 : 10.
a/ Xác định số e, số khối và viết kí hiệu của nguyên tử nguyên tố X.
b/ Viết cấu hình e của ng/tử X? Cho biết X là kim loại, phi kim hay khí hiếm và loại ng/tố s, p, d, hay f? Giải thích?
Giúp em với ạ!!!!!!!
cho mình hỏi bài này làm sao vậy Bài 1 : nguyên tử X có tổng số hạt các loại là 28 hạt . Số notron nhiều hơn số proton 1 hạt a) xác định số hạt mỗi loại ? b) tính số khối của hạt nhân nguyên tử X c) viết cấu hình electron nguyên tử d) nguyên tố X thuộc loại nguyên tố nào ( kim loại , phi kim , khí hiếm ) ?.Bài 2 : nguyên tử của nguyên tố B có tổng số các hạt cấu tạo là 93 . Trong đó số hạt mang điện nhiều hơn không mang điện là 23 hạt .Xác định số hiệu nguyên tử của nguyên tố và viết cấu hình el...
Đọc tiếp
cho mình hỏi bài này làm sao vậy
Bài 1 : nguyên tử X có tổng số hạt các loại là 28 hạt . Số notron nhiều hơn số proton 1 hạt
a) xác định số hạt mỗi loại ?
b) tính số khối của hạt nhân nguyên tử X
c) viết cấu hình electron nguyên tử
d) nguyên tố X thuộc loại nguyên tố nào ( kim loại , phi kim , khí hiếm ) ?.
Bài 2 : nguyên tử của nguyên tố B có tổng số các hạt cấu tạo là 93 . Trong đó số hạt mang điện nhiều hơn không mang điện là 23 hạt .Xác định số hiệu nguyên tử của nguyên tố và viết cấu hình electron nguyên tử của nó .
Bài 3 : nguyên tử của nguyên tố A có tổng số các hạt cấu tạo là 40 . Xác định số hiệu nguyên tử của nguyên tố và viết cấu hình electron nguyên tử của nó .
ta co p+e+n=93 mà p=e=z => 2z+n=93
2z-n=23 ( vì số hạt mang điện nhiều hơn số hạt ko mang điện là 23)
tu 2 pt trên ta có z =29,,n=35
=> số hiệu nguyên tử của B = Z = 29
cấu hình electron
\(1s^22s^22p^63s^23p^64s^23d^9\)
Đúng 0
Bình luận (0)
đối với các dạng bài này , bạn cần nhớ kiến thức như sau :
Tổng số hạt trong nguyên tử = 2p + n ( gồm có 3 loại hạt : n , p, e trong đó p=e)
số hạt mang điện là 2p
số hạt không mang điện là n
số hiệu nguyên tử là Z= p = e = số thứ tự nhóm .
Sau khi xác định được p ,, tức là cũng xác định được e thì
cấu hình viết theo dãy trật tự các mức năng lượng
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10.......
Các nguyên tử có 1, 2, 3e ở lớp ngoài cùng là các nguyên tử kim loại, trừ H, He và B.Các nguyên tử có 5, 6, 7e ở lớp ngoài cùng thường là các nguyên tố phi kim. Các nguyên tử có 4e ở lớp ngoài cùng có thể là nguyên tử kim loại hoặc phi kim
Đúng 0
Bình luận (3)
bài 1 : a/
tacó p+e+n=28
<=> z+z+n=28
> 2z+n=28 1
vì n lớn hơn p là 1 nên ta có pt:
n-z=1hay -z+n=1 2
từ 1 và 2 ta có hệ phương trình
2z+n=28
-z+n=1
=>z= 9,n=10
b/ số khối A = Z + N = 9 + 10 = 19
c/ Cấu hình electron nguyên tử :\(1s^22s^22p^63s^23p^64s^1\)
d/ Nguyên tố X là kim loại cụ thể ở đây là Kali
Đúng 0
Bình luận (3)
Xem thêm câu trả lời
Tổng số hạt nguyên tử X là 50. Trong nguyên tử X tổng số hạt mang điện nhiều hơn số hạt ko mang điện là 14.
a) Tính số hạt p, n và e trong nguyên tử X.
b) Biết trong nguyên tử X, các electron được phân bố trên ba lớp, lớp thứ nhất 2e, lớp thứ hai có 8e, lớp thứ ba có 6e. Hãy vẽ sơ đồ cấu tạo nguyên tử X.
Nguyên tử của nguyên tố X có tổng số hạt electron trong các phân lớp p là 7. Một nguyên tử của nguyên tố Y có số hạt mang điện nhiều hơn số hạt mang điện của một nguyên tử X là 8 hạt. Xác định X, Y.
X : Các phân lớp p của X có 7 e → có 2 phân lớp p → 2 p 6 và 3 p 1
→ Cấu hình e của X : 1 s 2 2 s 2 2 p 6 3 s 2 3 p 1 → z = 13 (Al)
Số hạt mang điện của X là 2 Z X = 26
→ Số hạt mang điện của Y : 26 + 8 = 34 → Z Y = 17 (Cl)
Đúng 1
Bình luận (0)