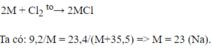Cho 1 luồng khí Cl2 dư tác dụng với 9,2 g kim loại thu được 23,4 g muối clorua của kim loại hóa trị I. Tìm tên kim loại trên.

Những câu hỏi liên quan
Cho một luồng khí clo dư tác dụng với 9,2 gam kim loại sinh ra 23,4 gam muối của kim loại có hoá trị I. Hãy xác định tên của kim loại.
- Gọi kí hiệu và nguyên tử khối của kim loại là M.
Phương trình hoá học :
2M + Cl 2 → 2MCl
9,2 x 2(M + 35,5) = 2M x 23,4
653,2 = 28,4M
M = 23. Vậy kim loại M là kim loại natri (Na).
Đúng 2
Bình luận (0)
Cho luồng khí clo (dư) tác dụng với 9,2g kim loại hóa trị I, tạo ra 23,4 g muối. Xác định tên kim loại (Na=23, Ag=108, Li=7, K=39, Cl=35,5).
Cho một luồng khí clo dư tác dụng với 9,2 gam kim loại sinh ra 23,4 gam muối kim loại M hoá trị I. Muối kim loại hoá trị I là muối nào sau đây ?
A. NaCl
B. KCl
C. LiCl
D. Kết quả khác
Đáp án A
2M + Cl2 → 2MCl
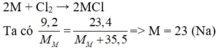
Vậy muối là NaCl.
Đúng 0
Bình luận (0)
Cho luồng khí clo dư tác dụng với 9,2 gam kim loại A sinh ra 23,4 gam muối .Xác định tên kim loại .
Xem chi tiết
Giả sử kim loại A có hóa trị n.
PTHH : 2A + nCl2 --> 2ACln
Áp dụng ĐLBT khối lượng => mCl2 = 23,4-9,2 =14,2 gam <=> nCl2=\(\dfrac{14,2}{71}\)= 0,2 mol
=> nA = 0,4/n => MA = \(\dfrac{9,2.n}{0,4}\)= 23n
=> giá trị thỏa mãn là n = 1 , MA = 23 ( g/mol ) , A là natri (Na)
Đúng 1
Bình luận (0)
cho 1 luồng khí có dư tác dụng với 9,2g kim loại hóa trị I sinh ra 23,4g muối clorua . Xác định kim loại
2A+Cl2->2ACl
nA=nACl
mA/mACl=MA/MA+35.5
Theo bài ra:mA:mACl=9.2:23.4
->MA/MA+35.5=9.2/23.4
->MA=23(g/mol)->A là Natri
Đúng 0
Bình luận (4)
theo đề bài, khí là Cl2
gọi Kim loại đó là A
PTK của nó là MA
số mol của nó là a
PT: 2A+CL2=>2ACl
nACl=nA=a
theo bài ra ta có :
MA*a=9,2
(MA+35,5)*a=23,4
giải hệ này ra sẽ tính được a=0,4
từ đó tính được PTK của kim loại = 23 => đó là Na
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
9,2 gam kim loại A phản ứng với khí clo thu được 23,4 gam muối duy nhất.Biết rằng A có hóa trị 1,hãy xác định tên kim loại A
HD:
2A + Cl2 \(\rightarrow\) 2ACl
9,2 m 23,4 (g)
Áp dụng ĐL BTKL ta có: m = 23,4 - 9,2 = 14,2 gam.
Như vậy số mol của A = 2 x số mol của Cl2 = 0,4 mol. Suy ra: A = 9,2/0,4 = 23 (Na).
Đúng 0
Bình luận (0)
A có hóa trị I nên công thức của muối clorua là ACl
PTHH: 2A + Cl2 → 2Acl
Theo định luật bảo toàn khối lượng ta có:
mCl2 = mmuối – mkim loại = 23,4 - 9,2 = 14,2
=>nCl2 = 14,2/71 = 0,2 mol
Theo phương trình hóa học => nA = 2 nCl2 = 0,4 mol
Suy ra 0,4.A = 9,2. Vậy А = 23 (Na).
Đúng 0
Bình luận (0)
Cho 9,2g 1 kim loại A chưa rõ hóa trị tác dụng với khí Clo dư, sau phản ứng tạo thành 23,4g muối clorua của kim loại đó. XĐ tên kim loại A
Gọi hóa trị của kim loại A là n
\(2A + nCl_2 \xrightarrow{t^o} 2ACl_n\)
Theo PTHH :
\(n_A = n_{ACl_n}\)
⇔ \(\dfrac{9,2}{A} = \dfrac{23,4}{A+35,5n}\)
⇔ A = 23n
Với n = 1 thì A = 23(Na)
Vậy kim loai A là Natri.
Đúng 3
Bình luận (0)
Cho 6,4 gam kim loại hóa trị II tác dụng với Cl2 dư, sau phản ứng thu được 13,5 gam muối. Xác
định tên kim loại?
Áp dụng ĐLBTKL, ta có:
m(kim loại) + mCl2 = m(muối)
=> mCl2 = 13,5 - 6,4 = 7,1 (g)
nCl2 = 7,1/71 = 0,1 (mol)
PTHH: R + Cl2 -> (t°) RCl2
Mol: 0,1 <--- 0,1
M(R) = 6,4/0,1 = 64 (g/mol)
=> R là Cu
Đúng 3
Bình luận (0)
\(X+Cl_2-^{t^o}\rightarrow XCl_2\\ Tacó:n_X=n_{XCl_2}\\ \Rightarrow\dfrac{6,4}{X}=\dfrac{13,5}{X+35,5.2}\\ \Rightarrow X=64\left(Cu\right)\)
Đúng 1
Bình luận (0)
Cho 5,6 g kim loại M(hóa trị 2) tác dụng với 94,6 gam dung dịch HCL thu được m(g) muối clorua và 2,24 lít khí (dkc)a. Tìm kim loại Mb. Tính m(g) muối thu đượcc. Tính nồng độ phần trăm muối sau phản ứng
Xem chi tiết
\(M + 2HCl \to MCl_2 + H_2\\ n_M = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)\\ \Rightarrow M = \dfrac{5,6}{0,1} = 56(Fe)\\ \)
Vậy M là kim loại Fe
\(n_{FeCl_2} = n_{H_2} = 0,1(mol)\\ m_{FeCl_2} = 0,1.127 = 12,7(gam)\\ m_{dd\ sau\ pư} =m_{Fe} + m_{dd\ HCl} -m_{H_2} = 5,6 + 94,6 -0,1.2 = 100(gam)\\ C\%_{FeCl_2} = \dfrac{12,7}{100}.100\% = 12,7\%\)
Đúng 2
Bình luận (0)