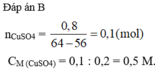Cho một bản Zn vào cốc chứa 200 gam dung dịch HCl 10% khi lấy bản Zn ra rửa sạch làm khô cân lại thấy khối lượng giảm đi 6,5 gam so với trước xác định nồng độ phần trăm dung dịch HCL Sau phản ứng

Những câu hỏi liên quan
ngâm 1 lá kẽm vào côc chứa 400g dung dịch HCL 15 phần trăm sau 1 thời gian phản ứng lấy lá kẽm ra khỏi dung dịch rửa sạch làm khô nhân thấy khối lượng của nó giảm 13g so với nước hãy xác định nồng độ phần trăm của các chất có trong dung dịch sau phản ứng
help me giúp em với
Cho một bản kẽm vào cốc chứa 200g dd HCl 10% khi lấy bản kẽm ra rữa sạch làm khô thấy khối lượng giảm đi 6,5 g so với trước. Xác định C% sau phản ứng
mHCl = \(\frac{2.10\%}{100\%}\)= 20 (g)
Khối lượng lá kẽm giảm 6,5 gam chính là khối lượng Zn tham gia phản ứng
\(\rightarrow\)nZn = mZn : MZn = 6,5 : 65 = 0,1 (mol)
PTHH: Zn + 2HCl\(\rightarrow\)ZnCl2 + H2
_______0,1___0,2__0,1_____0,1 (mol)
Theo PTHH: nH2 = nZnCl2 = nZn pư = 0,1(mol)
\(\rightarrow\)mZnCl2 = 0,1.136 = 13,6 (g)
Theo PTHH: nHCl pư = 2nZn = 2.0,1= 0,2 (mol)
\(\rightarrow\)mHCl pư = 0,2.36,5 = 7,3 (g)
\(\rightarrow\) mHCl dư = mHCl bđ - mHCl pư = 20 - 7,3 = 12,7(g)
Dung dịch sau phản ứng thu được gồm ZnCl2: 13,6 (g) và mHCl pư = 12,7 (g)
mdd sau = mZn pư + mdd HCl - mH2
= 6,5 + 200 - 0,1.2
= 206,3 (g)
Nồng độ phần trăm của các chất trong dd sau pư là:
C% ZnCl2 = \(\frac{13,6}{\text{ 206,3}}\).100% = 6,6%
C% HCl dư = \(\frac{7,3}{\text{ 206,3}}\).100% = 3,54%
nhúng một thanh Zn vào dung dịch có chứa 8,5g AgNO3, chỉ sau một thời gian ngắn lấy thanh Zn ra rửa sạch, làm khô cân lại thấy khối lượng Zn tăng thêm 5%. biết tất cả Ag bị đẩy ra bám hết vào thanh Zn
a, viết phương trình phản ứng
b. xác định khối lượng thanh Zn ban đầu.
gọi m Zn bđ= m
nAgNO3 = 0,05 mol
Zn + 2AgNO3 => Zn(NO3)2 + 2Ag
0,025<--0,05----->0.025--------->0,05
mZn tăng = 0,025( 216-65) = 3,775
<=> 5%m = 3,775 => m = 75,5 (g)
Đúng 0
Bình luận (0)
Cho một lá sắt có khối lượng 5 gam vào 50 ml dung dịch CuSO 4 15% có khối lượng riêng là 1,12 g/ml. Sau một thời gian phản ứng, người ta lấy lá sắt ra khỏi dung dịch, rửa nhẹ, làm khô, cân nặng 5,16 gam. Tính nồng độ phần trăm các chất còn lại trong dung dịch sau phản ứng.
Khối lượng dung dịch CuSO 4 : m dd CuSO 4 = 1,12 x 50 = 56 (gam).
CuSO 4 + Fe → FeSO 4 + Cu
64x — 56x = 5,16 - 5 = 0,16 (gam) => x = 0,02 mol.
m CuSO 4 tham gia phản ứng = 0,02 x 160 = 3,2 (gam);
100 gam dung dịch CuSO 4 có 15 gam CuSO 4 nguyên chất.
56 gam dung dịch CuSO 4 có X gam CuSO 4 nguyên chất.
x = 56 x 15/100 = 8,4g; m CuSO 4 còn lại = 8,4 - 3,2 = 5,2g
m FeSO 4 = 0,02 x 152 = 3,04g
m dd sau p / u = 56 - 0,16 = 55,84g
C % CuSO 4 = 5,2/55,84 x 100% = 9,31%
C % FeSO 4 = 3,04/55,84 x 100% = 5,44%
Đúng 1
Bình luận (0)
Cho 6,5 gam Zn tác dụng vừa đủ với 2 lít dung dịch axit HCl aM.a. Tính a.b. Nếu lấy 300 gam dung dịch muối ZnCl2 15% rồi làm bay hơi 135 gam nước, nhận thấy có 5 gam muối tách ra khỏi dung dịch bão hòa. Hãy xác định nồng độ phần trăm của dung dịch muối bão hòa trong điều kiện thí nghiệm trên?
Đọc tiếp
Cho 6,5 gam Zn tác dụng vừa đủ với 2 lít dung dịch axit HCl aM.
a. Tính a.
b. Nếu lấy 300 gam dung dịch muối ZnCl2 15% rồi làm bay hơi 135 gam nước, nhận thấy có 5 gam muối tách ra khỏi dung dịch bão hòa. Hãy xác định nồng độ phần trăm của dung dịch muối bão hòa trong điều kiện thí nghiệm trên?
1.Cho một bản kẽm vào cốc chứa 200g dd HCl 10%.Khi lấy bản kẽm ra rửa sạch, làm khô cân lại khối lượng giảm đi 6,5g so với trước.Xác định nồng độ dd HCl sau phản ứng.
2.Ngâm 1 lá sắt có khối lượng 5 gam trong 50ml dd CuSO4 15%(d=1.12g/ml). Sau một thời gian lấy lá sắt ra, rửa nhẹ, làm khô cân được 5,16 g. Tính nồng đô % (C%) của chất còn lại trong dd sau phản ứng.
Bài 1:
\(m_{HCl}=200.10\%=20g\)
\(\text{Zn+2HCl-->ZnCl2+h2}\)
m giảm=mZn phản ứng=6.5-->nZn phản ứng=0.1
-->nHCl phản ứng=0.1-->mHCl phản ứng=3.65
\(\Rightarrow\text{mHCl dư=20-3.65=16.35}\)
mdd sau phản ứng =200+6,5-0,1.2=206,3
\(\Rightarrow x\%_{HCl}=\frac{16,35}{206,3}=7,93\%\)
Bài 2:
\(\text{mdd cuso4= 56g-->nCuSO4=0.0525}\)
\(\text{Fe+CuSO4-->FeSO4+Cu}\)
a.........a..............a...........a
Ta có :
\(\text{5-56a+64a=5.16-->a=0.02}\)
mdd sau phản ứng m=56-0.16=55.84
\(C\%_{CuSO4_{du}}=\frac{\text{0.0325.160}}{\text{55.84}}\text{=9.3%}\)
\(C\%_{FeSO4}=\frac{\text{0,02.152}}{\text{55,84}}=\text{5.44 }\text{ }\)
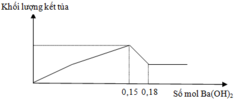
Cho từ từ đến dư dung dịch Ba(OH)2 vào dung dịch X chứa H+, Cr3+, Cl- và SO42-. Phản ứng được biểu diễn theo đồ thị sau: Nếu nhúng thanh Zn vào dung dịch X trên, kết thúc phản ứng lấy thanh Zn ra, lau khô cân lại thấy khối lượng giảm m gam so với ban đầu. Giá trị m là A. 9,75 gam B. 11,7 gam. C. 3,90 gam D. 5,85 gam
Đọc tiếp
Cho từ từ đến dư dung dịch Ba(OH)2 vào dung dịch X chứa H+, Cr3+, Cl- và SO42-. Phản ứng được biểu diễn theo đồ thị sau:
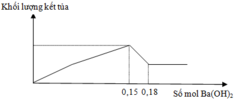
Nếu nhúng thanh Zn vào dung dịch X trên, kết thúc phản ứng lấy thanh Zn ra, lau khô cân lại thấy khối lượng giảm m gam so với ban đầu. Giá trị m là
A. 9,75 gam
B. 11,7 gam.
C. 3,90 gam
D. 5,85 gam
Nhúng một thanh Zn vào dung dịch A chứa 8,5 gam AgNO3 sau một thời gian ngắn Lấy Thanh Zn ra rửa sạch làm khổ con lại thấy có lượng Zn tăng thêm 5% biết tất cả bạn đều bị đẩy bán hết cho Zn xác định khối lượng Zn ban đầu
Ngâm một đinh sắt sạch trong 200 ml dung dịch
C
u
S
O
4
sau khi phản ứng kết thúc, lấy đinh sắt ra khỏi dung dịch rửa nhẹ làm khô nhận thấy khối lượng đinh sắt tăng thêm 0,8 gam. Nồng độ mol/lít của dung dịch
C
u
S
O
4
đã dùng là: A. 0,3M. B. 0,5M. C. 0,4M. D. 0,25M.
Đọc tiếp
Ngâm một đinh sắt sạch trong 200 ml dung dịch C u S O 4 sau khi phản ứng kết thúc, lấy đinh sắt ra khỏi dung dịch rửa nhẹ làm khô nhận thấy khối lượng đinh sắt tăng thêm 0,8 gam. Nồng độ mol/lít của dung dịch C u S O 4 đã dùng là:
A. 0,3M.
B. 0,5M.
C. 0,4M.
D. 0,25M.