Có bao nhiêu gam đồng điều chế được khi cho tương tác 16g đồng sunfat với một lượng sắt cần thiết

Những câu hỏi liên quan
Có bao nhiêu gam đồng điều chế được khi cho tương tác 16g đồng sunfat với một lượng sắt cần thiết.
Cần bao nhiêu gam Pôtat ăn da cho phản ứng với 10g sắt III clorua ?
Có bao nhiêu gam đồng điều chế được khi cho tương tác 16g đồng sunfat với một lượng sắt cần thiết.
Bài giải
Phương trình Hoá học: CuSO4 + Fe - > FeSO4 + Cu
160g 64g
16g xg
=> x = 
Vậy điều chế được 6,4g đồng.
Cần bao nhiêu gam Pôtat ăn da cho phản ứng với 10g sắt III clorua ?
Bài giải
PTHH FeCL3 + 3KOH -> Fe(OH)3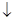 + 3KCL
+ 3KCL
10g ?
Tính tỉ số hợp thức giữa khối lượng Kali hiđrôxit và sắt II clorua
MKOH = (39 + 16 + 1) = 56g


* Tìm khối lượng KOH: m
Đúng 0
Bình luận (0)
Cho kim loại sắt tác dụng với vừa đủ với 12,775 g axit clohiđric (HCl). a - Viết phư¬ơng trình hoá học xảy ra. b - Tính thể tích khí hiđro thu được (ở điều kiện tiêu chuẩn) c - Tính số gam Cu thu được khi dùng lượng khí H2 điều chế được ở trên để khử 16g đồng (II) oxit .
Để tạo thành nhôm oxit người ta cho nhôm tác dụng với oxi. Hãy tính:
a) khối lượng oxi cần thiết để điều chế được 5,1g nhôm oxit
b) để điều chế được lượng oxi cần phải dung bao nhiêu gam KMnO4
a) nAl2O3= 5,1/102=0,5(mol)
PTHH: 4Al +3 O2 -to-> 2 Al2O3
nO2= 3/2. nAl2O3= 3/2 . 0,05= 0,075(mol)
=>mO2=0,075 x 32= 2,4(g)
b) 2 KMnO4 -to-> K2MnO4 + MnO2 + O2
nKMnO4= 2.nO2= 2. 0,075= 0,15(mol)
=> mKMnO4= 0,15 x 158= 23,7(g)
Đúng 2
Bình luận (0)
nAl2O3 = \(\dfrac{5,1}{102}\)=0,05
PTHH
4Al + 3O2 = 2Al2O3
theo phương trình 4 mol : 3 mol : 2 mol
theo đề bài 0,075mol : 0,05mol
mO2 = 0,075. 32= 2,4g
PTHH
2KMnO4 ➜ K2MnO4 + MnO2 + O2
theo phương trình 2mol : 1mol : 1mol : 1mol
theo đề bài 0,05 mol : 0,075 mol
mKMnO4= 0,05. 158= 7,9g
Đúng 0
Bình luận (2)
cho một đinh sắt nặng 90 gam được nhúng vào dung dịch đồng sunfat . sau một thời gian lấy đinh sắt ra cân được 91,3 kg hỏi thanh sắt còn lại có bao nhiêu khối lượng sắt và cu
Fe + CuSO4 → FeSO4 + Cu
x..........x..................x............x..........(mol)
Sau phản ứng :
$m_{thanh\ sắt} = 90 - 56x + 64x = 91,3 \Rightarrow x = 0,1625$
$m_{Cu} = 0,1625.64 = 10,4(gam)$
$m_{Fe} = 91,3 - 10,4 = 80,9(gam)$
Đúng 2
Bình luận (0)
Cần phải điều chế một lượng muối đồng sunfat. Phương pháp nào sau đây tiết kiệm được axit sunfuric ? Axit sunfuric tác dụng với đồng(II) oxit.
Viết các phương trình hoá học và giải thích.
Hướng dần
- Viết hai phương trình hoá học.
- Muốn điều chế n mol CuSO 4 thì số mol H 2 SO 4 trong mỗi phản ứng sẽ là bao nhiêu ?
Từ đó rút ra, phản ứng của H 2 SO 4 với CuO sẽ tiết kiệm được H 2 SO 4
Ta có phương trình:
CuO + H 2 SO 4 → CuSO 4 + H 2 O
Đúng 0
Bình luận (0)
Cần phải điều chế một lượng muối đồng sunfat. Phương pháp nào sau đây tiết kiệm được axit sunfuric ? Axit sunfuric đặc tác dụng với đồng kim loại.
Viết các phương trình hoá học và giải thích.
Hướng dần
- Viết hai phương trình hoá học.
- Muốn điều chế n mol CuSO 4 thì số mol H 2 SO 4 trong mỗi phản ứng sẽ là bao nhiêu ?
Từ đó rút ra, phản ứng của H 2 SO 4 với CuO sẽ tiết kiệm được H 2 SO 4
Ta có phương trình:
CuO + 2 H 2 SO 4 ( đ ) → CuSO 4 + SO 2 + 2 H 2 O
Gỉa sử cần điều chế 1 mol CuSO 4
Theo pt (a) n H 2 SO 4 = n CuSO 4 = 1 mol
Theo pt (b) n H 2 SO 4 = 2 n CuSO 4 = 2 mol
⇒ Dùng theo phương pháp a tiết kiệm axit hơn
Đúng 0
Bình luận (0)
Có thể điều chế bao nhiêu gam axit sunfuric khi cho 240g SO4 tác dụng với nước?
Đốt cháy hỗn hợp khí gồm 1,12 lít khí hidro và 1,68 khí oxi (đktc) tính khối lượng nước và thể tích nước ( trạng thái lỏng ) thu được?
Để có một dung dịch chứa 16g NaOH thì cần bao nhiêu gam Na2O cho vào nước?
a)
SO3 + H2O $\to$ H2SO4
n H2SO4 = n SO3 = 240/80 = 3(mol)
m H2SO4 = 3.98 = 294(gam)
b)
2H2 + O2 $\xrightarrow{t^o}$ 2H2O
V H2 / 2 = 0,56 < V O2 = 1,68 nên O2 dư
n H2O = n H2 = 1,12/22,4 = 0,05(mol)
m H2O = 0,05.18 = 0,9(gam)
V H2O = m/D = 0,9/1 = 0,9(ml)
c)
n NaOH = 16/40 = 0,4(mol)
Na2O + H2O $\to$ 2NaOH
n Na2O = 1/2 n NaOH = 0,2(mol)
m Na2O = 0,2.62 = 12,4(gam)
Đúng 3
Bình luận (2)
a)Ta có PT:SO4+H2O=H2SO4
Theo bài ra t có nSO4=240:96=2,5
Mà nSo4=nH2So4=2,5 mol
suy ra:mH2So4=2,5.98=245g
Đúng 1
Bình luận (0)
ta có PT 2H2+O2=2H2O
nH2=1,12:22,4=0,05MOL
nO2=1,68:22.4=0,075mol
theo pt ta có 0,05:2<0,075:1
suy ra H2 hết,O2 dư.
theo PT ta có:nH2O=nH2=0,05mol
suy ra VH2O=.....
mH2O=.....
Đúng 1
Bình luận (0)
Cho 6,4 gam đồng tác dụng vừa đủ với khí oxi ở nhiệt độ cao. Sau phản ứng thu được chất rắn màu đen là đồng (II) oxit. a. Viết PTHH của phản ứng. b. Tính khối lượng oxit sắt từ thu được. c. Tính khối lượng thuốc tím KMnO4 cần dùng để điều chế được khí oxi cho phản ứng trên. d. Nếu cho không khí tác dụng với lượng đồng ở trên thì cần bao nhiêu lít không khí (ở đktc). Biết oxi chiếm 20% thể tích không khí. Cho Cu 64 ; O 16
Đọc tiếp
Cho 6,4 gam đồng tác dụng vừa đủ với khí oxi ở nhiệt độ cao. Sau phản ứng thu được chất rắn màu đen là đồng (II) oxit. a. Viết PTHH của phản ứng. b. Tính khối lượng oxit sắt từ thu được. c. Tính khối lượng thuốc tím KMnO4 cần dùng để điều chế được khí oxi cho phản ứng trên. d. Nếu cho không khí tác dụng với lượng đồng ở trên thì cần bao nhiêu lít không khí (ở đktc). Biết oxi chiếm 20% thể tích không khí. Cho Cu = 64 ; O = 16
a)
\(2Cu + O_2 \xrightarrow{t^o} 2CuO\)
b)
\(n_{CuO} = n_{Cu} = \dfrac{6,4}{64} = 0,1(mol)\\ \Rightarrow m_{CuO} = 0,1.80 = 8(gam)\)
c)
\(n_{O_2} = \dfrac{1}{2}n_{Cu} = 0,05(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ m_{KMnO_4} = 2n_{O_2} = 0,05.2 = 0,1.158 = 15,8(gam)\)
d)
\(V_{không\ khí} = 5V_{O_2} = 0,05.22,4.5 = 5,6(lít)\)
Đúng 1
Bình luận (0)
Cho khí hiđro tác dụng vừa đủ với 16g sắt (III) oxit ở nhiệt độ cao.a. Tính khối khối lượng sắt thu đượcb. Tính thể tích khí hiđro (đktc) được dùng để điều chế lượng sắt nói trên. c. Tính khối lượng magie để khi tác dụng với dung dịch axit clohiđric dư (HCl) thu được lượng hiđro trên?
Đọc tiếp
Cho khí hiđro tác dụng vừa đủ với 16g sắt (III) oxit ở nhiệt độ cao.
a. Tính khối khối lượng sắt thu được
b. Tính thể tích khí hiđro (đktc) được dùng để điều chế lượng sắt nói trên.
c. Tính khối lượng magie để khi tác dụng với dung dịch axit clohiđric dư (HCl) thu được lượng hiđro trên?
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Ta có: \(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
a, \(n_{Fe}=2n_{Fe_2O_3}=0,2\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,2.56=11,2\left(g\right)\)
b, \(n_{H_2}=3n_{Fe_2O_3}=0,3\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
c, PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Theo PT: \(n_{Mg}=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{Mg}=0,3.24=7,2\left(g\right)\)
Đúng 2
Bình luận (1)




















