Cho 9,6 g một kim loại M chưa biết hóa trị tác dụng với lượng dư khí Oxi rồi cho toàn bộ chất rắn thu được sau phản ứng tan hoàn toàn .Trong dung dịch H2SO4 loãng thấy phải dùng hết 14,7 g Oxit
Xác định kim loại M.
Cho 11,76 g hỗn hợp X gồm Fe, Mg, Cu tác dụng với 100ml dung dịch HNO3 3,4 M. Sau phản ứng thấy tạo khí NO và còn một kim loại chưa tan hết. Cho từ từ dung dịch H2SO4 0,5 M vào hỗn hợp thu được, đến khi kim loại vừa tan hết thấy tốn hết 220ml axit, phản ứng lại sinh ra thêm khí NO. Lấy toàn bộ dung dịch thu được tác dụng với NaOH dư. Tách kết tủa nung nóng trong không khí đến khối lượng không đổi tạo 15,6 g chất rắn. Tính % khối lượng các chất trong X.
Bài 10: Cho một lượng kim loại M phản ứng hoàn toàn với dung dịch CuSO4 sau phản ứng khối lượng chất rắn thu được gấp 1,143 lần khối lượng M đem dùng.Mặt khác, nếu dùng 0,02mol kim loại M tác dụng với H2SO4 loãng lấy dư thì thu được 0,448lits khí (đktc) . Xác định kim loại M.
Thí nghiệm 2 : 2M + nH2SO4 ---> M2(SO4)n + nH2
Theo pthh : nH2 = \(\dfrac{n}{2}n_M\)
=> 0,02 = \(\dfrac{n}{2}.0,02\)
=> n = 2 => M hóa trị II
Thí nghiệm 1 : Đặt nM = x (mol)
M + CuSO4 ---> MSO4 + Cu
Theo pthh : nCu = nM = x (mol)
=> \(\dfrac{m_{Cu\left(spu\right)}}{m_{M\left(bandau\right)}}=\dfrac{64x}{M_Mx}=\dfrac{64}{M_M}=1,143\Rightarrow M_M=56\) (g/mol)
Vậy kim loại M là Fe (Sắt)
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
A. Al.
B. Na
C. Ca.
D. K.
Nhiệt phân hoàn toàn 0,1 mol KMnO4 toàn bộ khí oxi thu được cho tác dụng hết với 11,7g kim loại M, được chất rắn X. Cho chất rắn X vào dung dịch H2SO4 loãng, dư thu được 1,792 lít H2 (đktc). M là kim loại gì ?
\(n_{O_2}=\dfrac{1}{2}\cdot n_{KMnO_4}1=\dfrac{1}{2}\cdot0.1=0.05\left(mol\right)\)
\(n_{H_2}=\dfrac{1.792}{22.4}=0.08\left(mol\right)\)
\(\Rightarrow n_{M\left(dư\right)}=\dfrac{0.08\cdot2}{n}=\dfrac{0.16}{n}\left(mol\right)\)
\(n_{M\left(pư\right)}=\dfrac{0.05\cdot4}{n}=\dfrac{0.2}{n}\left(mol\right)\)
\(m_M=\left(\dfrac{0.16}{n}+\dfrac{0.2}{n}\right)\cdot M=11.7\left(g\right)\)
\(\Leftrightarrow0.36M=11.7n\)
\(\Leftrightarrow M=32.5n\)
\(BL:n=2\Rightarrow M=65\)
\(M:Zn\)
\(\)
\(PTHH:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
\(\Rightarrow n_{O_2}=0,05\left(mol\right)\)
Gọi hóa trị của M là n
Bảo toàn e: \(\Rightarrow n_M=0,2+0,16=\dfrac{0,36}{n}\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{11,7n}{0,36}=32,5n\)
Biện luận:
\(n=2\rightarrow M=65\left(Zn\right)\)
Cho 16,2 gam kim loại M (hóa trị không đổi) tác dụng với 0,15 mol oxi. Chất rắn sau phản ứng cho hòa tan hoàn toàn vào dung dịch HCL dư, thu được 13,44 lít H2 (đktc). Biết các phản ứng xảy ra hoàn toàn. Kim loại M là
A. Ca
B. Zn
C. Al
D. Mg
Đáp án C
Các phương trình phản ứng :
M tác dụng với O2: 4 M + 2 n O 2 → t 0 2 M n O n
Chất rắn sau phản ứng tác dụng với dung dịch HCl thu được khí H2, chứng tỏ chất rắn sau có M dư nên O2 hết - chất rắn sau gồm M dư và M2On :
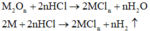
Tính toán:
Số mol H2 thu được là: n H 2 = 13 , 44 22 , 4 = 0 , 6 m o l
Sơ đồ phản ứng:
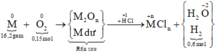
Các quá trình nhường, nhận electron cho cả quá trình:
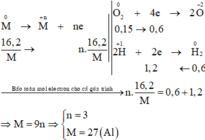
Cho 10,8g hỗn hợp X gồm Fe, Fe2O3 và Oxit kim loại hóa trị II tác dụng với 3,36 lít CO thu được khí Y và m(g) rắn Z. Dẫn toàn bộ lượng Y vào dung dịch nước vôi trong dư thu được 12,5g chất rắn không tan. Cho m(g) Z trên vào dung dịch HCl dư thì thu được 2,24 lít khí và 0,05 mol chất rắn A không tan. Xác định công thức hóa học của oxit kim loại hóa trị II trên và tính thành phần % khối lượng mỗi chất hỗn hợp X.
Các phản ứng trên xảy ra hoàn toàn, khí được đo ở đktc.
Các thánh hóa giúp mình với.
Chuyển đổi hết từ khối lượng chất sang mol chất, rồi viết phương trình phản ứng , tính từng bước theo phương trình hóa học sẽ ra được.
Bạn giải chi tiết được không????
cho 30,4 gam Mg và kim loại A hóa trị II đứng sau H trong dãy hoạt động hóa học tác dụng với một lượng dư dung dịch H2SO4 loãng thấy thoát ra 4,48 lít khí. Phần không tan cho tác dụng với H2SO4 đặc nóng dư phản ứng hoàn toàn thì sinh ra 8,96 lít khí sunfurơ
a/ xác định A
b/ Nếu cho 2 kim loại trên tác dụng với 200 gam dung dịch H2SO4 đặc, nóng thì thu được bao nhiêu lít khí có mùi trứng thối? Tính C% của dung dịch sau khi phản ứng
Mg + H2SO4 -- > MgSO4 + H2
1 1 1 1 (mol)
0,2 0,2 0,2 0,2 (mol)
nH2 = 4,48 / 22,4 = 0,2 (mol)
A + 2H2SO4 ( đặc nóng ) --> ASO4 + SO2 + 2H2O
1 2 1 1 2 (mol)
0,4 0,4 (mol)
nSO2 = 8,96 / 22,4 = 0,4 (mol)
Theo đề ta có :
24.0,2 + A.0,4 = 30,4
=> A = 64 => kim loại A là Cu
Mg + 2H2SO4 ( đặc nóng )---> MgSO4 + SO2 + 2H2O
1 2 1 1 2 (mol)
0,2 0,2 (mol)
Cu + 2H2SO4 ( đặc nóng ) ---> CuSO4 + SO2 + 2H2O
1 2 1 1 2 (mol)
0,4 0,4 (mol)
nSO2 = 0,2+0,4 = 0,6 (mol)
= > VSO2 = 0,6 . 22,4 = 13,44 (l)
mMgSO4 = 0,2 . 120 = 24 (g)
mCuSO4 = 0,4.160 = 64 (g)
mSO2 (cả pứ ) = 0,6.64 = 38,4 (g)
mdd = mhhkl + mddH2SO4 - mSO2
= 30,4 + 200 - 38,4 = 192 (g)
=> \(C\%_{ddMgSO_4}=\dfrac{24.100}{192}=12,5\%\)
\(C\%_{ddCuSO_4}=\dfrac{64.100}{192}=33,33\%\)
a) để hòa tan hoàn toàn 8 g oxit một kim loại R cần dùng 10,95 g HCl .hỏi R là kim loại gì ?
b) hòa tan hoàn toàn 1,44 g kim loại hóa trị 2 bằng dung dịch H2SO4 loãng chứa 7,35 g H2SO4 để phản ứng hết lượng dư axit người ta phải dùng 1,3 g NaOH sau phản ứng thu được muối Natrisunjat và nước . viết PTHH và xác định kim loại đem dùng
a) CT : R2On
nHCl = 10.95/36.5 = 0.3 (mol)
R2On + 2nHCl => 2RCln + nH2O
0.15/n_____0.3
M= 8/0.15/n = 160n/3
=> 2R + 16n = 160n3
=> 2R = 112n/3
BL : n 3 => R = 56
R là : Fe
b)2NaOH + H2SO4 => Na2SO4 + H2O
nH2SO4(bđ) = 7.36/98 = 0.075 (mol)
nNaOH = 1.3/40 = 0.0325 (mol)
=> nH2SO4(pư) = 0.075 - 0.0325/2 = 0.05875 (mol)
R + H2SO4 => RSO4 + H2
0.05875_0.05875
M = 1.44/0.05875= 24
R là : Mg
Chúc bạn học tốt !!!
Nung 22,4 gam kim loại M hoá trị 2 với lưu huỳnh dư, sau phản ứng hoàn toàn thu được chất rắn X. Cho chất rắn X tác dụng hoàn toàn với lượng dư dung dịch HCl thu được khí Y và 6,4 gam bã rắn không tan. Làm khô chất bã rắn rồi đốt cháy hoàn toàn thu được khí Z. Khí Z phản ứng vừa đủ với khí Y thu được 19,2 gam đơn chất rắn. Vậy M là:
A. Ca
B. Mg
C. Fe
D. Zn.