trong một bình kín chứa 500 mol hỗn hợp gồm N2 và H2 theo tỉ lệ số mol là 1:4. Với điều kiện thích hợp 2 khí trên phản ứng tạo thành 50 mol NH3. Tính hiệu suất phản ứng tạo thành NH3

Những câu hỏi liên quan
trong một bình kín chứa 500 mol hỗn hợp gồm N2 và H2 theo tỉ lệ số mol là 1:4. Với điều kiện thích hợp 2 khí trên phản ứng tạo thành 50 mol NH3. Tính hiệu suất phản ứng tạo thành NH3
ban đầu nN2+ nH2=500 và nN2/nH2=1/4
=>nN2=100 mol và nH2=400 mol
N2 + 3H2 ---> 2NH3
ban đầu 100 400 0
phản ứng x 3x 2x
sau phản ứng (100-x ) ( 400-3x) 2x
lại có 50=2x=> x=25 => H%=( 25/100). 100%=25%.
Đúng 0
Bình luận (3)
Trong một bình kín chứa 8 mol khí H2 và 3 mol khí N2 và một ít bột Ni làm xúc tác. Nung nóng bình trong một thời gian tới khi có 60% thể tích H2 phản ứng thì thu được hỗn hợp khí A (gồm N2, H2 và NH3).
a/ Tính thể tích NH3 tạo thành (đktc).
b/ Tính tỉ khối của A đối với H2.
a) \(N_2+3H_2-^{t^o}\rightarrow2NH_3\)
3..........8
Lập tỉ lệ \(\dfrac{3}{1}>\dfrac{8}{3}\) => Tính theo số mol H2
\(n_{H_2\left(pứ\right)}=8.60\%=4,8\left(mol\right)\)
=> \(n_{NH_3}=\dfrac{4,8.2}{3}=3,2\left(mol\right)\)
=> \(V_{NH_3}=3,2.22,4=71,68\left(l\right)\)
b) Hỗn hợp A gồm N2 dư, H2 dư, NH3
\(n_{N_2\left(dư\right)}=3-\dfrac{4,8}{3}=1,4\left(mol\right)\)
\(n_{H_2\left(dư\right)}=8-4,8=3,2\left(mol\right)\)
\(M_A=\dfrac{3,2.2+1,4.28+3,2.17}{3,2+1,4+3,2}=12,82\)
=>dA/H2 \(=\dfrac{12,82}{2}=6,41\)
Đúng 2
Bình luận (0)
Hỗn hợp X gồm: N2 và H2 với tỉ lệ mol là 1 : 4. Nung hỗn hợp X ở điều kiện thích hợp để phản ứng xảy ra. Biết hiệu suất phản ứng là 40%. Phần trăm theo thể tích của amoniac (NH3) trong hỗn hợp thu được sau phản ứng là: A. 16,04%. B. 17,04%. C. 18,04%. D. 19,04%.
Đọc tiếp
Hỗn hợp X gồm: N2 và H2 với tỉ lệ mol là 1 : 4. Nung hỗn hợp X ở điều kiện thích hợp để phản ứng xảy ra. Biết hiệu suất phản ứng là 40%. Phần trăm theo thể tích của amoniac (NH3) trong hỗn hợp thu được sau phản ứng là:
A. 16,04%.
B. 17,04%.
C. 18,04%.
D. 19,04%.
Hỗn hợp X gồm: N2 và H2 với tỉ lệ mol là 1 : 4. Nung hỗn hợp X ở điều kiện thích hợp để phản ứng xảy ra. Biết hiệu suất phản ứng là 40%. Phần trăm theo thể tích của amoniac (NH3) trong hỗn hợp thu được sau phản ứng là: A. 16,04%. B. 17,04%. C. 18,04%. D. 19,04%.
Đọc tiếp
Hỗn hợp X gồm: N2 và H2 với tỉ lệ mol là 1 : 4. Nung hỗn hợp X ở điều kiện thích hợp để phản ứng xảy ra. Biết hiệu suất phản ứng là 40%. Phần trăm theo thể tích của amoniac (NH3) trong hỗn hợp thu được sau phản ứng là:
A. 16,04%.
B. 17,04%.
C. 18,04%.
D. 19,04%.
Đáp án D
Dễ thấy hiệu suất tính theo N2.
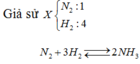
Bd: 1 4
Pu: 0,4→1,2→0,8
Sau: 0,6 2,8 0,8
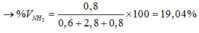
Đúng 0
Bình luận (0)
Hỗn hợp X gồm: N2 và H2 với tỉ lệ mol là 1 : 4. Nung hỗn hợp X ở điều kiện thích hợp để phản ứng xảy ra. Biết hiệu suất phản ứng là 40%. Phần trăm theo thể tích của amoniac (NH3) trong hỗn hợp thu được sau phản ứng là: A. 16,04% B. 17,04% C. 18,04% D. 19,04%
Đọc tiếp
Hỗn hợp X gồm: N2 và H2 với tỉ lệ mol là 1 : 4. Nung hỗn hợp X ở điều kiện thích hợp để phản ứng xảy ra. Biết hiệu suất phản ứng là 40%. Phần trăm theo thể tích của amoniac (NH3) trong hỗn hợp thu được sau phản ứng là:
A. 16,04%
B. 17,04%
C. 18,04%
D. 19,04%
Đáp án D
Dễ thấy hiệu suất tính theo N2
Giả sử X N 2 : 1 H 2 : 4
![]()
Đúng 0
Bình luận (0)
Trong một bình kín chứa 4 mol khí H2 và 2 mol khí N2 và một ít bột Ni làm xúc tác. Nung nóng bình trong một thời gian thì thu được hỗn hợp khí A.a/ Nếu hiệu suất phản ứng đạt 75% thì có bao nhiêu lít khí NH3 tạo thành (đktc) .b/ Nếu tổng số mol các khí trong hỗn hợp A là 4,5 mol thì có bao nhiêu % số mol H2 bị oxi hoá thành NH3.
\(N_2+3H_2\rightarrow2NH_3\)
So sánh:
\(\dfrac{n_{N_2}}{1}=2>\dfrac{n_{H_2}}{3}=1,333\)
-> Tính theo H2
\(n_{H_2}pư=75\%.4=3\left(mol\right)\)
\(\rightarrow n_{NH_3}=2\left(mol\right)\)
\(\rightarrow V_{NH_3}=2.22,4=44,8\left(l\right)\)
b. \(N_2+3H_2\rightarrow2NH_3\)
Bđ : 2 ..... 4 ..........
Pứ : a ....... 3a ........ 2a
Sau: (2-a) : (4-3a) : 2a
2-a+4-3a+2a = 4,5
=> a = 0,75 (mol)
%nH2 bị oxh = \(\dfrac{3.0,75}{4}.100\%=56,25\%\)
Đúng 3
Bình luận (0)
Một bình kín có thể tích 0,5 lít chứa 0,5 mol H2 và 0,5 mol N2 ở nhiệt độ thích hợp, khi đạt tới trạng thái cân bằng có 0,2 mol NH3 được tạo thành. Hiệu suất của phản ứng là bao nhiêu?
A. 20%
B. 30%
C. 60%
D. 50%
Đáp án C.
N2+ 3H2 ⇌ 2NH3
Vì  nên hiệu suất tính theo H2
nên hiệu suất tính theo H2
N2+ 3H2 ⇌ 2NH3
Ban đầu 0,5 0,5 mol
Phản ứng x/3 x 2x/3 mol
Sau pứ 0,2 mol
Ở trạng thái cân bằng có 0,2 mol NH3 tạo thành nên 2x/3= 0,2
→x=0,3

Đúng 0
Bình luận (0)
Cho V lít (đktc) hỗn hợp khí
N
2
và
H
2
có tỉ lệ mol 1:4 vào bình kín và nung nóng. Sau phản ứng thu được 1,5 mol
NH
3
. Biết hiệu suất phản ứng là H 25%. Giá trị của V là A. 42 lít. B. 268,8 lít. C. 336 lít. D. 448 lít.
Đọc tiếp
Cho V lít (đktc) hỗn hợp khí N 2 và H 2 có tỉ lệ mol 1:4 vào bình kín và nung nóng. Sau phản ứng thu được 1,5 mol NH 3 . Biết hiệu suất phản ứng là H = 25%. Giá trị của V là
A. 42 lít.
B. 268,8 lít.
C. 336 lít.
D. 448 lít.
Chọn C
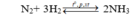
Giả sử phản ứng xảy ra với H = 100% → N 2 hết →Hiệu suất tính theo N 2 .
Đặt số mol N 2 ban đầu là x mol, n N 2 ban đầu = 4x mol;
Do hiệu suất phản ứng là 25% nên n N 2 pứ = 25%.x = 0,25x mol
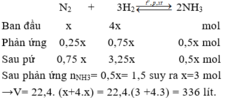
Đúng 1
Bình luận (0)
Một hỗn hợp A gồm hai khí N2 và H2 theo tỉ lệ 1:3. Tạo phản ứng giữa H2 với N2 cho ra NH3. Sau phản ứng thu được hỗn hợp khí B có tỉ khối: dA/B 0,6. Tính hiệu suất phản ứng tổng hợp NH3. A. 80% B. 50% C. 20% D. 75%
Đọc tiếp
Một hỗn hợp A gồm hai khí N2 và H2 theo tỉ lệ 1:3. Tạo phản ứng giữa H2 với N2 cho ra NH3. Sau phản ứng thu được hỗn hợp khí B có tỉ khối: dA/B = 0,6. Tính hiệu suất phản ứng tổng hợp NH3.
A. 80%
B. 50%
C. 20%
D. 75%












