Nung 1,32 a (g) hỗn hợp Mg(OH)2 và Fe(OH)2 trong không khí đến khối lượng không đổi nhận được một chất rắn có khối lượng bằng a (g).Tính % mỗi oxit tạo ra.

Những câu hỏi liên quan
Nung 1,32 a (g) hỗn hợp Mg(OH)2 và Fe(OH)2 trong không khí đến khối lượng không đổi nhận được một chất rắn có khối lượng bằng a (g).Tính % mỗi oxit tạo ra.
PTHH: Mg(OH)2 → MgO + H2O
Fe(OH)2 → FeO + H2O
Gọi số mol của Mg(OH)2 là x , số mol của Fe(OH)2 là y => Số mol của MgO là a , số mol của FeO là b
Ta có hệ phương trình sau:
58x + 90y = 1,32a (1) 40x + 72y = a (2)Nhân phương trình (2) với 1,32 ta có :
52,8x + 95,04y = 1,32a (3)
Vì phương trình (3) và phương trình (1) đều bằng 1,32a
=> 58x + 90y = 52,8x + 95,04y
=> x = 0,97y
%MgO trong hỗn hợp oxit là:
\(\dfrac{40x}{40x+72y}.100\%=\dfrac{40.0,97y}{40.0,97y+72y}.100\%=35,02\%\)
%FeO trong hỗn hợp oxit là:
100% - 35,02% = 64,98%
Đúng 0
Bình luận (0)
Nung nóng 1,32 a gam hỗn hợp mg(oh)2 và Fe(OH)2 trong không khí đến khối lượng ko đổi thu đc chất rắn Y có khối lượng a gam
Tính % khối lượng mỗi chất có trong Y
PTHH: Mg(OH)2 =(nhiệt)==> MgO + H2O
x x
4Fe(OH)2 + O2 =(nhiệt)==> 2Fe2O3 + 4H2O
y 0,25y 0,5y
Gọi số mol của Mg(OH)2, Fe(OH)2 lần lượt là x, y
Lập các số mol theo phương trình và theo đề ra ta có hệ phương trình sau:
\(\begin{cases}58x+90y=1,32a\\40x+80y=a\end{cases}\)
Giải phương trình ta đc \(\begin{cases}x=0,015a\\y=0,005a\end{cases}\)
=> %mMgO =\(\frac{0,015a.40}{a}\) x 100% = 60%
=>%mFe2O3 = 100% - 60% = 40%
Chúc bạn hoc tốt!!!
Đúng 1
Bình luận (0)
Nung nóng 1,32a gam hỗn hợp Mg(OH)2, Fe(OH)2 trong không khí đến khối lượng khôn đổi thu được chất rắn Y có khối lượng bằng a gam. Viết PTHH, tính % khối lượng mỗi chất trong hỗn hợp đầu?
PTHH:
\(Mg\left(OH\right)_2\underrightarrow{t^o}MgO+H_2O\)
x....................x
\(4Fe\left(OH\right)_2+O_2\underrightarrow{t^o}2Fe_2O_3+4H_2O\)
y...................................0,5y
Gọi số mol Mg(OH)2, Fe(OH)2 lần lượt là x, y (mol)
Theo đề ra, ta có:
\(\begin{cases}58x+90y=1,32a\\40x+80y=a\end{cases}\)
\(\Rightarrow\begin{cases}x=0,015a\\y=0,005a\end{cases}\)
=> mMgO = 0,015a x 40 = 0,6a (gam)
=> %mMgO = \(\frac{0,6a}{a}.100\%=60\%\)
=> %mFe2O3 = 100% - 60% = 40%
Đúng 0
Bình luận (0)
PTHH: Mg(OH)2 → MgO + H2O
Fe(OH)2 → FeO + H2O
Gọi số mol của Mg(OH)2 là x , số mol của Fe(OH)2 là y => Số mol của MgO là a , số mol của FeO là b
Ta có hệ phương trình sau:
58x + 90y = 1,32a (1)40x + 72y = a (2)Nhân phương trình (2) với 1,32 ta có :
52,8x + 95,04y = 1,32a (3)
Vì phương trình (3) và phương trình (1) đều bằng 1,32a
=> 58x + 90y = 52,8x + 95,04y
=> x = 0,97y
%MgO trong hỗn hợp oxit là:
40x/40x+72y.100%=40.0,97y/40.0,97y+72y.100%=35,02%.40x/40x+72y.100%=40.0,97y/40.0,97y+72y.100%=35,02%
%FeO trong hỗn hợp oxit là:
100% - 35,02% = 64,98%
Đúng 0
Bình luận (0)
Nung hỗn hợp gồm Mg(OH)2 và Fe(OH)2 ngoài không khí cho đến khi khối lượng không đổi thu được chất rắn có thành phần là
A. Mg và FeO.
B. MgO và Fe2O3.
C. MgO và FeO.
D. Mg và Fe.
Đáp án B
2Fe(OH)2 + ½ O2 → t 0 Fe2O3 + 2H2O
Vậy chất rắn gồm: MgO, Fe2O3
Đúng 0
Bình luận (0)
Nung hỗn hợp gồm Mg(OH)2 và Fe(OH)2 ngoài không khí cho đến khi khối lượng không đổi thu được chất rắn có thành phần là A. Mg và FeO. B. MgO và FeO. C. MgO và Fe2O3. D. Mg và Fe.
Đọc tiếp
Nung hỗn hợp gồm Mg(OH)2 và Fe(OH)2 ngoài không khí cho đến khi khối lượng không đổi thu được chất rắn có thành phần là
A. Mg và FeO.
B. MgO và FeO.
C. MgO và Fe2O3.
D. Mg và Fe.
Đáp án C
Mg(OH)2 → t 0 MgO + H2O
2Fe(OH)2 + ½ O2 → t 0 Fe2O3 + 2H2O
Vậy chất rắn gồm: MgO, Fe2O3
Đúng 0
Bình luận (0)
Nung nóng hỗn hợp gồm Mg(OH)2 và Fe(OH)2 ngoài không khí đến khối lượng không đổi thì chất rắn thu được gồm:
A. MgO, FeO
B. Fe, MgO
C. MgO, Fe2O3
D. Mg, Fe2O3
Đáp án C
Mg(OH)2 → t o MgO + H2O
2Fe(OH)2 + 0,5O2 → t o Fe2O3 + 2H2O
Đúng 0
Bình luận (0)
Nung hỗn hợp Fe(OH)2, FeO, Fe(OH)3, Fe2O3, Fe3O4 , Fe(NO3)2, Fe(NO3)3 trong không khí đến khối lượng không đổi thu được chất rắn A. Chất rắn A là A. Fe2O3 B. FeO, Fe2O3 C. Fe2O3, Fe3O4 D. FeO, Fe3O4
Đọc tiếp
Nung hỗn hợp Fe(OH)2, FeO, Fe(OH)3, Fe2O3, Fe3O4 , Fe(NO3)2, Fe(NO3)3 trong không khí đến khối lượng không đổi thu được chất rắn A. Chất rắn A là
A. Fe2O3
B. FeO, Fe2O3
C. Fe2O3, Fe3O4
D. FeO, Fe3O4
Đáp án A
2Fe(OH)3 → t o Fe2O3 + 3H2O
4Fe(OH)2 + O2 → t o 2Fe2O3 + 4H2O
FeO, Fe3O4 + O2 → Fe2O3
Fe(NO3)2, Fe(NO3)3 → Fe2O3
=> chất rắn A. Fe2O3
Chú ý:
nhiệt phân trong không khí =>Các oxit sắt chuyển hết thành Fe2O3
Đúng 0
Bình luận (0)
Khi nung hỗn hợp các chất
F
e
(
N
O
3
)
2
,
F
e
(
O
H
)
2
và
F
e
C
O
3
trong không khí đến khối lượng không đổi, thu được một chất rắn là A....
Đọc tiếp
Khi nung hỗn hợp các chất F e ( N O 3 ) 2 , F e ( O H ) 2 và F e C O 3 trong không khí đến khối lượng không đổi, thu được một chất rắn là
A. F e 3 O 4 .
B. FeO.
C. Fe.
D. F e 2 O 3 .
Nung hỗn hợp các chất Fe(NO3)2, Fe(OH)3 và FeCO3 trong không khí đến khối lượng không đổi thu được một chất rắn là: A. FeO B. Fe3O4 C. Fe D. Fe2O3
Đọc tiếp
Nung hỗn hợp các chất Fe(NO3)2, Fe(OH)3 và FeCO3 trong không khí đến khối lượng không đổi thu được một chất rắn là:
A. FeO
B. Fe3O4
C. Fe
D. Fe2O3
Đáp án D
Các phản ứng xảy ra:
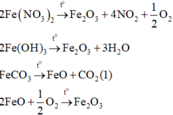
Vì sau phản ứng chỉ thu được MỘT chất rắn nên chất rắn đó phải là Fe2O3 (khi đó lượng O2 sinh ra từ phản ứng nhiệt phân Fe(NO3)2 đủ để oxi hóa hết lượng FeO sinh ra từ phản ứng (1)).
Đúng 0
Bình luận (0)