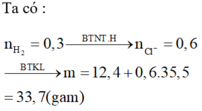Hòa tan 6,5 gam Zn trong dung dịch axit HCl dư, sau phản ứng cô cạn dung dịch thì số gam muối khan thu được là (Cho H = 1, Zn = 65, Cl = 35,5) ?

Những câu hỏi liên quan
Hoà tan 6,5 gam Zn trong dung dịch axit HCl dư, sau phản ứng cô cạn dung dịch thu được một lượng muối khan. Hãy tính lượng muối khan đó.
Phương trình hóa học của phản ứng:
Zn + 2HCl → ZnCl 2 + H 2
n Zn = 6,5/65 = 0,1 mol
Khối lượng muối thu được là: 0,1 x (65 +71) = 13,6g
Đúng 0
Bình luận (0)
Cho kim loại Kẽm tan hết trong dung dịch axit HCl. Sau phản ứng thu được 27,2 gam muối. Khối lượng Zn đã phản ứng là:
(Cho Zn = 65; H = 1; Cl = 35,5)
Zn+2HCl->ZnCl2+H2
0,2--------------0,2
n ZnCl2=27,2\136=0,2 mol
=>m Zn=0,2.65=13g
Đúng 0
Bình luận (0)
Hòa tan 6,5g Zn vào dung dịch axit HCl dư, sau phản ứng cô cạn dung dịch thu được 1 lượng muối khan. Hãy tính lượng muối khan đó
\(Zn+2HCl->ZnCl_2+H_2\)
n Zn = n ZnCl2 = 6,5:65=0,1 mol
m ZnCl2 = 0,1.(65+35,5.2)=13,6 g
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn hỗn hợp chứa 7,2 (gam) Mg và 6,5 (gam) Zn vào axit HCl thì thu được dung dịch Y. Cô cạn dung dịch Y thu được m (gam) muối khan. Tìm giá trị của m.
m = 7,2 (gam).
m = 13,7 (gam).
m = 6,5 (gam).
m = 42,1 (gam).
\(n_{Mg}=0,3\left(mol\right);n_{Zn}=0,1\left(mol\right)\)
PTHH:
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(Mg+2HCl\rightarrow ZnCl_2+H_2\)
\(\Rightarrow n_{MgCl_2}=n_{Mg}=0,3\left(mol\right)\)
\(n_{ZnCl_2}=n_{Zn}=0,1\left(mol\right)\)
\(\Rightarrow m=0,3.95+0,1.136=42,1\left(g\right)\)
Đúng 1
Bình luận (0)
Hòa tan 6,5 gam kẽm vừa đủ trong 100 gam dung dịch axit clohidric.(Biết: Zn = 65; H =1; Cl = 35,5).Nồng độ phần trăm của dung dịch muối tạo thành bằng bao nhiêu?
\(PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\ \Rightarrow n_{ZnCl_2}=n_{Zn}=n_{H_2}=0,1\left(mol\right);n_{HCl}=2n_{Zn}=0,2\left(mol\right)\\ \Rightarrow\left\{{}\begin{matrix}m_{ZnCl_2}=0,1\cdot136=13,6\left(g\right)\\m_{H_2}=0,1\cdot2=0,2\left(mol\right)\\m_{dd_{ZnCl_2}}=6,5+100-0,2=106,3\left(g\right)\end{matrix}\right.\\ \Rightarrow C\%_{ZnCl_2}=\dfrac{13,6}{106,3}\cdot100\%\approx12,8\%\)
Đúng 1
Bình luận (0)
Để hòa tan m gam kẽm cần vừa đủ 50 gam dung dịch HCl 7,3 %
a/ Viết PTPƯ
b/ Tính m
c/ Tính thể tích khí thu được ở đktc?
d/ Tính khối lượng muối tạo thành sau phản ứng ?
( Biết Zn = 65 , H = 1, Cl = 35,5 )
\(m_{HCl}=50.7,3\%=3,65\left(g\right)\\ n_{HCl}=\dfrac{3,65}{36,5}=0,1\left(mol\right)\\ PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{Zn}=n_{H_2}=n_{ZnCl_2}=\dfrac{1}{2}n_{HCl}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\\ m_{Zn}=0,05.65=3,25\left(g\right)\\ V_{H_2\left(ĐKTC\right)}=0,05.22,4=1,12\left(l\right)\\ m_{ZnCl_2}=0,05.136=6,8\left(g\right)\)
Đúng 4
Bình luận (0)
mHCl=50.7,3%=3,65(g) -> nHCl=0,1(mol)
a) PTHH: Zn + 2 HCl -> ZnCl2 + H2
nH2=nZnCl2=nZn=nHCl/2= 0,1/2=0,05(mol)
b) m=mZn=0,05.65=3,25(g)
c) V(H2,đktc)=0,05.22,4=1,12(l)
d) mZnCl2= 136.0,05= 7,8(g)
Đúng 2
Bình luận (1)
Hòa tan 12.4 gam hỗn hợp X gồm Mg, Na, Zn trong dung dịch HCl. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y và 6.72 lít H2 (dktc). Cô cạn toàn bộ dung dịch Y thu được m gam muối khan. Giá trị của m là A.33,7 B. 34,3 C. 23,05 D. 23,35
Đọc tiếp
Hòa tan 12.4 gam hỗn hợp X gồm Mg, Na, Zn trong dung dịch HCl. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y và 6.72 lít H2 (dktc). Cô cạn toàn bộ dung dịch Y thu được m gam muối khan. Giá trị của m là
A.33,7
B. 34,3
C. 23,05
D. 23,35
Hòa tan hoàn toàn 5,65 gam hỗn hợp Mg và Zn trong dung dịch HCl dư, thu được 3,36 lít (đktc) khí H2 và dung dịch X. Cô cạn dung dịch X, được m gam muối khan. Giá trị m là:
A. 16,3
B. 21,95
C. 11,8
D. 18,10
Chọn đáp án A
Mg + 2HCl → MgCl2 + H2↑ || Zn + 2HCl → ZnCl2 +H2↑.
nH2↑ = 0,15 mol ⇒ nCl− trong muối = 2nH2 = 0,3 mol.
||→ m = mmuối = mkim loại + mCl− = 5,65 + 0,3 × 35,5 = 16,3 gam. Chọn A.
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 5,65 gam hỗn hợp Mg và Zn trong dung dịch HCl dư, thu được 3,36 lít (đktc) khí H2 và dung dịch X. Cô cạn dung dịch X, được m gam muối khan. Giá trị m là:
A. 16,3
B. 21,95
C. 11,8
D. 18,10
Chọn đáp án A
Mg + 2HCl → MgCl2 + H2↑ || Zn + 2HCl → ZnCl2 +H2↑.
nH2↑ = 0,15 mol ⇒ nCl- trong muối = 2nH2 = 0,3 mol.
||→ m = mmuối = mkim loại + mCl- = 5,65 + 0,3 × 35,5 = 16,3 gam. Chọn A
Đúng 0
Bình luận (0)