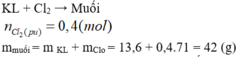Đốt cháy 13,6g hỗn hợp Mg,Fe trong bình khí Clo dư.sau phản ứng thấy thể tích khí Clo Giảm 8,96 lít .tính khối lựng muối clo khan

Những câu hỏi liên quan
đốt cháy hết 13,6g hỗn hợp Mg,Fe trong bình khí Clo dư, sau phản ứng thấy thể tích khí Clo giảm 8,96 lít. Khối lượng muối clorua khan thu được là ?
\(n_{Cl_2\ pư} = \dfrac{8,96}{22,4} = 0,4(mol)\)
Bảo toàn khối lượng :
\(m_{muối} = m_{hỗn\ hợp} + m_{Cl_2} = 13,6 + 0,4.71 = 42(gam)\)
Đúng 4
Bình luận (0)
\(m_{Cl_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(BTKL:m_{hh}+m_{Cl_2}=m_{Muối}\)
\(\Leftrightarrow13.6+0.4\cdot71=m_{Muối}\)
\(\Leftrightarrow m_{Muối}=42\left(g\right)\)
Chúc bạn học tốt !!!
Đúng 2
Bình luận (0)
Ta có: \(n_{Cl_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(\Rightarrow n_{Cl\left(trongmuoi\right)}=2n_{Cl_2}=0,8\left(mol\right)\)
Có: mmuối = mKL + mCl = 13,6 + 0,8.35,5 = 42 (g)
Bạn tham khảo nhé!
Đúng 3
Bình luận (0)
Xem thêm câu trả lời
Đốt cháy hết 13,6g hỗn hợp Mg, Fe trong bình khí clo dư, sau phản ứng thấy thể tích khí clo giảm 8,96 lít. Khối lượng muối clorua khan thu được là : A. 65,0 g B. 38,0 g C. 50,8 g D. 42,0 g
Đọc tiếp
Đốt cháy hết 13,6g hỗn hợp Mg, Fe trong bình khí clo dư, sau phản ứng thấy thể tích khí clo giảm 8,96 lít. Khối lượng muối clorua khan thu được là :
A. 65,0 g
B. 38,0 g
C. 50,8 g
D. 42,0 g
Đốt cháy hết 13,6 gam hỗn hợp Mg,Fe trong bình khí clo dư sau phản ứng thấyThể tích khí clo giảm 8,96l. khối lượng muối clorua khan thu được là?
hoá 10
Câu 56: Đốt cháy hỗn hợp bột Al và Mg trong bình dụng khi Clo dư, sau khi phản ứng xảy ra hoàn toàn thấy khối lượng chất rắn trong bình tăng 4,26 gam. Thể tích khí Clo đã phản ứng ở đktc là? A. 1,344 lit B. 13,44 lit C. 2,688 lit. D. 26,88 lit
mtăng = mCl2 = 4.26 (g)
nCl2 = 4.26 / 71 = 0.06 (mol)
VCl2 = 0.06 * 22.4 = 1.344 (l)
=> A
Đúng 2
Bình luận (1)
mtăng = mCl2 = 4.26 (g)
nCl2 = 4.26 / 71 = 0.06 (mol)
VCl2 = 0.06 * 22.4 = 1.344 (l)
=> A
Đúng 0
Bình luận (0)
Đốt cháy 11,2 g kim loại Fe trong khí Clo thủ được FeCl3 Tính thể tích khí Clo cần dùng cho phản ứng
PTHH: \(2Fe+3Cl_2\xrightarrow[]{t^o}2FeCl_3\)
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Theo PTHH: \(n_{Cl_2}=\dfrac{0,2.3}{2}=0,3\left(mol\right)\)
\(\Rightarrow V_{Cl_2}=n_{Cl_2}.22,4=0,3.22,4=6,72\left(l\right)\)
Đúng 3
Bình luận (0)
Số molcuar Fe là:
\(n_{Fe}=\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(PTHH:Fe+3Cl\xrightarrow[]{t^0}FeCl_3\)
tỉ lệ : 1 3 1
số mol : 0,2 0,6 0,2
Thể tích khí Cl cần dùn cho phản ứng là:
\(V_{Cl}=n_{Cl}.22,4=0,6.22,4=13,44\left(l\right)\)
Đúng 1
Bình luận (3)
Câu 1: cho 2,24 lít khí clo phản ứng với Na. Tính khối lượng muối thu được( Na=23, Cl=35,5)
Câu 2: Hòa tan hoàn toàn 1,45g hỗn hợp 3 kim loại Zn,Mg, Fe bằng dung dịch HCl dư thấy thoát ra 0,896 lít khí (đktc). Tính khối lượng muối khan thu được sau phản ứng.
Câu 1:
PTHH: \(Na+\dfrac{1}{2}Cl_2\xrightarrow[]{t^o}NaCl\)
Ta có: \(n_{NaCl}=2n_{Cl_2}=2\cdot\dfrac{2,24}{22,4}=0,2\left(mol\right)\)
\(\Rightarrow m_{NaCl}=0,2\cdot58,5=11,7\left(g\right)\)
Đúng 2
Bình luận (0)
Câu 2:
Ta có: \(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\) \(\Rightarrow m_{H_2}=0,04\cdot2=0,08\left(g\right)\)
Bảo toàn nguyên tố: \(n_{HCl}=2n_{H_2}=0,08\left(mol\right)\) \(\Rightarrow m_{HCl}=0,08\cdot36,5=2,92\left(g\right)\)
Bảo toàn khối lượng: \(m_{muối}=m_{KL}+m_{HCl}-m_{H_2}=4,29\left(g\right)\)
Đúng 3
Bình luận (0)
Câu 2 :
nH2 = 0.896 / 22.4 = 0.04 (mol)
nHCl = 2nH2 = 0.04 * 2 = 0.08 (mol)
mHCl = 0.08 * 36.5 =2.92 (g)
BTKL :
mM = mKl + mHCl - mH2 = 1.45 + 2.92 - 0.04*2 = 4.29 (g)
Đúng 2
Bình luận (0)
Đốt cháy kim loại R trong bình chứa khí clo, thu được 32,5 gam muối. Thể tích khí clo đã phản ứng là 6,72 lít (ở đktc). Kim loại R là
A. Fe
B. Mg
C. Cu
D. Al
Đốt cháy hết 12gam kim loại magie (Mg) trong bình chứa đầy khí clo CL2, thu được 47,5 gam magie clorua MgCL2 A)viết công thức của phản ứng xảy ra B)tính khối lượng khí clo đã phản ứng
P/ứng hóa học: \(Mg+Cl_2->MgCl_2\)
Công thức của p/ứng có phải CT về khối lượng không nhỉ? Mình chưa hiểu lắm. Nếu là CT về kh lượng thì:
\(m_{Mg}+m_{Cl_2}=m_{MgCl_2}\)
* Khối lượng khí clo đã p/ứ:
Theo ĐLBTKL:
\(m_{Mg}+m_{Cl_2}=m_{MgCl_2}\\ =>12g+m_{Cl_2}=47,5g\\ =>m_{Cl_2}=47,5g-12g=35,5g\)
Vậy có 35,5g khí Clo tham gia p/ứng.
Đúng 0
Bình luận (0)
Đốt 16,8 g Fe trong bình đựng khí clo. Thể tích khí clo (đktc) tham gia phản ứng là:
A. 4,48
B.10,08
C. 2,24
D. 8,96
Đáp án B
nFe = 0,3 (mol)
2Fe + 3Cl2→ 2FeCl3
0,3 0,45 (mol)
V = 0,45.22,4 = 10,08 (l)
Đúng 0
Bình luận (0)