bài 1: Hòa tan 10,4 gam hỗn hợp Fe và Mg trong dung dịch chứa 25,55 gam HCl.
a/ Viết PTHH.
b/ Chứng minh HCl đã dùng dư.
bài 2: Hòa tan 11 gam hỗn hợp Fe và Al trong dung dịch chứa 68,6 gam H2SO4.
a/ Viết PTHH.
b/ Chứng minh H2SO4 đã dùng dư.
Hòa tan 10,4 gam hỗn hợp Fe và Ca trong dung dịch chứa 25,55 gam HCl.
a/ Viết PTHH.
b/ Chứng minh HCl đã dùng dư.
Gọi \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Ca}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow56x+40y=10,4\left(1\right)\)
\(n_{HCl}=\dfrac{25,55}{36,5}=0,7mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(Ca+2HCl\rightarrow CaCl_2+H_2\uparrow\)
\(\Rightarrow2x+2y=0,7\left(2\right)\)
Tư (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=-0,225mol\\y=0,575mol\end{matrix}\right.\)
Kết quả âm![]()
Hòa tan hết 39,8 gam hỗn hợp bột kim loại Mg, Al, Zn, Fe cần dùng 800ml dung dịch hỗn hợp HCl 1M và H2SO4 1M (vừa đủ), thu được dung dịch X chứa m gam muối. giá trị của m là
A. 72,5.
B. 155,0.
C. 145,0.
D. 125,0.
Giải thích: Đáp án C
nHCl = 0,8.1 = 0,8 (mol) ; nH2SO4 = 0,8 (mol)
Vì phản ứng vừa đủ => mmuối = mKL + mCl- + mSO42- = 39,8 + 0,8.35,5 + 0,8.96 = 145 (g)
Hòa tan hết 16,0 gam hỗn hợp X gồm Mg, MgO, Fe và FeO trong dung dịch H2SO4 loãng (vừa đủ), thu được dung dịch chứa 49,6 gam muối. Nếu hòa tan hết 16,0 gam X trên cần dùng dung dịch chứa xmol HCl và y mol H2SO4, thu được 6,72 lít khí H2 (đktc) và dung dịch chứa 45,6 gam muối. Tỉ lệ của x : y là
A. 8:5
B. 2:3
C. 4:5
D. 5:3
Chọn đáp án A.
Đặt nMg = a, nFe = b và nO = c
Ta có:
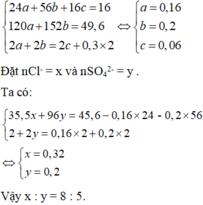
Hòa tan hoàn toàn 10,4 gam hỗn hợp gồm Fe và Mg trong dung dịch HCl (dư), thu được 6,72 lít khí H2 (đktc) và dung dịch chứa m gam muối. Giá trị của m là
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
______a---------------->a------>a
Mg + 2HCl --> MgCl2 + H2
b----------------->b------->b
=> \(\left\{{}\begin{matrix}56a+24b=10,4\\a+b=0,3\end{matrix}\right.=>\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}m_{FeCl_2}=0,1.127=12,7\left(g\right)\\m_{MgCl_2}=0,2.95=19\left(g\right)\end{matrix}\right.\)
=> mmuối = 12,7 + 19 = 31,7(g)
Hòa tan hoàn toàn 3,02 gam hỗn hợp X chứa Al, Fe, Mg trong 200 ml dung dịch hỗn hợp chứa HCl 0,6M và H2SO4 0,3M. Sau phản ứng thu được 1,792 lít khí H2 (đktc). Cô cạn dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là?
A. 9,7 gam
B. 10,2 gam
C. 9,4 gam
D. 10,6 gam
Hòa tan hoàn toàn 3,02 gam hỗn hợp X chứa Al, Fe, Mg trong 200 ml dung dịch hỗn hợp chứa HCl 0,6M và H2SO4 0,3M. Sau phản ứng thu được 1,792 lít khí H2 (đktc). Cô cạn dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là?
A. 9,7 gam
B. 10,2 gam
C. 9,4 gam
D. 10,6 gam
Hòa tan hoàn toàn 3,02 gam hỗn hợp X chứa Al, Fe, Mg trong 200 ml dung dịch hỗn hợp chứa HCl 0,6M và H2SO4 0,3M. Sau phản ứng thu được 1,792 lít khí H2 (đktc). Cô cạn dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là
A. 9,7 gam
B. 10,2 gam
C. 9,4 gam
D. 10,6 gam
Hòa tan 12,12 gam hỗn hợp gồm Fe, Al trong dung dịch chứa 0,1 mol HNO3 và 0,41 mol H2SO4 thu được 6,272 lít (đktc) hỗn hợp khí Y gồm H2 và NO và dung dịch Z chỉ chứa m gam muối và thấy có 1,12 gam chất rắn không tan. Phần trăm khối lượng của Fe trong hỗn hợp ban đầu gần nhất là:
A. 44,56%
B. 49,12%
C. 50,88%
D. 55,44%
Hoà tan hết 10,4 gam hỗn hợp gồm Mg và Fe cần dùng m gam dung dịch H2SO4 10%. Sau phản ứng thu
được dung dịch X và 6,72 lít H2(đktc).
1.Viết các PTPU ?
2.Tính m? Tính % khối lượng Mg trong hỗn hợp ban đầu?
PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
a______________________a (mol)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b_____________________b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}24a+56b=10,4\\a+b=\dfrac{6,72}{22,4}=0,3\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,2\cdot24}{10,4}\cdot100\%\approx46,15\%\\m_{ddH_2SO_4}=\dfrac{\left(0,2+0,1\right)\cdot98}{10\%}=294\left(g\right)\end{matrix}\right.\)