Bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì
Nội dung lý thuyết
I. Thành phần của các oxide và hydroxide
Hóa trị cao nhất của các nguyên tố nhóm A trong hợp chất với oxygen tăng từ I đến VII khi đi từ trái qua phải trong một chu kì (trừ chu kì 1 và nguyên tố fluorine ở chu kì 2), do đó thành phần của các oxide và hydroxide có sự lặp lại theo chu kì.
Công thức oxide, hydroxide với hóa trị cao nhất ở chu kì 2, 3
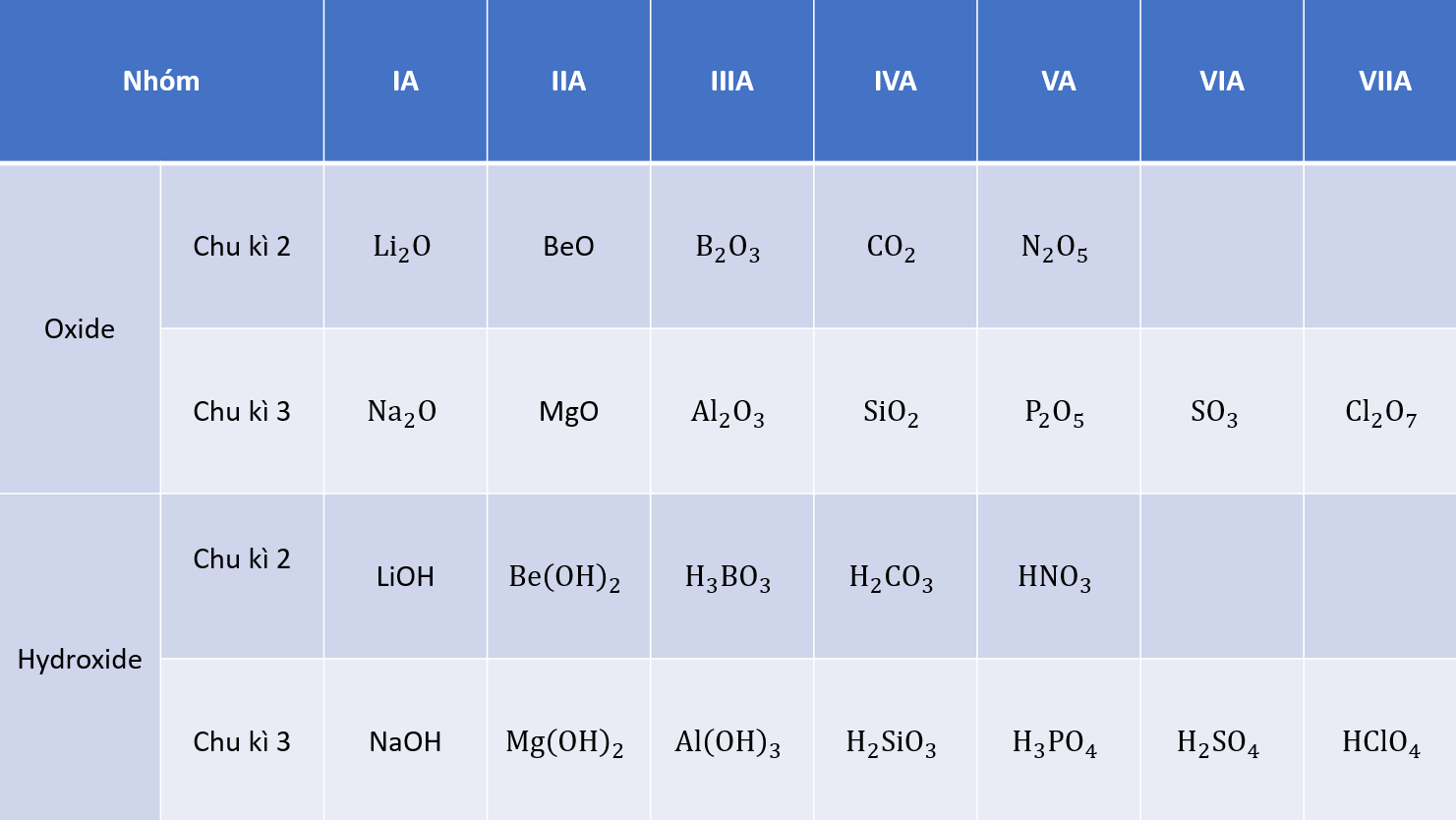
@2026846@
II. Tính chất của oxide và hydroxide
1. Phản ứng của oxide với nước
Trong một thí nghiệm, cho các oxide \(Na_2O,MgO,P_2O_5\) vào nước, nhúng giấy quỳ tím vào dung dịch sau phản ứng. Hiện tượng phản ứng được trình bày trong bảng sau:
| Oxide | Hiện tượng |
| \(Na_2O\) | Tan hoàn toàn trong nước. Quỳ tím chuyển màu xanh đậm. |
| \(MgO\) | Tan một phần trong nước. Quỳ tím chuyển màu xanh nhạt. |
| \(P_2O_5\) | Tan hoàn toàn trong nước. Quỳ tím chuyển màu đỏ. |
Phương trình phản ứng:
\(Na_2O+H_2O\rightarrow2NaOH\)
\(MgO+H_2O\rightarrow Mg\left(OH\right)_2\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
2. Phản ứng của muối với dung dịch acid
Chuẩn bị: dung dịch \(Na_2CO_3\) vào ống nghiệm chứa dung dịch \(HNO_3\).
Hiện tượng:sủi bọt khí \(CO_2\)
Phương trình phản ứng: \(Na_2CO_3+2HNO_3\rightarrow2NaNO_3+CO_2+H_2O\)
Các oxide khi tác dụng với nước tạo thành hydroxide có tính base hoặc acid. Nói chung, hydroxide của các nguyên tố nhóm IA thể hiện tính base mạnh, hydorxide ứng với hóa trị cao nhất của các nguyên tố nhóm VIIA (trừ fluorine) thể hiện tính acid mạnh.
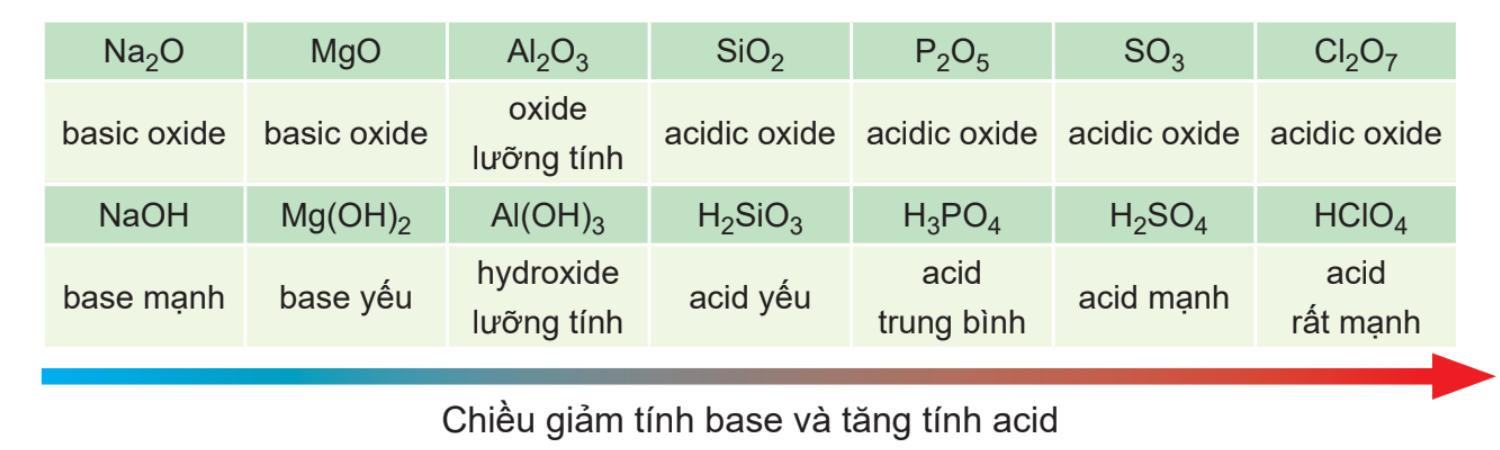
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính base của oxide và hydroxide tương ứng giảm dần, đồng thời tính acid của chúng tăng dần.
@2026945@@2027019@
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!