Đốt cháy hoàn toàn m gam hỗn hợp khí A gồm CO, H2, CH4, C4H10 cần dùng 21,28 lít O2 (đktc) thì thu được 28,6 gam CO2 và 14,4 gam H2O.
a. Tính m.
b. Tính phần trăm khối lượng của CO trong hỗn hợp A.
Ai giúp mình giải với ạ mình xin cảm ơn
Hôn hợp Y gồm CH4 và C2H6.Đốt cháy hoàn toàn 6,72 lít (đktc) hỗn hợp Y bằng khí O2 thu được 14,4 gam H2O.
a) Tính % thể tích của mỗi khí trong hỗn hợp.
b) Tính thể tích khí O2 cần lấy. Biết đã dùng dư 10% so với lượng cần thiết.
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_6}=y\left(mol\right)\end{matrix}\right.\)
\(n_{H_2O}=\dfrac{14,4}{18}=0,8\left(mol\right)\)
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
x-------->2x----------->2x
\(C_2H_6+\dfrac{7}{2}O_2\underrightarrow{t^o}2CO_2+3H_2O\)
y-------->3,5y------------->3y
Có hệ phương trình: \(\left\{{}\begin{matrix}x+y=\dfrac{6,72}{22,4}=0,3\\2x+3y=0,8\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
a
\(\%V_{CH_4}=\dfrac{0,1.22,4.100\%}{6,72}=33,33\%\)
\(\%V_{C_2H_6}=\dfrac{0,2.22,4.100\%}{6,72}=66,67\%\)
b
\(V_{O_2}=\left(2x+3,5y\right).22,4=\left(2.0,1+3,5.0,2\right).22,4=20,16\left(l\right)\)
Cho dữ liệu dư 10% như thế thì phải hỏi là V khí \(O_2\) đã lấy/ đã dùng chứ "cần lấy" là theo PTHH (không cần cho "Biết ...")
\(V_{O_2.đã.lấy}=\dfrac{20,16.\left(100+10\right)\%}{100\%}=22,176\left(l\right)\)
Làm giúp em câu b với ạ, em cảm ơn
Đốt cháy hoàn toàn m gam hỗn hợp gồm C2H2, CH4,C2H6, C4H10. sau phản ứng thu được 8,96 lít khí CO2 và 10,8 gam H2O.
a. tính m?
b. tính v không khí cần dùng để đốt cháy hết hỗn hợp trên? Biết Oxi chiếm 20% thể tích không khí
help me !!!!![]()
a, Ta có: \(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\Rightarrow n_H=0,6.2=1,2\left(mol\right)\)
m = mC + mH = 0,4.12 + 1,2.1 = 6 (g)
b, Theo ĐLBT KL, có: m + mO2 = mCO2 + mH2O
⇒ mO2 = 22,4 (g) \(\Rightarrow n_{O_2}=\dfrac{22,4}{32}=0,7\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,7.22,4=15,68\left(g\right)\)
\(\Rightarrow V_{kk}=\dfrac{15,68}{20\%}=78,4\left(g\right)\)
Đốt cháy hoàn toàn 7,4 gam hỗn hợp CH4 và C4H10 trong không khí biết rằng sau phản ứng thu được 22 gam khí CO2.
a. Tính khối lượng các chất có trong hỗn hợp đầu ?
b. Tính VO2 cần dùng ( đktc) để đốt cháy hết hỗn hợp trên?
\(a,Đặt:n_{CH_4}=a\left(mol\right);n_{C_4H_{10}}=b\left(mol\right)\left(a,b>0\right)\\ PTHH:CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\\ 2C_4H_{10}+13O_2\rightarrow\left(t^o\right)8CO_2+10H_2O\\ \Rightarrow\left\{{}\begin{matrix}16a+58b=7,4\\22,4a+22,4.4b=22\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}m_{CH_4}=0,1.16=1,6\left(g\right)\\m_{C_4H_{10}}=0,1.58=5,8\left(g\right)\end{matrix}\right.\\ b,n_{O_2}=2a+\dfrac{13}{2}b=2.0,1+6,5.0,1=0,85\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,85.22,4=19,04\left(l\right)\)
a) PTHH: \(2CO+O_2\underrightarrow{t^o}2CO_2\) (1)
\(4H_2+O_2\underrightarrow{t^o}2H_2O\) (2)
b) Ta có: \(\left\{{}\begin{matrix}\Sigma n_{O_2}=\dfrac{9,6}{32}=0,3\left(mol\right)\\n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{O_2\left(1\right)}=0,1mol\\n_{O_2\left(2\right)}=0,2mol\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{CO}=0,1\cdot28=2,8\left(g\right)\\m_{H_2}=0,2\cdot2=0,4\left(g\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}\%m_{CO}=\dfrac{2,8}{2,8+0,4}\cdot100\%=87,5\%\\\%m_{H_2}=12,5\%\end{matrix}\right.\)
c) PTHH: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
Theo PTHH: \(n_{KMnO_4}=2n_{O_2}=0,6mol\)
\(\Rightarrow m_{KMnO_4}=0,6\cdot158=94,8\left(g\right)\)
Hỗn hợp khí A gồm C2H2, CH4 và H2. Dẫn m gam hỗn hợp A vào bình kín chứa chất xúc tác Ni, rồi đun nóng. Sau một thời gian thu được hỗn hợp khí B gồm CH4, C2H4, C2H6, C2H2 và H2. Dẫn toàn bộ lượng khí B vào dung dịch brom ( dư) thấy khối lượng bình đựng brom tăng 4,1 gam và thoát ra hỗn hợp khí D. Đốt cháy hoàn toàn D cần dùng 9,52 lít khí O2 (đktc), thu được sản phẩm cháy gồm CO2 và 8,1 gam H2O.
Viết các phương trình phản ứng xảy ra và tính m.
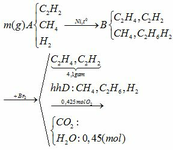
C2H2 + H2 C2H4
C2H2 + H2 C2H6
Khi cho hỗn hợp B qua dd nước Br2 chỉ có C2H4 và C2H2 phản ứng C2H2 +2Br2 → C2H2Br4
C2H4 + Br2 → C2H4Br2
=> khối lượng bình Br2 tăng chính bằng khối lượng của C2H2 và C2H4
mC2H2 + mC2H4 = 4,1 (g)
Hỗn hợp khí D đi ra là CH4, C2H6 và H2
CH4 + 2O2 → t ∘ CO2 + 2H2O
C2H6 + O2 → t ∘ 2CO2 + 3H2O
2H2 + O2 → t ∘ 2H2O
Bảo toàn nguyên tố O cho quá trình đốt cháy hh D ta có:
2nCO2 = 2nO2 – nH2O => nCO2 = ( 0,425. 2– 0,45)/2 = 0,2 (mol)
Bảo toàn khối lượng : mhh D = mCO2 + mH2O – mO2 = 0,2.44 + 0,45.18 – 0,425.32 = 3,3 (g)
Bảo toàn khối lương: mA = (mC2H2 + mC2H4) + mhh D = 4,1 + 3,3 = 7,4 (g)
Tiến hành cracking 22,4 lít khí C4H10 (ở đktc) thu được hỗn hợp A gồm CH4, C2H6, C2H4, C3H6, C4H8, H2 và C4H10 dư. Đốt cháy hoàn toàn A thu được x gam CO2 và y gam H2O. Tính giá trị của x và y.
A. x = 176 gam, y = 90 gam
B. x = 76 gam, y = 90 gam
C. x = 160 gam, y = 90 gam
D. x = 76 gam, y = 190 gam
đôt cháy hoàn toàn hỗn hợp khí gồm co và h2 cần dùng 6,72 lít khí o2.thu được 4,48 lít co2.tính phần trăm theo khối lượng và thể tích của hỗn hợp ban đầu
\(2CO + O_2 \xrightarrow{t^o} 2CO_2(1)\\ 2H_2 + O_2 \xrightarrow{t^o} 2H_2O(2)\\ n_{CO} = n_{CO_2} = \dfrac{4,48}{22,4} = 0,2(mol)\\ n_{O_2(1)} = \dfrac{n_{CO_2}}{2} = 0,1(mol)\\ \Rightarrow n_{H_2} = 2n_{O_2(2)} = 2.(\dfrac{6,72}{22,4}-0,1)=0,4(mol)\\ \%V_{CO} = \dfrac{0,2}{0,2+0,4}.100\% = 33,33\%\\ \%V_{H_2} = 100\% -33,33\% = 66,67\%\)
\(\%m_{CO} = \dfrac{0,2.28}{0,2.28+0,4.2}.100\% = 87,5\%\\ \%m_{H_2} = 100\% - 87,5\% = 12,5\%\)
Đốt cháy hoàn toàn gam hỗn hợp X gồm CH4, C3H6, C4H10 cần dùng vừa đủ V lít không khí (gồm 20% thể tích O2 và 80% thể tích N2) thu được 26,4 gam CO2 và 13,5 gam H2O a) Viết PTHH b) Tính a và V
nO (trong CO2) = 2 . nCO2 = 2 . 26,4/44 = 1,2 (mol)
nO (trong H2O) = nH2O = 13,5/18 = 0,75 (mol)
nO (trong O2) = 1,2 + 0,75 = 1,95 (mol)
nO2 = 1,95/2 = 0,975 (mol)
VO2 = 0,975 . 22,4 = 21,84 (l)
Vkk = 21,84 . 5 = 109,2 (l)
nO (trong CO2) = 2 . nCO2 = 2 . 26,4/44 = 1,2 (mol)
nO (trong H2O) = nH2O = 13,5/18 = 0,75 (mol)
nO (trong O2) = 1,2 + 0,75 = 1,95 (mol)
nO2 = 1,95/2 = 0,975 (mol)
VO2 = 0,975 . 22,4 = 21,84 (l)
Vkk = 21,84 . 5 = 109,2 (l)
nCO2 = 8.8/44 = 0.2 (mol)
nO2 = 9.6/32 = 0.3 (mol)
2CO + O2 -to-> 2CO2
0.2____0.1______0.2
2H2 + O2 -to-> 2H2O
0.4___0.3-0.1
%CO = 0.2*28 / ( 0.2*28 + 0.4*2) * 100% = 87.5%
%H2 = 12.5%
=> D
\(2CO + O_2\xrightarrow{t^o} 2CO_2(1)\\ n_{CO} = n_{CO_2} = \dfrac{8,8}{44} = 0,2(mol)\\ n_{O_2(1)} = \dfrac{n_{CO_2}}{2} = 0,1(mol)\\ 2H_2 +O_2 \xrightarrow{t^o} 2H_2O(2)\\ n_{H_2} = 2n_{O_2(2)} = 2.(\dfrac{9,6}{32}-0,1) = 0,4(mol)\\ \Rightarrow \%m_{CO} = \dfrac{0,2.28}{0,2.28 + 0,4.2}.100\% = 87,5\%\\ \%m_{H_2} = 100\% - 87,5\% = 12,5\%\)
PTHH: \(2CO+O_2\underrightarrow{t^o}2CO_2\) (1)
\(2H_2+O_2\underrightarrow{t^o}2H_2O\) (2)
Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\\n_{O_2}=\dfrac{9,6}{32}=0,3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{CO}=0,2\left(mol\right)\\n_{H_2}=0,4\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{CO}=0,2\cdot28=5,6\left(g\right)\\m_{H_2}=0,4\cdot2=0,8\left(g\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}\%m_{CO}=\dfrac{5,6}{5,6+0,8}\cdot100\%=87,5\%\\\%m_{H_2}=12,5\%\end{matrix}\right.\)