Phức chất aqua của Ni2+ và Zn2+ đều có dạng hình học bát diện.
a) Viết công thức hoá học của mỗi phức chất aqua trên.
b) Mô tả sự hình thành liên kết giữa phối tử và nguyên tử trung tâm trong mỗi phức chất trên.
Trong một phản ứng hoá học, các chất phản ứng và chất tạo thành phải chứa cùng: *
A. Số nguyên tử của mỗi nguyên tố
B. Số liên kết giữa các nguyên tử trong mỗi chất
C. Số phân tử trong mỗi chất
D. Số lượng chất
A. Nhỏ hơn B. Lớn hơn C. Bằng D. Nhỏ hơn hoặc bằng
1. Cho các ký hiệu : Na; O; S;
a. Cho biết thành phần cấu tạo nguyên tử của các nguyên tố trên.
b. Viết cấu hình e và cho biết tính chất hoá học cơ bản của mỗi nguyên tố trên.
c. Xác định vị trí của mỗi nguyên tố trong bảng tuần hoàn.
Một hợp chất có phân tử gồm 2 nguyên tử N liên kết với 5 nguyên tử X và nặng hơn phân tử khí Oxi 3,375 lần a/ Tính phân tử khối của hợp chất b/ Tính ngtử khối của X, cho biết kí hiệu hóa học của ngtố X c/ Viết công thức hóa học của hợp chất d/Tính thành phần % khối lượng mỗi ngtố trong hợp chất
a,Ta có công thức chung của hợp chất là N2X5
phan tử khối của hợp chất là:3,375.32=108
b,ta có 14.2+X.5=108
X=16
vậy nguyên tử khối của X=16
KHHH là O
c,công thức hóa học của hợp chất là N2O5
d,thành phần phần trăm mỗi nguyen to trong hợp chất là
%Nito=(14.2.100):108=25,93%
%oxi=100%-25,93%=74,07%
a)Lập công thức hóa học của hợp chất tạo bởi C có hóa trị IV và O
b)Mô tả sự liên kết trong phân tử vừa lập ở câu a
\(a,\) Gọi ct chung: \(C^{IV}_xO^{II}_y\)
Theo qui tắc hóa trị: \(IV.x=y.II\Rightarrow\dfrac{x}{y}=\dfrac{II}{IV}=\dfrac{1}{2}\)
\(\Rightarrow x=1;y=2\)
\(\Rightarrow CTHH:CO_2\)
\(b,\) Khi hình thành phân tử Carbon dioxide, 2 nguyên tử O đã liên kết với 1 nguyên tử C bằng cách nguyên tử C góp chung 2 electron với mỗi nguyên tử O để tạo thành cặp electron dùng chung.
*Hình ảnh về cấu tạo của phân tử nhé.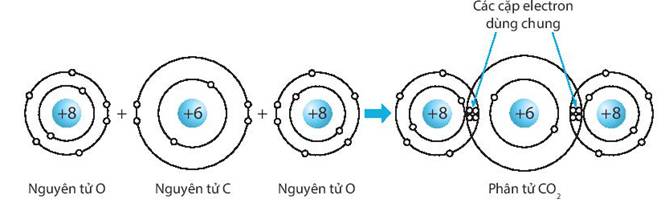
Cho các chất sau : Na2O, MgO, HBr, H2CO3, CaBr2.
Hãy xác định loại liên kết hóa học giữa các nguyên tử trong các phân tử trên. Viết sự hình thành của liên kết ion đối với hợp chất ion, viết công thứ electron và công thứ cấu tạo đối với hợp chất cộng hóa trị trong các phân tử trên. Xác định hóa trị của các nguyên tố trong các hợp chất trên.
Dựa vào hiệu độ âm điện, trong:
* Na2O: liên kết ion.
* MgO: liên kết ion.
* HBr: liên kết công hóa trị phân cực.
* CaBr2: liên kết ion.
Cho các chất sau : Na2O, MgO, HBr, H2CO3, CaBr2.
Hãy xác định loại liên kết hóa học giữa các nguyên tử trong các phân tử trên. Viết sự hình thành của liên kết ion đối với hợp chất ion, viết công thứ electron và công thứ cấu tạo đối với hợp chất cộng hóa trị trong các phân tử trên. Xác định hóa trị của các nguyên tố trong các hợp chất trên.
Khi nói về giai đoạn tiến hóa hóa học, có bao nhiêu phát biểu sau đây đúng?
(1) Trong giai đoạn tiến hóa hóa học, các chất vô cơ kết hợp với nhau hình thành nên các chất hữu cơ đôn giản rồi từ đó hình thành các chất hữu cơ phức tạp dưới tác động của các nguồn năng lượng tự nhiên (bức xạ nhiệt, tia tử ngoại,…).
(2) Thực chất của tiến hóa hóa học là quá trình phức tạp hóa các hợp chất hữu cơ từ các chất vô cơ.
(3) Quá trình hình thành các hợp chất vô cơ từ chất hữu cơ bằng con đường hóa học.
(4) Năm 1950, Fox và cộng sự đã chứng minh được các protein nhiệt có thể tự hình thành các axit amin mà không cần đến các cơ chế dịch mã.
A. 1
B. 2
C. 3
D. 4
Viết chương trình C++ mỗi công thức hoá học đều được biểu diễn bởi một dãy từng nhóm kí hiệu hoá học các nguyên tố ( mỗi nguyên tố là một kí tự) tiếp theo là một số nguyên mô tả số lượng của các nguyên tử của nguyên tố đó. Số 1 được bỏ qua khi chỉ có một nguyên tử của nguyên tố hiện diện trong công thức. Hãy tính các nguyên tử trong công thức hoá học.
Phân tử của hợp chất A gồm: 1 nguyên tử của nguyên tố X liên kết với 4 nguyên tử H và nặng gấp 8 lần phân tử hiđro. Xác định nguyên tố X và viết công thức hoá học của hợp chất A.
Ta có công thức: X=8H4 =\(8\times1\times4\)=32 đvC
=>X là lưu huỳnh
vậy CTHH là SH4
Viết công thức cấu tạo dạng đầy đủ của các hydrocarbon có công thức phân tử là CH4, C2H6 và C3H8. Dự đoán tính chất hoá học của các chất dựa vào đặc điểm liên kết của chúng.
Tham khảo:
- CH4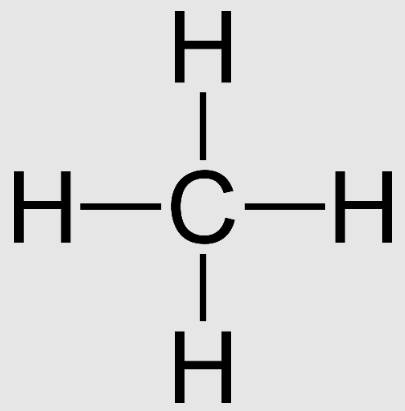
- C2H6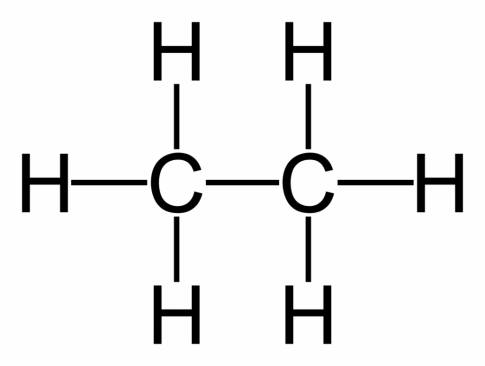
- C3H8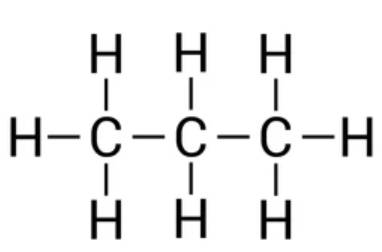
Trong phân tử alkane chỉ có các liên kết σ bền và kém phân cực. Mỗi nguyên tử carbon cũng như hydrogen đã tạo ra số liên kết cộng hoá trị lớn nhất của chúng. Vì thế, các alkane khó tham gia vào các phản ứng hoá học và phản ứng xảy ra sẽ kèm theo việc thay thế nguyên tử hydrogen hoặc bẻ gãy mạch carbon. Ở điều kiện thường, các alkane kém hoạt động, chúng không tác dụng với acid, kiềm và một số chất oxi hoá như dung dịch KMnO4, K2Cr2O7,... Các phản ứng tiêu biểu của alkane là phản ứng thế halogen (chlorine, bromine), phản ứng cracking, phản ứng reforming và phản ứng cháy.