Hãy dùng các hệ thức (12.2) và (12.3) để giải thích tại sao áp suất trong quá trình đẳng tích của một lượng khí xác định tỉ lệ thuận với nhiệt độ tuyệt đối.


Trong quá trình đẳng tích thì?
A. Thể tích của một lượng khí xác định tỉ lệ với nhiệt độ tuyệt đối.
B. Thể tích của một lượng khí không thay đổi theo nhiệt độ.
C. Thể tích tỉ lệ với nhiệt độ tuyệt đối.
D. Thể tích của một lượng khí xác định tỉ lệ nghịch với nhiệt độ tuyệt đối.
A. Thể tích của một lượng khí xác định tỉ lệ với nhiệt độ tuyệt đối.
Một binh kín chứa một lượng khí ở nhiệt độ 27 độ C và áp suất 1 atm. Hãy vẽ đồ thị biểu diễn sự biến thiên của áp suất theo nhiệt độ trong quá trình nung nóng đẳng tích lên tới nhiệt độ 127 độ C trong hệ tọa độ áp suất-nhiệt độ tuyệt đối (p, T)
Các câu sau đây, có bao nhiêu câu đúng,
(1). Trong quá trình đẳng tích, áp suất cuả một lượng khí tỉ lệ với nhiệt độ.
(2). Trong quá trình đẳng tích khi nhiệt độ tăng từ 200oC lên 400oC thì áp suất tăng lên gấp đôi.
(3). Trong quá trình đẳng tích khi nhiệt độ tăng từ 200K lên 400K thì áp suất tăng lên gấp đôi
(4). Đường biểu diễn quá trình đẳng tích trong hệ toạ độ (p, T) là đường thẳng có đường kéo dài đi qua gốc toạ độ.
A. 4
B. 1
C. 3
D. 2
Đáp án: C
Trong nhiệt giai Ken-vin, công thức của định luật Sác-lơ là: p T = hằng số.
→ phát biểu (1), (3) đúng, phát biểu (2) sai vì từ 200oC lên 400oC tương ứng với 473K lên 673K, không tăng gấp đôi được.
Đường đẳng tích (p, T) là nửa đường thẳng có đường kéo dài đi qua gốc tọa độ → (4) đúng.
trong quá trình đẳng áp, khối lượng riêng của khí và nhiệt độ tuyệt đối có công thức liên hệ:
A. 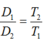
B. 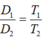
C. 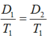
D. Cả A, B, C đều đúng
Cho một lượng khí có thể tích 30 lít ở áp suất 0,75 at được nén đẳng nhiệt đến thể tích 10 lít. Xác định áp suất của một lượng khí lúc này và vẽ đồ thị mô tả quá trình trên trong hệ tọa độ ( P, v)
Trạng thái 1: \(\left\{{}\begin{matrix}p_1=0,75atm\\V_1=30l\end{matrix}\right.\)
Trạng thái 2: \(\left\{{}\begin{matrix}p_2=???\\V_2=10l\end{matrix}\right.\)
Quá trình đẳng nhiệt:
\(p_1V_1=p_2V_2\Rightarrow0,75\cdot30=p_2\cdot10\)
\(\Rightarrow p_2=2,25atm\)
Một khối khí lí tưởng có thể tích 10 lít, áp suất 2 atm, nhiệt độ 87 độ C thực hiện biến đổi theo 2 quá trình liên tiếp: quá trình 1 đẳng áp, nhiệt độ tuyệt đối giảm 2 lần. Quá trình 2: đẳng nhiệt, áp suất sau cùng là 0,5 atm. Thể tích sau cùng của khối khí trên là bao nhiêu
Tóm tắt đề bài như sau:
\(\left\{{}\begin{matrix}V=10\left(l\right)\\p=2\left(atm\right)\\T=87+273=360\left(K\right)\end{matrix}\right.\underrightarrow{Đẳngáp}\left\{{}\begin{matrix}V_1=?\\p_1=2\left(atm\right)\\T_1=\dfrac{T}{2}=180\left(K\right)\end{matrix}\right.\) \(\underrightarrow{Đẳngnhiet}\left\{{}\begin{matrix}V_2=?\\p_2=0,5\left(atm\right)\\T_2=180\left(K\right)\end{matrix}\right.\)
Phương trình trạng thái khí lí tưởng ( Claperon Mendeleep ): \(\dfrac{pV}{T}=const\)
Đẳng áp: \(\dfrac{V}{T}=\dfrac{V_1}{T_1}\Leftrightarrow V_1=\dfrac{10.180}{360}=5\left(l\right)\)
Đẳng nhiệt: \(p_1V_1=p_2V_2\Rightarrow V_2=\dfrac{p_1V_1}{p_2}=\dfrac{2.5}{0,5}=20\left(l\right)\)
Vậy thể tích sau cùng của khối khí trên là V2=20(l)
Một lượng khí lúc đầu có các thông số trạng thái p1,V1,T1. Lượng khí biến đổi đẳng áp đến thể tích tăng 2 lần thì biến đổi đẳng tích, sao cho nhiệt độ bằng 1,5 lần nhiệt độ ở cuối quá trình đẳng áp. Nhiệt độ và áp suất của khí ở cuối quá trình là bao nhiêu?
Mối liên hệ giữa áp suất, thể tích và nhiệt độ của một lượng khí trong quá trình nào sau đây không được xác định bằng phương trình trạng thái của khí lí tưởng?
A. Dùng tay bóp méo quả bóng bay.
B. Nung nóng một lượng khí trong xi-lanh kín có pit-tông làm khí nóng lên, nở ra, đẩy pit-tông di chuyển;
C. Nung nóng một lượng khí trong một bình đậy kín;
D. Nung nóng một lượng khí trong một bình không đậy kín;
Đáp án: D
Phương trình trạng thái của khí lí tưởng được dùng cho một lượng khí xác định, do vậy khi nung nóng một lượng khí trong một bình không đậy kín thì lượng khí có khối lượng thay đổi → không thể áp dụng phương trình trạng thái khí lí tưởng cho trường hợp này.
Hãy dùng thuyết động học phân tử chất khí để giải thích tại sao chất khí gây áp suất lên thành bình và tại sao áp suất này lại tỉ lệ nghịch với thể tích chất khí.
Các phân tử khí trong thành bình chuyển động hoàn toàn hỗn độn. Khi va chạm với thành bình các phân tử khí bị phản xạ và truyền động lượng cho thành bình. Mỗi phân tử khí tác dụng lên thành bình một lực rất nhỏ, nhưng vô số phân tử khí cùng tác dụng lên thành bình sẽ gây ra một lực tác dụng đáng kể. Lực này tạo ra áp suất chất khí lên thành bình.
Áp suất chất khí tác dụng lên thành bình càng lớn khi càng có nhiều phân tử cùng tác dụng lên một đơn vị diện tích thành bình. Số các phân tử khí tác dụng lên một đơn vị diện tích thành binh phụ thuộc vào số phân tử khí có trong một đơn vị thể tích, nghĩa là phụ thuộc vào mật độ phân tử khí. Với một lượng khí nhất định thì mật độ khí tỉ lệ nghịch với thế tích khí (n = N/V, trong đó n là mật độ phân tử, N là số phân tử khí có trong thể tích V). Do đó, áp suất của chất khí tác dụng lên thành bình tỉ lệ nghịch với thể tích V.
(Chú ỷ : Áp suất chất khí tác dụng lên thành bình còn phụ thuộc các yếu tố khác mà chúng ta chưa xét ở đây).
Trong một quá trình biến đổi trạng thái của một lượng khí xác định néu có cả áp xuất và nhiệt độ tuyệt đối đều tăng gắp đôi thì thể tích của khí đó sẽ thay đồi như thế nào
V thay đổi mất một nửa là nhiệt độ tuyệt đối tăng gấp đôi mà V khí tỉ lệ nghịch nên V mất một nửa á.