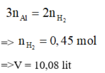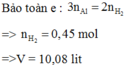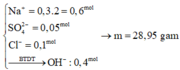Hòa tan một lượng Na dư vào 25 gam dung dịch H2SO4 9,8%. Tính thể tích H2 (đktc) thoát ra (coi hiệu suất các phản ứng đạt 100%)

Những câu hỏi liên quan
Cho một lượng bột nhôm dư vào 100 gam dung dịch H2SO4 9,8%
a) Tính khối lượng nhôm phản ứng
b) Tính thể tích khí thoát ra ở đktc
c) Tính nồng độ % muối nhôm
2Al+3H2SO4->Al2(SO4)3+3H2(khí)
mH2SO4=100*9.8:100=9.8(g)
nH2SO4=0.1(mol)
theo pthh:nAl=2/3 nH2SO4->nAl=2/3*0.1=0.07(mol)
mAl=0.07*27=1.89(g)
theo pthh:nH2=nH2SO4->nH2=0.1(mol)
VH2=0.1*22.4=2.24(l)
Theo pthh:nAl2(SO4)3=1/3 nH2SO4->nAl2(SO4)3=0.03(mol)
m muối=0.03*342=10.26(g)
mdd=1.89+100-0.1*2=101.69(g)
C% muối:10.26:101.69*100=10.09%
Đúng 0
Bình luận (0)
A là hỗn hợp của Na, Mg, Al
- Cho a gam A vào nước dư phản ứng xong thoát ra 4,48 lít khí H2
- Cho a gam A vào dung dịch Ba(OH)2 dư thấy thoát ra 7,84 lít khí H2
- Cho a gam A vào dung dịch H2SO4 dư thoát ra 11,2 lít khí H2
Hãy tính a và phần trăm khối lượng của mỗi kim loại trong hỗn hợp ban đầu( biết thể tích các khí đo ở ĐKTC)
HD:
Thí nghiệm 1 chỉ có Na phản ứng:
Na + HOH \(\rightarrow\) NaOH + 1/2H2 (1)
0,4 0,2 mol
Thí nghiệm 2 chỉ có Al phản ứng (kim loại lưỡng tính):
Al + OH- + H2O \(\rightarrow\) AlO2- + 3/2H2 (2)
0,7/3 0,35 mol
Thí nghiệm 3 cả 3 chất đều phản ứng:
2Na + H2SO4 \(\rightarrow\) Na2SO4 + H2 (3)
Mg + H2SO4 \(\rightarrow\) MgSO4 + H2 (4)
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2 (5)
Gọi x, y, z tương ứng là số mol của Na, Mg và Al trong a gam hh.
Ta có: x = 0,4 mol; z = 0,7/3 mol; x/2 + y + 3z/2 = 0,5. Suy ra: y = -0.5 < 0 (vô lí)
Bạn xem lại đề bài, đề bài ko đúng.
Đúng 0
Bình luận (0)
Do ở thí nghiệm 2 nH2 > n H2 thí nghiệm 1 -> ở thí nghiệm 1 NaOH hết ( Nếu NaOH dư thì nH2 ở 2 thí nghiệm đầu phải bằng nhau)
gọi a là số mol na b là số mol al c là số mol mg
Thí nghiệm 1 : Na+H20 - Naoh+1/2 H2
a a a/2
Al+naoh+h20-> naal02+3/2 H2
a 3/2a (do Naoh hết)
Vậy a/2+3/2 a = 0.2-> a=0.1
Thí nghiệm 2 : Na+h20 - naoh +1/2 H2
a a/2
Al+Oh-+h20--> alo2-+3/2 H2
b 3/2 b
a/2 +3/2 b = nH2=0.35-> b=0.2
Thí nghiệm 3: nH2 =0.5 = a/2+3/2b+c--> c =0.15
Vậy hh A gồm 0.1 Na 0.2 Al 0.15 Mg
Đúng 0
Bình luận (0)
Hòa tan 6,5 gam kẽm bằng dung dịch H2SO4 19.6% vừa đủ a)Tính thể tích khí H2 thoát ra (đktc) b) Tính nồng độ % của dung dịch sau phản ứng
a) \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + H2SO4 ---> ZnSO4 + H2
0,1--->0,1------->0,1------>0,1
=> \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
b) \(m_{\text{dd}H_2SO_4}=\dfrac{0,1.98}{19,6\%}=50\left(g\right)\)
=> \(m_{\text{dd}.sau.p\text{ư}}=50+6,5-0,1.2=56,3\left(g\right)\)
=> \(C\%_{ZnSO_4}=\dfrac{0,1.161}{56,3}.100\%=28,6\%\)
Đúng 1
Bình luận (0)
Hòa tan 8,1 gam Al bằng một lượng dung dịch H2SO4 loãng dư. Sau phản ứng thoát ra V lít khí H2 (ở đktc). Giá trị của V là
A. 4,48 lít
B. 5,6 lít
C. 6,72 lít
D. 10,08 lít
Hòa tan 8,1 gam Al bằng một lượng dung dịch H2SO4 loãng dư. Sau phản ứng thoát ra V lít khí H2 (ở đktc). Giá trị của V l
A. 4,48 lít
B. 6,72 lít
C. 10,08 lít
D. 5,6 lít
Đáp án : C
Bảo toàn e : 3nAl = 2 n H 2
=> n H 2 = 0,45 mol
=> V H 2 = 10,08 lit
Đúng 0
Bình luận (0)
Hòa tan 8,1 gam Al bằng một lượng dung dịch H2SO4 loãng dư. Sau phản ứng thoát ra V lít khí H2 (ở đktc). Giá trị của V là
A. 4,48 lít
B. 5,6 lít
C. 6,72 lít
D. 10,08 lít
Hoà tan canxi cacbonat vào 200ml dung dịch axit axetic 1M a. Tính thể tích khí thoát ra ở đktc b. Đun nóng 50ml dung dịch axít trên với 23g rượu etylíc có xúc tác H2SO4 đặc. Tính khối lượng este thu được. Biết hiệu suất phản ứng đạt 80%
\(CaCO_3+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Ca+CO_2+H_2O\\ a,n_{CH_3COOH}=0,2.1=0,2\left(mol\right)\Rightarrow n_{CO_2}=\dfrac{0,2}{2}=0,1\left(mol\right)\Rightarrow V_{CO_2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\\ b,CH_3COOH+C_2H_5OH⇌\left(H^+,t^o\right)CH_3COOC_2H_5+H_2O\\ n_{CH_3COOH}=\dfrac{50}{200}.0,2=0,05\left(mol\right)\\ n_{C_2H_5OH}=\dfrac{23}{46}=0,5\left(mol\right)\\ Vì:\dfrac{0,5}{1}>\dfrac{0,05}{1}\Rightarrow Rượu.dư\\ \Rightarrow n_{este\left(LT\right)}=n_{axit}=0,05\left(mol\right)\\ \Rightarrow n_{este\left(TT\right)}=80\%.0,05=0,04\left(mol\right)\\ m_{CH_3COOC_2H_5}=88.0,04=3,52\left(g\right)\)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn a gam Na vào 100 ml dung dịch Y gồm H2SO4 0,5M và HCl 1M, thấy thoát ra 6,72 lít H2 (đktc). Cô cạn dung dịch sau phản ứng thu được m gam chất rắn khan. Giá trị của m gần nhất với
A. 23.
B. 21.
C. 13.
D. 29.
Hòa tan hoàn toàn a gam Na vào 100 ml dung dịch Y gồm H 2 S O 4 0,5M và HCl 1M, thấy thoát ra 6,72 lít khí H 2 đktc. Cô cạn dung dịch sau phản ứng thu được m gam rắn khan. Giá trị gần nhất của m là
A. 23
B. 21
C. 13
D. 29