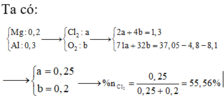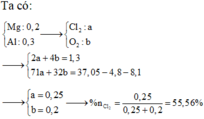C1: Cho 3,6g Mg va 2,7g Al tác dụng vừa đủ với V l (dktc) Cl2 và O2. Biết dx/h2=22,5. Tìm v

Những câu hỏi liên quan
Cho hỗn hợp X gồm 4,08g Mg và 2,7g Al tác dụng vừa đủ với V lít (đktc) hỗn hợp khí Y gồm Cl2 và O2(có tỉ khối so với H2 là 23,8), thu được m gam hỗn hợp rắn Z. Giá trị m là
\(n_{Mg}=\dfrac{4,08}{24}=0,17\left(mol\right)\)
\(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
Gọi số mol Cl2 và O2 là a, b
Mg0-2e-->Mg+2
0,17->0,34
Al0-3e-->Al+3
0,1->0,3
Cl20 +2e--> 2Cl-
a--->2a
O20 +4e --> 2O2-
b--->4b
Bảo toàn e: 2a + 4b = 0,64
Có \(\dfrac{71a+32b}{a+b}=23,8.2=47,6\)
=> a = 0,08; b = 0,12
=> mZ = 4,08 + 2,7 + 0,08.71 + 0,12.32 = 16,3 (g)
Đúng 1
Bình luận (0)
Cho 6,72 lít (đktc) hỗn hợp X gồm O 2 , C l 2 có d X / H 2 = 22 , 5 tác dụng vừa đủ với m (g) hỗn hợp Y gồm Al và Zn thu được 31,9 gam hỗn hợp B gồm muối clorua và oxit của 2 kim loại. Tính m và %m mỗi chất trong Y?
Cho 6,72 lít hỗn hợp X ( O2 và Cl2 ) có tỉ khối so với H2 là 22,5 tác dụng vừa đủ với hỗn hợp Y ( Al và Mg ) thu được 23,7 gam hh clorua và oxit của hai kim loại. Tính % về khối lượng các chất trong X và Y.
*) Xét 6,72 lít hỗn hợp X. Gọi số mol O2 và Cl2 lần lượt là x, y mol.
nhh=0,3mol;
¯M=22,5.2=45
Khi đó ta có hpt:
x+y=0,3
¯M=32x+71y\x+y=45
→{x=0,2y=0,1mol
⇒%mO2=0,2.32\0,2.32+0,1.71.100%=47,4%;%mCl2=100−47,4=52,6%
*) Gọi số mol Al và Mg lần lượt là a, b mol →
số mol AlCl3và MgCl2 lần lượt là a, b mol →
Các quá trình cho và nhận e:
Al0→Al+3+3e; Mg0→Mg+2+2e
O2+4e→2O2−;Cl2+2e→2Cl−
Bảo toàn e: 3a+2b=0,2.4+0,1.2=1 (1)
Mà hỗn hợp clorua và oxit của hai kim loại có khối lượng 23,7g
BTKL: → 27a+24b+45.0,3=23,7 (2)
Từ (1), (2) ta được: →{a=0,2
b=0,2mol
⇒ %mAl=0,2.27\0,2.27+0,2.24.100%=52,94%→%mMg=47,06%
Xét 6,72 lít hỗn hợp X. Gọi số mol O2O2 và Cl2Cl2 lần lượt là x, y mol.
\(n_{hh}=0,3\left(mol\right);\overline{M}=22,5.2=45\)
Khi đó ta có hpt:
\(\left\{{}\begin{matrix}x+y=0,3\\\overline{M}=\frac{32x+71y}{x+y}=45\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m_{O2}=\frac{0,2.32}{0,2.32+0,1.71}.100\%=47,4\%\)
\(\Rightarrow\%m_{Cl2}=100\%-47,4\%=52,6\%\)
Gọi số mol Al và Mg lần lượt là a, b mol →số mol AlCl3 và MgCl2 lần lượt là a, b mol →
Các quá trình cho và nhận e:
\(Al^o\rightarrow Al^{+3}+3e;Mg^o\rightarrow Mg^{+2}+2e\)
\(O_2+4e\rightarrow2O^{2-};Cl_2+2e\rightarrow2Cl^-\)
Bảo toàn e:
\(3a+2b=0,2.4+0,1.2=1\left(1\right)\)
Mà hỗn hợp clorua và oxit của hai kim loại có khối lượng 23,7g
BTKL:
\(\Rightarrow27a+24n+45.0,3=23,7\left(2\right)\)
\(\left(1\right)+\left(2\right)\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\b=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m_{Al}=\frac{0,2.27}{0,2.27+0,2.44}.100\%=52,94\%\)
\(\Rightarrow\%m_{Mg}=100\%-52,94\%=47,06\%\)
Cho hỗn hợp X gồm AI và Mg tác dụng vừa đủ với 1,344 lít (đktc) hỗn hợp khí Y gồm
O
2
và
Cl
2
.
d
Y
/
H
2
27,375 . Sau phản ứng thu được 5,055 gam chất rắn. Tính khối lượng của Al và Mg trong hỗn hợp ban đầu...
Đọc tiếp
Cho hỗn hợp X gồm AI và Mg tác dụng vừa đủ với 1,344 lít (đktc) hỗn hợp khí Y gồm O 2 và Cl 2 . d Y / H 2 = 27,375 . Sau phản ứng thu được 5,055 gam chất rắn. Tính khối lượng của Al và Mg trong hỗn hợp ban đầu.
- Từ giả thiết tính được : n Cl 2 = 0,035 mol; n O 2 = 0,025 mol
Theo ĐLBT khối lượng :
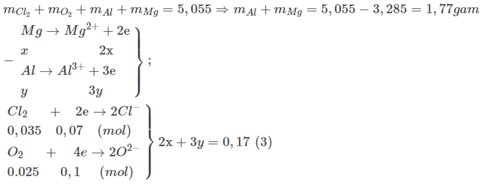
Từ (3)(4) ⇒ x = 0,04; y = 0,03
⇒ m Mg = 0,04.24 = 0,96g; m Al = 0,03.27 = 0,81g
Phản ứng không oxi hoá - khử
Đúng 0
Bình luận (0)
Cho 20,4g hỗn hợp X gồm Al , Zn và Fe tác dụng với dung dịch HCl dư thu được 10,08 lit H2. Mặt khác 0,2 mol hỗn hợp X tác dụng vừa đủ với 6,16 lit Cl2. Tính thành phần % về khối lượng của Al trong hỗn hợp X ( biết khí thu được đều đo ở dktc) A. 33,09% B. 26,47% C. 19,85% D. 13,24%
Đọc tiếp
Cho 20,4g hỗn hợp X gồm Al , Zn và Fe tác dụng với dung dịch HCl dư thu được 10,08 lit H2. Mặt khác 0,2 mol hỗn hợp X tác dụng vừa đủ với 6,16 lit Cl2. Tính thành phần % về khối lượng của Al trong hỗn hợp X ( biết khí thu được đều đo ở dktc)
A. 33,09%
B. 26,47%
C. 19,85%
D. 13,24%
Đáp án : D
Gọi số mol Al ; Zn ; Fe lần lượt là x ; y ; z
=> 27x + 65y + 56z = 20,4 (1)
Và 1,5x + y + z = nH2 = 0,45 (2)
Xét 0,2 mol X có lượng chất gấp t lần 20,4g X
=> t(x + y +z) = 0,2 mol (3)
Lại có : Bảo toàn e : 2nCl2 = (3x + 2y + 3z)t = 0,55 (4)
Từ (1),(2),(3),(4) => x = y = 0,1 ; z = 0,2
=> %mAl(X) = 13,24%
Đúng 0
Bình luận (0)
Cho hỗn hợp A gồm O2 và Cl2 tác dụng với hỗn hợp gồm 4,8 gam Mg và 8,1 gam Al vừa đủ thì thu được 37,05g chất rắn. Tỷ lệ phần trăm theo thể tích của Cl2 và O2 trong hỗn hợp A là A. 45,56%; 54,44% B. 55,56%; 44,44% C. 44,44%; 55,56% D. 54,44%; 45,56%.
Đọc tiếp
Cho hỗn hợp A gồm O2 và Cl2 tác dụng với hỗn hợp gồm 4,8 gam Mg và 8,1 gam Al vừa đủ thì thu được 37,05g chất rắn. Tỷ lệ phần trăm theo thể tích của Cl2 và O2 trong hỗn hợp A là
A. 45,56%; 54,44%
B. 55,56%; 44,44%
C. 44,44%; 55,56%
D. 54,44%; 45,56%.
Cho hỗn hợp A gồm O2 và Cl2 tác dụng với hỗn hợp gồm 4,8 gam Mg và 8,1 gam Al vừa đủ thì thu được 37,05g chất rắn. Tỷ lệ phần trăm theo thể tích của Cl2 và O2 trong hỗn hợp A là A. 45,56%; 54,44% B. 55,56%; 44,44% C. 44,44%; 55,56% D. 54,44%; 45,56%.
Đọc tiếp
Cho hỗn hợp A gồm O2 và Cl2 tác dụng với hỗn hợp gồm 4,8 gam Mg và 8,1 gam Al vừa đủ thì thu được 37,05g chất rắn. Tỷ lệ phần trăm theo thể tích của Cl2 và O2 trong hỗn hợp A là
A. 45,56%; 54,44%
B. 55,56%; 44,44%
C. 44,44%; 55,56%
D. 54,44%; 45,56%.
Cho hỗn hợp A gồm O2 và Cl2 tác dụng với hỗn hợp gồm 4,8 gam Mg và 8,1 gam Al vừa đủ thì thu được 37,05g chất rắn. Tỷ lệ phần trăm theo thể tích của Cl2 và O2 trong hỗn hợp A là A. 45,56%; 54,44% B. 55,56%; 44,44% C. 44,44%; 55,56% D. 54,44%; 45,56%.
Đọc tiếp
Cho hỗn hợp A gồm O2 và Cl2 tác dụng với hỗn hợp gồm 4,8 gam Mg và 8,1 gam Al vừa đủ thì thu được 37,05g chất rắn. Tỷ lệ phần trăm theo thể tích của Cl2 và O2 trong hỗn hợp A là
A. 45,56%; 54,44%
B. 55,56%; 44,44%
C. 44,44%; 55,56%
D. 54,44%; 45,56%.
Cho 5,4g AL tác dụng vừa đủ với V lít khí Cl2 ở đktc. Tìm v và tìm khối lượng sản phẩm?
\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\\ 2Al+3Cl_2\underrightarrow{^{to}}2AlCl_3\\ n_{Cl_2}=\dfrac{3}{2}.0,2=0,3\left(mol\right)\\ \Rightarrow V=V_{Cl_2\left(đktc\right)}=0,3.22,4=6,72\left(l\right)\\ n_{AlCl_3}=n_{Al}=0,2\left(mol\right)\\ \Rightarrow m_{AlCl_3}=0,2.133,5=26,7\left(g\right)\)
Đúng 3
Bình luận (0)